下载高清试卷
【2019年广东省深圳市中考化学试卷】-第1页
试卷格式:2019年广东省深圳市中考化学试卷.PDF
试卷热词:最新试卷、2019年、广东试卷、深圳市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.化学与人类的生产、生活密切相关。下列描述正确的是( )
- A. 引起贫血的主要原因是缺锌
- B. 不合理施用化肥会造成水体污染
- C.
 是电池回收标志
是电池回收标志 - D. 用水喷淋燃着的酒精以降低着火点
2.下列化学用语表述正确的是( )
- A. 硫酸钾的化学式:K2SO4
- B. 1 个氯分子:Cl
- C. 2 个硝酸根:2NO2
- D. 铜离子:
+2 Cu
3.下列实验不涉及化学变化的是( )
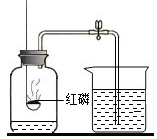 | 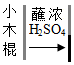 | 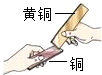 | 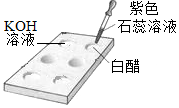 |
| A.测定空气中O2的含量 | B.验证浓H2SO4的腐蚀性 | C.比较合金与纯金属的硬度 | D.判断溶液的酸碱性 |
- A. A
- B. B
- C. C
- D. D
4.钪(Kc)是一种"工业的维生素"。下图为钪在元素周期表中的相关信息及其原子的结构示意图。下列说法正确的是( )
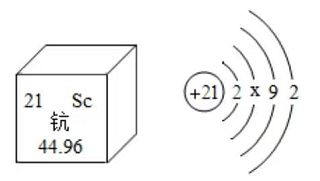

- A. 钪属于非金属元素

- B. 钪的相对原子质量是21
- C. 原子结构示意图中x=10

- D. 钪原子核外有四个电子层
5.科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为CH2O),该反应过程的微观示意图如下。下列说法正确的是( )
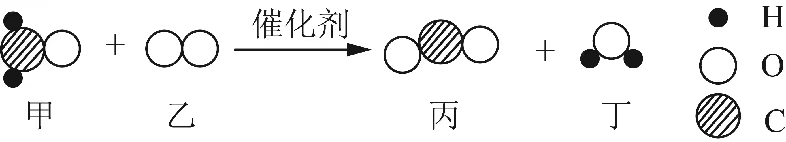

- A. 物质甲为甲醛,其分子由碳原子和水分子构成
- B. 物质乙中氧元素的化合价为-2价
- C. 该反应前后原子种类和数目均发生改变
- D. 该反应消耗物质甲和生成物质丁的质量比为5:3
6.CuO粉末与H2在加热条件下会发生反应。下列说法错误的是( )
- A. 反应所需H2可由Cu与稀H2SO4反应制得
- B. 反应过程可观察到固体粉末由黑色变成红色
- C. 发生的反应为CuO+H2Cu+H2O
△ - D. 该反应说明H2具有还原性
7.异烟肼(化学式:C6H7N3O;相对分子质量:137)是治疗肺结核药物的有效成分.下列说法正确的是( )
- A. 异烟肼属于氧化物
- B. 异烟肼分子中H、O原子个数比为7:1
- C. 异烟肼中C、H两种元素的质量比为36:7
- D. 异烟肼中N元素质量分数的计算式为×100%
14 137
8.为达到以下实验目的,下列相应实验方案合理的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 获得廉价的新能源 | 电解水制H2 |
| B | 将河水净化为纯水 | 经沉淀、过滤、吸附 |
| C | 验证金属活动性Zn>Cu | 利用Zn片与CuSO4溶液的反应 |
| D | 除去NaCl固体中少量的MgCl2 | 加水溶解,再加入过量NaOH溶液 |
- A. A
- B. B
- C. C
- D. D
9.现有t2℃时的溶液Ⅰ、Ⅱ各100g,溶液Ⅰ中含物质甲50g,溶液Ⅱ是物质乙的饱和溶液.物质甲、乙(均不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
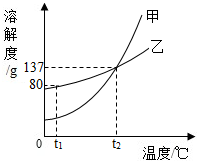

- A. t2℃时,溶液Ⅰ是甲的饱和溶液
- B. t2℃时,溶液Ⅰ中甲的质量分数为50%
- C. t2℃时,溶液Ⅱ中含乙37g
- D. 从t2℃降温至t1℃时,乙不会从溶液Ⅱ中析出
10.关系图中"一"两端的物质能发生化学反应,"→"表示物质的转化方向。下列说法错误的是( )
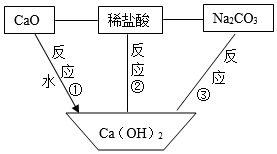

- A. 反应①放出热量
- B. 反应②所得的溶液可呈中性
- C. 反应③可得NaOH
- D. 不能将图中稀盐酸换为稀H2SO4
11.生铁用途十分广泛.工业上利用赤铁矿(主要成分是Fe2O3,还含少量SiO2等杂质)冶炼生铁的过程如下:

回答下列问题:
(1)生铁属于 材料(填“合成”或“金属”)。“高炉气体”中的 (填化学式)会导致酸雨。
(2)“煅烧”时:
①生成CO的反应之一为C+CO2
2CO,该反应属于 反应(填基本反应类型)。
②用化学方程式表示利用CO炼铁的原理 。
③CaCO3和SiO2固体在高温条件下发生反应,生成CO2气体和CaSiO3,该反应的化学方程式为 。
(3)生活中铁制品锈蚀的过程,实际上是Fe与空气中 、 等发生化学反应的过程。下列措施能防止铁制品锈蚀的是 (填标号)。
A、涂油、喷漆 B、镀耐腐蚀的铬层
C、用盐水清洗 D、久置于酸性环境

回答下列问题:
(1)生铁属于 材料(填“合成”或“金属”)。“高炉气体”中的 (填化学式)会导致酸雨。
(2)“煅烧”时:
①生成CO的反应之一为C+CO2
| 高温 |
②用化学方程式表示利用CO炼铁的原理 。
③CaCO3和SiO2固体在高温条件下发生反应,生成CO2气体和CaSiO3,该反应的化学方程式为 。
(3)生活中铁制品锈蚀的过程,实际上是Fe与空气中 、 等发生化学反应的过程。下列措施能防止铁制品锈蚀的是 (填标号)。
A、涂油、喷漆 B、镀耐腐蚀的铬层
C、用盐水清洗 D、久置于酸性环境
12.为探究某塑料的组成元素,设计了实验Ⅰ和Ⅱ.回答下列问题:
Ⅰ.制取氧气
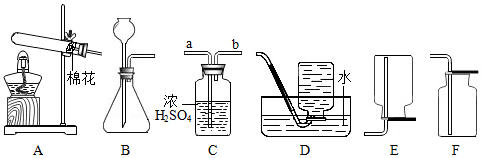
(1)若用一种暗紫色固体制取O2,发生反应的化学方程式为 ,发生装置应选择上述装置 (填标号)。
(2)欲制取干燥的O2,装置合理的连接顺序为:发生装置→C→ (填标号)。连接装置时,发生装置的出气口应与装置C中 (填“a”或“b”)端相连。
Ⅱ.组成探究
(3)定性检测(已知:无水CuSO4遇水变蓝色)
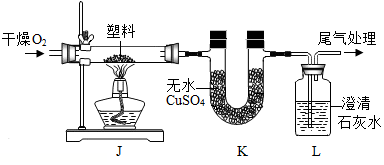
③由上述实验可知,该塑料一定含有的元素是 (填元素符号)。
(4)定量测定
为进一步确定组成,将1.4g该塑料在足量O2中完全燃烧,共产生了4.4g CO2和1.8g H2O,依据质量守恒定律,可判断该塑料 (填“含有”或“不含”)除上述③中结论之外的元素。
Ⅰ.制取氧气

(1)若用一种暗紫色固体制取O2,发生反应的化学方程式为 ,发生装置应选择上述装置 (填标号)。
(2)欲制取干燥的O2,装置合理的连接顺序为:发生装置→C→ (填标号)。连接装置时,发生装置的出气口应与装置C中 (填“a”或“b”)端相连。
Ⅱ.组成探究
(3)定性检测(已知:无水CuSO4遇水变蓝色)

| 实验操作 | 实验现象 | 结论 |
| 连接装置,检查气密性,装入试 剂并按如图进行实验。通入O2,一段时间后,点燃J处酒精灯。 | 装置K中无水CuSO4变① 色 | 塑料燃烧产物中有H2O |
| 装置L中② 。 | 塑料燃烧产物中有CO2 |
③由上述实验可知,该塑料一定含有的元素是 (填元素符号)。
(4)定量测定
为进一步确定组成,将1.4g该塑料在足量O2中完全燃烧,共产生了4.4g CO2和1.8g H2O,依据质量守恒定律,可判断该塑料 (填“含有”或“不含”)除上述③中结论之外的元素。
13.已知:①NaHCO3 固体受热分解 2NaHCO3
Na2CO3+CO2↑+H2O;②Na2CO3 受热不分解。回答下列问题:
(1)关于 NaHCO3 固体的叙述错误的是 (填标号)。
A.俗称小苏打 B.难溶于水 C.可与稀盐酸发生反应 D.是发酵粉的主要成分之一
(2)欲测定某 NaHCO3固体样品(只含Na2CO3杂质且分布均匀)中NaHCO3的质量分数,将 5.0g 该样品加热至质量不再改变,测得剩余固体的质量、生成CO2的质量随时间变化如图所示。
①NaOH溶液的pH 7(填“>”、“=”或“<”),用该溶液将生成的CO2完全吸收,发生反应的化学方程式为 。
②由图中数据可知,上述5.0g NaHCO3 样品完全分解产生CO2的质量为 g,产生H2O的质量是 g。
③计算该样品中NaHCO3的质量分数 (根据化学方程式写出完整的计算步骤)。

| △ |
(1)关于 NaHCO3 固体的叙述错误的是 (填标号)。
A.俗称小苏打 B.难溶于水 C.可与稀盐酸发生反应 D.是发酵粉的主要成分之一
(2)欲测定某 NaHCO3固体样品(只含Na2CO3杂质且分布均匀)中NaHCO3的质量分数,将 5.0g 该样品加热至质量不再改变,测得剩余固体的质量、生成CO2的质量随时间变化如图所示。
①NaOH溶液的pH 7(填“>”、“=”或“<”),用该溶液将生成的CO2完全吸收,发生反应的化学方程式为 。
②由图中数据可知,上述5.0g NaHCO3 样品完全分解产生CO2的质量为 g,产生H2O的质量是 g。
③计算该样品中NaHCO3的质量分数 (根据化学方程式写出完整的计算步骤)。

查看全部题目