下载高清试卷
【2019年上海市中考化学试卷】-第1页
试卷格式:2019年上海市中考化学试卷.PDF
试卷热词:最新试卷、2019年、上海试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.属于稀有气体的是( )
- A. 氮气
- B. 氦气
- C. 氢气
- D. 氧气
2.能使紫色石蕊试液变蓝的是( )
- A. 水
- B. 石灰水
- C. 稀硫酸
- D. 稀盐酸
3.灼烧氯化钠,火焰呈( )
- A. 黄色
- B. 红色
- C. 绿色
- D. 紫鱼
4.能提供氮元素的化肥是( )
- A. KCl
- B. K2CO3
- C. NH4Cl
- D. Ca(H2PO4)2
5.Fe2O3中Fe的化合价是( )
- A. -3
- B. -2
- C. +2
- D. +3
6.放入一定量水中,充分搅拌后形成乳浊液的是( )
- A. 蔗糖
- B. 麻油
- C. 食盐
- D. 白醋
7.图示实验操作规范的是( )
- A.
取用液体
- B.
滴加液体
- C.
量筒读数
- D.
加热液体
8.净水过程中可加入的吸附剂是( )
- A. 活性炭
- B. 生石灰
- C. 熟石灰
- D. 烧碱
9.在氧气中燃烧,产生明亮蓝紫色火焰的是( )
- A. 硫
- B. 红磷
- C. 铁丝
- D. 氢气
10.瓶中CO气体分子的微观示意图为(“ ”表示C原子,“
”表示C原子,“  ”表示O原子)( )
”表示O原子)( )
 ”表示C原子,“
”表示C原子,“  ”表示O原子)( )
”表示O原子)( )- A.
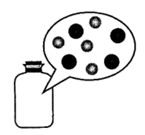
- B.
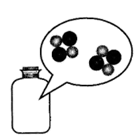
- C.
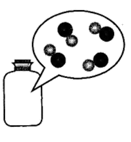
- D.

11.有关CuSO4说法正确的是( )
- A. 俗称胆矾
- B. 可检验水的存在
- C. 摩尔质量为160
- D. 不含原子团
12.一定条件下,能与二氧化碳反应的是( )
- A. 木炭
- B. 一氧化碳
- C. 氧化铜
- D. 氧气
13.能鉴别氢氧化钠溶液和碳酸钠溶液的是( )
- A. 酚酞试液
- B. 盐酸
- C. 氢氧化钾溶液
- D. 碳酸钾溶液
14.实验室制氧气的化学方程式书写正确的是( )
- A. KClO3KCl+O2↑
催化剂 △ - B. 2KClO3 2KCl+3O2↑
△ - C. 2H2O22H2O+O2↑
MnO2 - D. H2O2H2↑+O2↑
MnO2
15.能使气体物质溶解度增大的操作是( )
- A. 增加溶剂
- B. 振荡溶液
- C. 增大压强
- D. 升高温度
16.燃烧前常将汽油(含C8H18等)喷成雾状,可以( )
- A. 减少O2消耗量
- B. 增大汽油与空气的接触面积
- C. 减少CO2生成量
- D. 使C8H18等分子变得更小
17.只含一种分子的物质一定是( )
- A. 单质
- B. 化合物
- C. 纯净物
- D. 混合物
18.25℃时,pH=1的盐酸与pH=13的氢氧化钠溶液混合,立即测定混合液的温度T,然后测定混合液的pH(25℃时)。有关判断合理的是( )
- A. T=25℃ pH=7
- B. T=25℃ 1≤pH≤13
- C. T>25℃ pH=14
- D. T>25℃ 1<pH<13
19.含氧元素质量相同的SO2和SO3 , 具有相同的( )
- A. 硫元素质量
- B. 质量
- C. 氧原子个数
- D. 分子个数
20.一定量甲烷(CH4)在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水的物质的量之比可能为( )
- A. 1:1:2
- B. 2:1:4
- C. 2:3:6
- D. 3:1:8
21.新中国成立70年来,我国化学工业得到长足发展。
(1)积极开发燃料酒精等石油替代品。酒精(C2H6O)由 种元素组成,属于 (选填"有机物"或"无机物")。酒精燃烧属于 (选填"物理"或"化学")变化。
(2)人造金刚石世界闻名。金刚石硬度大,可用于 。金刚石、 (填物质名称)和碳60互为同素异形体,其中碳元素以 (选填"游离"或"化合")态存在。
(3)光伏产品遍及全球。生产中涉及反应:SiO2+2C
Si+2X↑。X的化学式是 。1molSiO2中约含 个Si原子。
(1)积极开发燃料酒精等石油替代品。酒精(C2H6O)由 种元素组成,属于 (选填"有机物"或"无机物")。酒精燃烧属于 (选填"物理"或"化学")变化。
(2)人造金刚石世界闻名。金刚石硬度大,可用于 。金刚石、 (填物质名称)和碳60互为同素异形体,其中碳元素以 (选填"游离"或"化合")态存在。
(3)光伏产品遍及全球。生产中涉及反应:SiO2+2C
| 高温 |
22.实验室制备并收集二氧化碳。
(1)选用药品:按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如下图所示:

图中丙对应实验 (选填"I""Ⅱ"或"Ⅲ")。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是 ;不用甲对应的药品,理由是 。
(2)搭建装置:组装简易启普发生器,应选用 (选填编号)。

(3)收集二氧化碳:用下图装置收集时,空气从 (选填"X"或"Y")端排出。

(4)检验二氧化碳:写出检验时反应的化学方程式 。
(1)选用药品:按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如下图所示:
| 实验编号 | 药品 |
| Ⅰ | 块状大理石、10%H2SO4溶液 |
| Ⅱ | 块状大理石、7%HC1溶液 |
| Ⅲ | 大理石粉末、7%HC1溶液 |

图中丙对应实验 (选填"I""Ⅱ"或"Ⅲ")。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是 ;不用甲对应的药品,理由是 。
(2)搭建装置:组装简易启普发生器,应选用 (选填编号)。

(3)收集二氧化碳:用下图装置收集时,空气从 (选填"X"或"Y")端排出。

(4)检验二氧化碳:写出检验时反应的化学方程式 。
23.研究物质的溶解对于生产、生活有着重要意义。
(1)下表是硝酸钾的部分溶解度数据。
由表中数据可知,硝酸钾的溶解度随温度升高而 (选填“变大”或“变小”)。60℃时硝酸钾饱和溶液中,溶质与溶剂的质量比为 ,能将该饱和溶液转化为不饱和溶液的一种方法是 。
(2)探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如下图所示:

坐标图中,符合实验结果的描点可能是 (选填编号)。

(3)取等质量甲和乙两种物质(均不含结晶水)进行如下图所示实验,最终烧杯中析出固体的质量乙大于甲。

40℃时,甲的溶解度 (选填“大于”“等于”或“小于”)乙的溶解度。根据本实验结果,能否判断40~80℃间甲、乙哪种物质的溶解度变化随温度影响更大 (选填“能”或“不能”)。
(1)下表是硝酸钾的部分溶解度数据。
| 温度(℃) | 20 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 31. 6 | 63. 9 | 110 | 169 |
由表中数据可知,硝酸钾的溶解度随温度升高而 (选填“变大”或“变小”)。60℃时硝酸钾饱和溶液中,溶质与溶剂的质量比为 ,能将该饱和溶液转化为不饱和溶液的一种方法是 。
(2)探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如下图所示:

坐标图中,符合实验结果的描点可能是 (选填编号)。

(3)取等质量甲和乙两种物质(均不含结晶水)进行如下图所示实验,最终烧杯中析出固体的质量乙大于甲。

40℃时,甲的溶解度 (选填“大于”“等于”或“小于”)乙的溶解度。根据本实验结果,能否判断40~80℃间甲、乙哪种物质的溶解度变化随温度影响更大 (选填“能”或“不能”)。
24.某混合溶液含一定量的硝酸银、硝酸铜和硝酸钡,为逐一沉淀分离其中的金属元素,从稀盐酸、稀硫酸、氢氧化钠稀溶液、氯化钠溶液、硫酸钠溶液中选择试剂进行实验。
(1)甲的实验如下表所示:
在Ⅱ中,需确认钡元素是否完全沉淀。甲在此环节的部分实验记录如下图所示:

请根据这部分记录,指出该环节中甲存在的具体问题并说明理由。
(2)乙仅调整了甲实验中所加试剂的顺序,既达到了实验目的,理论上又减少了氢氧化钠的消耗量。乙所加试剂依次为
(3)丙设计了一种新的方案,不仅达到了实验目的,而且理论上氢氧化钠的消耗量减到最少丙所加试剂依次为
(1)甲的实验如下表所示:
| 步骤 | 操作 | 现象与解释 |
| Ⅰ | 向混合溶液中加入过量稀盐酸,充分反应后过滤 | 得到白色沉淀,相应的化学方程式是 |
| Ⅱ | 向Ⅰ中滤液加入过量稀硫酸,充分反应后过滤 | 得到 色沉淀 |
| Ⅲ | 向Ⅱ中滤液加入过量氢氧化钠稀溶液,充分反应后过滤 | 得到蓝色沉淀,该沉淀的化学式是 |
在Ⅱ中,需确认钡元素是否完全沉淀。甲在此环节的部分实验记录如下图所示:

请根据这部分记录,指出该环节中甲存在的具体问题并说明理由。
(2)乙仅调整了甲实验中所加试剂的顺序,既达到了实验目的,理论上又减少了氢氧化钠的消耗量。乙所加试剂依次为
(3)丙设计了一种新的方案,不仅达到了实验目的,而且理论上氢氧化钠的消耗量减到最少丙所加试剂依次为
25.实验室以氧化铜、铁粉和稀硫酸为原料制备铜。
(1)方法一:氧化铜
硫酸铜溶液
铜
I中反应的化学方程式是 ;Ⅱ中反应的基本类型是 。
该方法利用了铁的金属活动性比铜 (选填“强”或“弱”)。
(2)方法二:用铁粉与稀硫酸制得氢气进行如图实验。
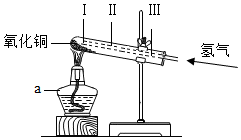
仪器a的名称是 。通入氢气的导管末端应位于试管 (选填“I”“Ⅱ”或“Ⅲ”)处。该制备铜的方法利用了氢气的 性。
(3)0.1mol氧化铜与足量氢气反应,计算参加反应氢气的质量。(根据化学方程式列式计算)。
(4)通过比较,写出方法一和方法二各自的一条优点 。
(1)方法一:氧化铜
稀硫酸 |
| 步骤Ⅰ |
铁粉 |
| 步骤Ⅱ |
I中反应的化学方程式是 ;Ⅱ中反应的基本类型是 。
该方法利用了铁的金属活动性比铜 (选填“强”或“弱”)。
(2)方法二:用铁粉与稀硫酸制得氢气进行如图实验。

仪器a的名称是 。通入氢气的导管末端应位于试管 (选填“I”“Ⅱ”或“Ⅲ”)处。该制备铜的方法利用了氢气的 性。
(3)0.1mol氧化铜与足量氢气反应,计算参加反应氢气的质量。(根据化学方程式列式计算)。
(4)通过比较,写出方法一和方法二各自的一条优点 。
查看全部题目