下载高清试卷
【2018年山东省济宁市中考化学试卷】-第1页
试卷格式:2018年山东省济宁市中考化学试卷.PDF
试卷热词:最新试卷、2018年、山东试卷、济宁市试卷、化学试卷、九年级试卷、中考试卷、初中试卷

扫码查看解析
试卷题目
1.下列有关物质的性质和用途,不存在对应关系的是( )
- A. 干冰升华 人工降雨
- B. 大理石硬度大 建筑材料
- C. 钢铁熔点高 金属导线
- D. 过氧化氢易分解 制取氧气
2.日常生活中的下列做法,一定含有化学变化的是( )
- A. 用胶带粘合破损书画
- B. 用白醋泡制软皮鸡蛋
- C. 用钢丝球擦除灶具污渍
- D. 用汽油清洗衣服油污
3.从分子、原子角度对下面一些现象和变化的解释,合理的是( )
- A. 花香四溢 分子很小,质量也很小
- B. 热胀冷缩 温度变化,分子或原子大小发生变化
- C. 滴水成冰 温度降低,分子间隔变小,停止运动
- D. 食品变质 分子发生变化,分子性质发生变化
4.下列物质的分类,不正确的一组是( )
- A. H2O、MgO、H2CO3 都属于氧化物
- B. H2S、H2SO3、H2SO4 都属于酸
- C. NaOH、Ca(OH)2、Fe(OH)2 都属于碱
- D. NaCl、Na2CO3、NaHCO3 都属于盐
5.下列化学方程式书写和对反应类型的判断,都正确的是( )
- A. 4Fe+3O22Fe2O3 化合反应
点燃 - B. Cu+2AgCl=2Ag+CuCl2 置换反应
- C. SiO2+3CSiC+2CO↑ 置换反应
高温 - D. BaCO3+2HCl=BaCl2+H2O+CO2↑ 复分解反应
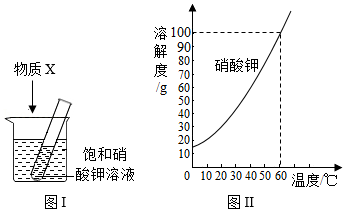
6.为探究物质溶解过程中的能量变化,某同学设计图Ⅰ所示装置。在盛有水的烧杯中放入一装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌。结合图Ⅱ硝酸钾溶解度曲线,对硝酸钾溶液变化的推断,合理的是( )
①X为NaCl固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
②X为NaOH固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
③X为NH4NO3晶体,试管中有晶体析出,硝酸钾溶液仍是饱和溶液
④X为浓H2SO4,试管中无晶体析出,硝酸钾溶液为不饱和溶液
①X为NaCl固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
②X为NaOH固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
③X为NH4NO3晶体,试管中有晶体析出,硝酸钾溶液仍是饱和溶液
④X为浓H2SO4,试管中无晶体析出,硝酸钾溶液为不饱和溶液

- A. ①②③
- B. ①③④
- C. ①②④
- D. ②③④
7.除去下列物质中混有的少量杂质所选用的操作方法,正确的是( )
| 选项 | 物质 | 操作方法 |
| A | CO2混有HCl气体 | 将气体通过足量NaOH溶液 |
| B | CuO混有碳粉 | 加入适量稀HCl,过滤,洗涤,干燥 |
| C | NaCl溶液混有CaCl2 | 加入过量Na2CO3溶液、过滤 |
| D | Cu(NO3)2溶液混有CuCl2 | 加入适量AgNO3溶液、过滤 |
- A. A
- B. B
- C. C
- D. D
8.分别向50g FeSO4和CuSO4溶液中,加入一定质量Mg粉恰好完全反应。随Mg粉消耗,Mg粉与溶液中FeSO4、CuSO4的质量变化见图。请读取图象信息并结合金属活动性顺序分析,下面说法不合理的是( )
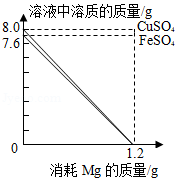

- A. 反应前,溶液中溶质质量分数:FeSO4<CuSO4
- B. 反应后,两溶液底部分别析出的金属是Fe和Cu
- C. 反应后,两溶液底部析出金属的质量:Fe<Cu
- D. 反应后,若FeSO4和CuSO4对应新溶液的溶质质量分数分别为A、B,则A>B
9.通过物质间相互反应可以实现物质间的相互转化。下列物质间的转化,通过一步化学反应不能实现的是( )
- A. C→CO→CO2
- B. Mg→MgO→MgCl2
- C. CuO→Cu(OH)2→CuCl2
- D. NaOH→NaCl→NaNO3
10.不使用其它试剂,利用物质间两两混合反应将物质区别开(提供的物质可重复使用),也是物质鉴别的常用方法。下面四组物质利用上述方法可鉴别开的是( )
- A. H2SO4、Na2SO4、BaCl2、FeCl3
- B. BaCl2、HCl、NaNO3、AgNO3
- C. Na2CO3、HNO3、NaNO3、BaCl2
- D. H2SO4、NaOH、MgCl2、Ba(NO3)2
11.高锰酸钾用途广泛,医药上可用作消毒剂、杀毒剂,实验室也经常使用高锰酸钾制取氧气。请按要求完成下面问题:
(1)高锰酸钾的化学式 ;
(2)高锰酸钾中锰元素的化合价 ;
(3)高锰酸钾中阳离子的符号 ;
(4)高锰酸钾中阴离子的符号 。
(1)高锰酸钾的化学式 ;
(2)高锰酸钾中锰元素的化合价 ;
(3)高锰酸钾中阳离子的符号 ;
(4)高锰酸钾中阴离子的符号 。
12.镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。请阅读信息后回答:
(1)金属镓 (填物理性质);
(2)镓原子结构示意图中X的数值 ;
(3)镓的氧化物的化学式 ;
(4)氮化镓(GaN)是第三代半导体材料,一般采用GaCl3与NH3在一定条件下反应制得,同时得到另一种化合物。该反应的化学方程式为 。

(1)金属镓 (填物理性质);
(2)镓原子结构示意图中X的数值 ;
(3)镓的氧化物的化学式 ;
(4)氮化镓(GaN)是第三代半导体材料,一般采用GaCl3与NH3在一定条件下反应制得,同时得到另一种化合物。该反应的化学方程式为 。
13.海水晒制粗盐的主要成分为NaCl,还含有少量的MgCl2、CaCl2、MgSO4、泥沙等杂质.下面是由粗盐获取较纯净精盐的一种方法:
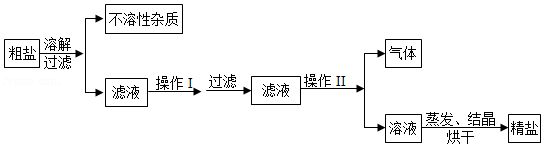
请分析上面流程图示,回答:
(1)为除去MgCl2、CaCl2、MgSO4可溶性杂质,操作I中依次加入的物质(过量)和顺序,合理的是 ;
A.NaOH、BaCl2、Na2CO3
B.Ba(NO3)2、Na2CO3、NaOH
C.Na2CO3、BaCl2、NaOH
D.BaCl2、NaOH、Na2CO3
(2)操作I过量加入各物质的目的是 ;
(3)为获取较纯净精盐,操作Ⅱ的具体方法是 .

请分析上面流程图示,回答:
(1)为除去MgCl2、CaCl2、MgSO4可溶性杂质,操作I中依次加入的物质(过量)和顺序,合理的是 ;
A.NaOH、BaCl2、Na2CO3
B.Ba(NO3)2、Na2CO3、NaOH
C.Na2CO3、BaCl2、NaOH
D.BaCl2、NaOH、Na2CO3
(2)操作I过量加入各物质的目的是 ;
(3)为获取较纯净精盐,操作Ⅱ的具体方法是 .
14.某工业园区甲、乙两化工厂排放的废水中含有K+、Cu2+、Fe3+、Cl﹣、OH﹣、
NO
六种离子,甲厂含有其中的三种,乙厂含有另外三种,两厂废水的直接排放对当地水质带来严重影响。某课外实践小组对两厂废水进行实地检测,发现甲厂废水呈碱性。
(1)甲厂废水中一定含有的离子是 ,可能含有的离子是 ;
(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是 (填离子符号),过滤后的废水中主要含有 两种物质 (填化学式),处理后的废水符合排放标准。
NO
| ﹣ |
| 3 |
(1)甲厂废水中一定含有的离子是 ,可能含有的离子是 ;
(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是 (填离子符号),过滤后的废水中主要含有 两种物质 (填化学式),处理后的废水符合排放标准。
15.洗洁精是家庭必备的清洁用品,可迅速分解油腻、去污、除菌,有味道淡雅、洁净温和、泡沫柔细、低残留的优点。洗洁精的有效成分是表面活性剂,还含有泡沫剂、香精、水、色素等多种成分。请回答:

(1)洗洁精去除油污的有效成分是 ;
(2)洗洁精去除油污的原理是 。

(1)洗洁精去除油污的有效成分是 ;
(2)洗洁精去除油污的原理是 。
16.(1)某研究性学习小组为验证“氨气还原氧化铜”的实验,认真阅资料并做出以下准备。
资料准备:
I.氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,溶液呈碱性。
Ⅱ.氨气还原氧化铜的化学反应原理:2NH3+3CuO
3Cu+N2+3H2O。
实验准备:

请回答:
①为达成“氨气还原氧化铜”的实验目的,装置A、B、D、E的正确连接顺序 ;(填序号)
②装置A中发生反应的化学方程式 ;
③装置B观察到的现象 ,装置E的作用 ;
④将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变蓝色,原因是 。
(2)小凡同学利用氯化钡和氢氧化钠两种试剂,从硫酸钠、硫酸镁和氯化镁三瓶未贴标签的无色溶液中鉴别出硫酸镁溶液,设计并进行以下实验。请你补齐实验内容;
资料准备:
I.氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,溶液呈碱性。
Ⅱ.氨气还原氧化铜的化学反应原理:2NH3+3CuO
| △ |
实验准备:

请回答:
①为达成“氨气还原氧化铜”的实验目的,装置A、B、D、E的正确连接顺序 ;(填序号)
②装置A中发生反应的化学方程式 ;
③装置B观察到的现象 ,装置E的作用 ;
④将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变蓝色,原因是 。
(2)小凡同学利用氯化钡和氢氧化钠两种试剂,从硫酸钠、硫酸镁和氯化镁三瓶未贴标签的无色溶液中鉴别出硫酸镁溶液,设计并进行以下实验。请你补齐实验内容;
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取三支洁净试管,分别倒入三种无色溶液,然后滴加 ,振荡,观察现象; | ||
| (2) |
17.维生素C(化学式:C6H8O6)对人体皮肤和牙龈健康有重要作用,缺乏维生素C,会引起坏血病,中学生每天需要补充60mg维生素C.请阅读信息后回答:
(1)维生素C中碳、氢、氧三种元素质量比是 ;
(2)维生素C分子的相对分子质量是 。

(1)维生素C中碳、氢、氧三种元素质量比是 ;
(2)维生素C分子的相对分子质量是 。

18.长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。某研究性学习小组为测定水垢中碳酸钙的质量分数,利用图Ⅰ装置将足量的盐酸加入到10.0g水垢中。随反应进行,装置C质量的变化如图Ⅱ所示。请回答:

(1)向图I装置A中不断通入氮气的目的是 ;
(2)若不考虑盐酸的挥发和水垢中含有其他成分,请根据图Ⅱ数据计算:
水垢中碳酸钙的质量是 ,水垢中氢氧化镁的质量分数是 ; (不要求计算过程,精确到0.1)
(3)若考虑盐酸的挥发,会造成水垢中碳酸钙质量分数的测量结果 (填"增大""减小"或"不变")。

(1)向图I装置A中不断通入氮气的目的是 ;
(2)若不考虑盐酸的挥发和水垢中含有其他成分,请根据图Ⅱ数据计算:
水垢中碳酸钙的质量是 ,水垢中氢氧化镁的质量分数是 ; (不要求计算过程,精确到0.1)
(3)若考虑盐酸的挥发,会造成水垢中碳酸钙质量分数的测量结果 (填"增大""减小"或"不变")。
查看全部题目