下载高清试卷
【2020年浙江省宁波市中考化学试卷】-第1页
试卷格式:2020年浙江省宁波市中考化学试卷.PDF
试卷热词:最新试卷、2020年、浙江试卷、宁波市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1."关爱生命,健康生活".下列行为不利于健康的是( )
- A. 保持乐观的生活态度
- B. 拒绝吸烟、酗酒、吸毒
- C. 参加体育锻炼
- D. 沉湎网络游戏
2.下列实验操作需要纠正的是( )
- A.
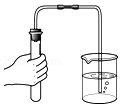 检查气密性
检查气密性 - B.
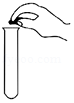 向试管中加固体
向试管中加固体 - C.
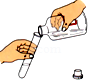 倾倒液体
倾倒液体 - D.
 收集氧气
收集氧气
3.某化学反应的反应物和生成物的微观示意图及反应前后的质量如下表所示。
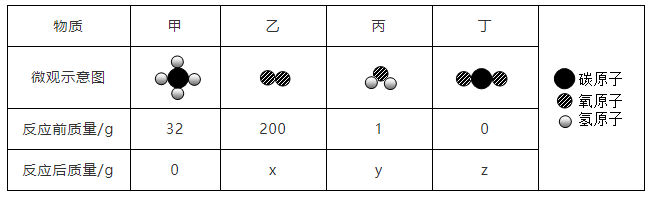
下列有关该反应的说法正确的是( )

下列有关该反应的说法正确的是( )
- A. 甲物质由碳原子和氢原子直接构成
- B. 该反应属于置换反应
- C. 参加反应的反应物分子个数比为1:1
- D. x+y+z=233
4.如图是一款变色眼镜,它的镜片内含有溴化银和氧化铜。在强光照射下,溴化银分解成单质溴和银,镜片颜色变深;当光线变暗时,溴和银在氧化铜催化作用下,又立即化合成溴化银,镜片颜色变浅。有关该眼镜的说法错误的是( )


- A. 塑料是高分子合成材料
- B. 铜螺丝久置在潮湿的空气中会产生铜锈
- C. 溴化银分解后,银元素的化合价升高
- D. 溴和银化合成溴化银前后,氧化铜化学性质不变
5.如图为一种自热火锅的构件图。该自热火锅的发热包内有铁粉、铝粉、炭粉、生石灰等物质,将发热包放到水中,会放出大量的热。有关该自热火锅的说法不合理的是( )
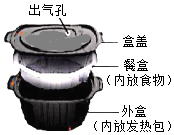

- A. 生石灰与水反应,会放出大量的热
- B. 设计出气孔的目的是为了避免使用时盒内气压过高
- C. 遇水能放出热量的物质都能作为发热包的内容物
- D. 使用过的发热包即使干燥后也不能重复使用
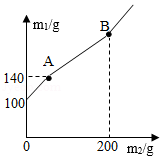
6.某锥形瓶内盛有盐酸和氯化铜的混合溶液100g,向其中加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量m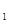 与加入的氢氧化钠溶液质量m
与加入的氢氧化钠溶液质量m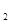 的变化关系如图所示。下列说法错误的是( )
的变化关系如图所示。下列说法错误的是( )
 与加入的氢氧化钠溶液质量m
与加入的氢氧化钠溶液质量m 的变化关系如图所示。下列说法错误的是( )
的变化关系如图所示。下列说法错误的是( )
- A. 反应至A点时,所加NaOH溶液的质量为40g
- B. 反应至A点时,溶液中的溶质有CuCl2和NaCl
- C. 反应至B点时,锥形瓶内溶液的质量为280.4g
- D. 反应至B点时,锥形瓶内溶液中NaCl的质量为23.4g
7.如图是某科学老师设计的一氧化碳还原氧化铁的实验装置。

(1)在B装置的液面下降到安全线之前,不能加热氧化铁,这是因为 。
(2)反应结束后停止加热,继续通CO,此时B装置的作用是 。

(1)在B装置的液面下降到安全线之前,不能加热氧化铁,这是因为 。
(2)反应结束后停止加热,继续通CO,此时B装置的作用是 。
8.铁的化合物有广泛用途,如碳酸亚铁(FeCO3)可作补血剂。某硫酸厂产生的炉渣中除了有Fe2O3、FeO,还有一定量的SiO2。兴趣小组利用炉渣尝试制备FeCO3,其流程如图:
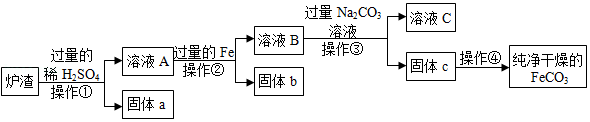
【已知:Fe+Fe2(SO4)3═3FeSO4;SiO2不溶于水,也不与稀硫酸反应】
(1)操作①的名称是 。
(2)溶液A中的溶质除H2SO4外,还存在 。
(3)上述流程中生成固体c的化学方程式 。

【已知:Fe+Fe2(SO4)3═3FeSO4;SiO2不溶于水,也不与稀硫酸反应】
(1)操作①的名称是 。
(2)溶液A中的溶质除H2SO4外,还存在 。
(3)上述流程中生成固体c的化学方程式 。
9.在"探究稀盐酸和稀硫酸的化学性质"实验中,小科发现镁带与稀盐酸反应后的试管内出现了灰白色沉淀。
【提出问题】灰白色沉淀是什么物质?
【提出猜想】小科在老师指导下,猜想灰白色沉淀是下列物质中的一种或几种:
①镁;②氯化镁;③氢氧化镁;④碱式氯化镁[Mg(OH)Cl]。
老师肯定了小科的猜想,并鼓励他继续进行实验探究。
【实验探究】步骤一:将上述镁带与稀盐酸反应后试管内的物质过滤,得到滤液和灰白色滤渣。
步骤二:取滤液于试管中,加入适量的氯化镁粉末,粉末全部溶解。
步骤三:取少量灰白色滤渣于试管中,加入适量稀盐酸,沉淀全部溶解,无其他现象。
步骤四:将剩余滤渣用蒸馏水充分洗涤。取洗涤后的滤渣于试管中,加入过量稀硝酸,滤渣全部溶解,再加入硝酸银溶液,有白色沉淀产生。
【实验反思及结论】
(1)从步骤二可知,灰白色沉淀不可能是氯化镁,因为滤液是氯化镁的 (填"饱和"或"不饱和")溶液。
(2)从步骤三可知,该沉淀中没有 。
(3)步骤四中将滤渣用蒸馏水充分洗涤是为了 。
(4)根据实验探究可知,该反应产生的灰白色沉淀中一定含有 。
【提出问题】灰白色沉淀是什么物质?
【提出猜想】小科在老师指导下,猜想灰白色沉淀是下列物质中的一种或几种:
①镁;②氯化镁;③氢氧化镁;④碱式氯化镁[Mg(OH)Cl]。
老师肯定了小科的猜想,并鼓励他继续进行实验探究。
【实验探究】步骤一:将上述镁带与稀盐酸反应后试管内的物质过滤,得到滤液和灰白色滤渣。
步骤二:取滤液于试管中,加入适量的氯化镁粉末,粉末全部溶解。
步骤三:取少量灰白色滤渣于试管中,加入适量稀盐酸,沉淀全部溶解,无其他现象。
步骤四:将剩余滤渣用蒸馏水充分洗涤。取洗涤后的滤渣于试管中,加入过量稀硝酸,滤渣全部溶解,再加入硝酸银溶液,有白色沉淀产生。
【实验反思及结论】
(1)从步骤二可知,灰白色沉淀不可能是氯化镁,因为滤液是氯化镁的 (填"饱和"或"不饱和")溶液。
(2)从步骤三可知,该沉淀中没有 。
(3)步骤四中将滤渣用蒸馏水充分洗涤是为了 。
(4)根据实验探究可知,该反应产生的灰白色沉淀中一定含有 。
10.覆盆子果实含有丰富的维生素、少量水杨酸以及钙、钾等元素,有"黄金水果"的美誉。其中的水杨酸常温下稳定,加热易分解,微溶于水,其水溶液呈酸性。

(1)覆盆子果实中的钙、钾等元素是以 (填"单质"或"化合物")的形态存在。
(2)水杨酸(C7H6O3)中碳元素和氧元素的质量比为 。
(3)水杨酸的上述性质中,属于物理性质的是: 。

(1)覆盆子果实中的钙、钾等元素是以 (填"单质"或"化合物")的形态存在。
(2)水杨酸(C7H6O3)中碳元素和氧元素的质量比为 。
(3)水杨酸的上述性质中,属于物理性质的是: 。
11.某科学兴趣小组同学取8.5g铁,放到含少量硫酸的硫酸铜溶液中,完全反应后,最终得到9.2g固体。为测定所得固体中各成分的含量,同学们将62.5g稀盐酸分五次加入到该固体中,得到数据如表:
请分析计算:
(1)表中a的值是 。
(2)9.2g固体中铁的质量是 。
(3)稀盐酸的溶质质量分数是多少?
(4)与硫酸铜反应的铁的质量是多少?
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入盐酸溶液质量/g | 12.5 | 12.5 | 12.5 | 12.5 | 12.5 |
| 剩余固体质量/g | 8.5 | 7.8 | a | 6.4 | 6.4 |
请分析计算:
(1)表中a的值是 。
(2)9.2g固体中铁的质量是 。
(3)稀盐酸的溶质质量分数是多少?
(4)与硫酸铜反应的铁的质量是多少?
查看全部题目