下载高清试卷
【2020年四川省泸州市中考化学试卷】-第1页
试卷格式:2020年四川省泸州市中考化学试卷.PDF
试卷热词:最新试卷、2020年、四川试卷、泸州市试卷、化学试卷、九年级试卷、中考试卷、初中试卷

扫码查看解析
试卷题目
1.下列变化属于化学变化的是( )
- A. 酒精挥发
- B. 冰糕融化
- C. 蔗糖溶解
- D. 钢铁生锈
2.空气是生命赖以存在的物质基础。下列属于空气的主要成分且能供给人体呼吸的是( )
- A. 氮气
- B. 氧气
- C. 乙炔
- D. 氩气
3.下面有关"舌尖上的泸州"的说法错误的是( )
- A.
 "泸州老窖"含有乙醇
"泸州老窖"含有乙醇 - B.
 "合江荔枝"含有维生素
"合江荔枝"含有维生素 - C.
 "泸州桂圆"含有大量塑料
"泸州桂圆"含有大量塑料 - D.
 "古蔺麻辣鸡"富含蛋白质
"古蔺麻辣鸡"富含蛋白质
4.下列物质不能与NaOH溶液反应的是( )
- A. 二氧化碳
- B. 硝酸
- C. 硫酸铜
- D. 氢氧化铁
5.下列关于化肥NH4H2PO4(磷酸二氢铵)的说法错误的是( )
- A. P元素的化合价是+3价
- B. N元素的化合价是﹣3价
- C. NH4H2PO4属于复合肥料
- D. NH4H2PO4不能与草木灰混合使用
6.2019年总理的政府工作报告明确要求"加强城市垃圾分类处置",于是各大城市分别出台垃圾分类处理办法,"垃圾分类"成为热词。下列有关说法错误的是( )
- A. 垃圾分类利用,能减少垃圾的危害
- B. 家庭废弃餐厨物品,属于无污染垃圾
- C. 废弃金属与废纸,属于可回收垃圾
- D. 废弃电池含有重金属,属于有害垃圾
7.下列实验或操作正确的是( )
- A. 将铁丝伸入硫酸铜溶液中证明铁比铜活泼
- B. 将水加入浓硫酸来配制稀硫酸
- C. 用湿润的pH试纸来精确测定溶液的pH
- D. 用玻璃棒搅拌过滤器中的溶液以加快过滤
8.下列溶液中的反应,其反应方程式与对应括号内的现象都正确的是( )
- A. H2SO4+NaHCO3═NaSO4+H2O+CO2↑(冒气泡)
- B. Mg(OH)3+3HCl═MgCl3+3H2O(白色沉淀逐渐溶解)
- C. 2NH4NO3+Ca(OH)2Ca(NO3)2+2H2O+2NH3↑(产生刺激味气体)
△ - D. Fe2O3+3H2SO4═Fe2(SO4)3+3H2O(固体逐渐溶解,溶液变蓝)
9.中国北斗、导航未来!2020年6月23日9时43分,北斗系统中第55颗卫星搭乘长征三号乙运载火箭,从西昌卫星发射中心成功升空,宣告北斗系统的正式完善。回答下列问题:
(1)卫星利用太阳能电池板进行能量转化,其能量转化方式是将太阳能转化为 能。
(2)运载火箭的第一、第二级燃料可用偏二甲肼(C2H8N2)和四氧化二氮的"二元推进剂",偏二甲肼属于 (选填"有机"或"无机")物,分子中碳、氢元素的质量比为 。
(3)氧化铝陶瓷可用于火箭腹部的隔热瓦,可知氧化铝的熔点 。
(1)卫星利用太阳能电池板进行能量转化,其能量转化方式是将太阳能转化为 能。
(2)运载火箭的第一、第二级燃料可用偏二甲肼(C2H8N2)和四氧化二氮的"二元推进剂",偏二甲肼属于 (选填"有机"或"无机")物,分子中碳、氢元素的质量比为 。
(3)氧化铝陶瓷可用于火箭腹部的隔热瓦,可知氧化铝的熔点 。
10.材料是人类社会物质文明进步的重要标志之一。回答下列问题:
(1)商代后母戊鼎代表着我国古代高超的金属制造水平,它主要是含 元素的合金。

(2)从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的一个反应的微观示意图如图:

①写出该图示表示的化学方程式 ,其基本反应类型是 。
②从如图图示看出:微观上,化学反应前后分子改变了,而 没有改变。
(1)商代后母戊鼎代表着我国古代高超的金属制造水平,它主要是含 元素的合金。

(2)从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的一个反应的微观示意图如图:

①写出该图示表示的化学方程式 ,其基本反应类型是 。
②从如图图示看出:微观上,化学反应前后分子改变了,而 没有改变。
11.中药灵芝有一定的防癌抗癌作用,现代科学研究表明是因为其中含硒等人体需要的微量元素,如图是元素周期表中硒元素的相关信息。回答下列问题:
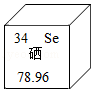
(1)硒属于 元素(填"金属"或"非金属"),它的化合价与同族的硫相似,则硒化氢的化学式是 。
(2)人体长期缺微量元素硒将不利于身体健康,那么摄入过多又是否有利于身体健康呢? (填"是"或"否")

(1)硒属于 元素(填"金属"或"非金属"),它的化合价与同族的硫相似,则硒化氢的化学式是 。
(2)人体长期缺微量元素硒将不利于身体健康,那么摄入过多又是否有利于身体健康呢? (填"是"或"否")
12.NaHCO3在生产和生活中有许多重要用途,某学习小组对其性质进行了如下探究。物质的溶解度见下表。回答下列问题:
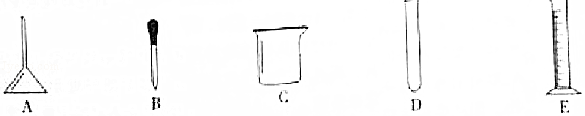
(1)在20℃时称取4g NaHCO3加入46mL蒸馏水(密度取值为1g/mL),充分搅拌制得澄清溶液。该实验可以达到探究NaHCO3 性的目的;实验中不需要的仪器是 (选填字母编号)。
(2)用pH计测得溶液的pH为8.2,说明溶液呈 性。
(3)所配NaHCO3溶液的质量分数等于 ,降温到10℃时溶液 (填"是"或"不是")饱和溶液。
(4)取2mL所配NaHCO3溶液于试管中,滴加5%的CaCl2溶液,观察到气泡和白色沉淀,实验证明该气体是CO2。据此小组同学讨论认为:白色沉淀不可能是Ca(OH)2,其理由是 ,于是得出结论:白色沉淀是 。
| 温度 | 10℃ | 20℃ |
| NaHCO3的溶解度(g/100g水) | 8.1 | 9.6 |
| Ca(HCO3)2的溶解度(g/100g水) | 16.6 |
(1)在20℃时称取4g NaHCO3加入46mL蒸馏水(密度取值为1g/mL),充分搅拌制得澄清溶液。该实验可以达到探究NaHCO3 性的目的;实验中不需要的仪器是 (选填字母编号)。

(2)用pH计测得溶液的pH为8.2,说明溶液呈 性。
(3)所配NaHCO3溶液的质量分数等于 ,降温到10℃时溶液 (填"是"或"不是")饱和溶液。
(4)取2mL所配NaHCO3溶液于试管中,滴加5%的CaCl2溶液,观察到气泡和白色沉淀,实验证明该气体是CO2。据此小组同学讨论认为:白色沉淀不可能是Ca(OH)2,其理由是 ,于是得出结论:白色沉淀是 。
13.过氧化氢能极缓慢分解,可看成分解为水和氧原子:H2O2→H2O+O,其水溶液显弱酸性。过氧化氢是实验室中重要化学试剂,在生产生活中有重要用途。回答下列问题:
(1)过氧化氢中氧元素的化合价为 。
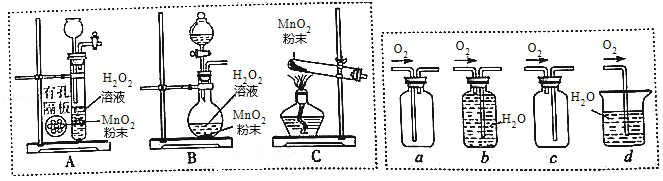
(2)MnO2能加快过氧化氢分解,氧原子再结合成氧分子而制得氧气,MnO2在反应中作 剂,下列装置可用于制取氧气的是 (选填字母编号,下同),可用于收集氧气的装置有 。
(3)氧原子容易与许多有机物反应而破坏其结构,所以过氧化氢溶液能杀死新冠病毒,这个过程叫做蛋白质的 。
(4)向氢氧化钠溶液中滴加酚酞试液,再滴加过氧化氢溶液,观察到溶液先变红后褪色,猜想其褪色原因可能有两种:
①H2O2显酸性消耗了NaOH,而使红色褪去;
②H2O2分解产生的氧原子与酚酞反应破坏其结构,而使红色褪去。究竟哪种猜想合理?请用本次实验用过的试剂设计实验 (补充完实验方案)。有兴趣的同学可在后续学习中通过实验得出结论。
(1)过氧化氢中氧元素的化合价为 。
(2)MnO2能加快过氧化氢分解,氧原子再结合成氧分子而制得氧气,MnO2在反应中作 剂,下列装置可用于制取氧气的是 (选填字母编号,下同),可用于收集氧气的装置有 。

(3)氧原子容易与许多有机物反应而破坏其结构,所以过氧化氢溶液能杀死新冠病毒,这个过程叫做蛋白质的 。
(4)向氢氧化钠溶液中滴加酚酞试液,再滴加过氧化氢溶液,观察到溶液先变红后褪色,猜想其褪色原因可能有两种:
①H2O2显酸性消耗了NaOH,而使红色褪去;
②H2O2分解产生的氧原子与酚酞反应破坏其结构,而使红色褪去。究竟哪种猜想合理?请用本次实验用过的试剂设计实验 (补充完实验方案)。有兴趣的同学可在后续学习中通过实验得出结论。
14.新能源页岩气,正在冲击传统能源体系。据报道,我国页岩气储量排名世界第一,合理开采将有利于改善我国的能源结构,川南页岩气田分布在泸州等地。页岩气是藏身于地下3000多米的页岩层裂缝中的天然气,在此高压环境中,还有部分溶解于裂缝中存在的少量石油里。目前,开采页岩气时从地表钻井到页岩层,向地下压入大量水和沙,使页岩气所在的地层产生缝隙,因压强降低,页岩气将从其藏匿处逸出。这些水和沙将被抽回地面,形成返排液。回答下列问题:
(1)页岩气中主要成分的化学式是 ,溶解在石油中的页岩气逸出的原因是 。
(2)页岩气中还可能含有乙烷(C2H6),写出乙烷完全燃烧的化学方程式 。
(3)返排液是油、水溶液和沙组成的混合物。从返排液中分离出沙的实验操作名称是 ;下表是某返排液中水溶液的主要成分及其含量,质量分数最高的金属离子是 ,这些离子的含量远高于自然水。
(4)结合上文分析简答:开采时可能产生的主要环保问题是 (写一点),你的解决建议是 。
(1)页岩气中主要成分的化学式是 ,溶解在石油中的页岩气逸出的原因是 。
(2)页岩气中还可能含有乙烷(C2H6),写出乙烷完全燃烧的化学方程式 。
(3)返排液是油、水溶液和沙组成的混合物。从返排液中分离出沙的实验操作名称是 ;下表是某返排液中水溶液的主要成分及其含量,质量分数最高的金属离子是 ,这些离子的含量远高于自然水。
| 离子 | K+ | Ca2+ | Mg2+ | HCO
| Cl﹣ | ||
| 含量(mg/L) | 310 | 491 | 129 | 470 | 26.1 |
(4)结合上文分析简答:开采时可能产生的主要环保问题是 (写一点),你的解决建议是 。
15.菱镁矿中主要含MgCO3、FeCO3和SiO2。以菱镁矿为原料制取镁的工艺流程如图。

回答下列问题:
(1)菱镁矿属于 (选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是 。
(3)写出菱镁矿中MgCO3与稀HCl反应的化学方程式 。
(4)溶液b→溶液c反应的化学方程式为:4FeCl2+ +4HCl=4FeCl3+2H2O(补充完方程式)
(5)溶液c调pH使Fe3+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8﹣ 。
已知:物质沉淀的pH见下表:
(6)结合流程中的数据计算。
①菱镁矿中镁元素的质量分数为________(不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量(写出计算过程)。

回答下列问题:
(1)菱镁矿属于 (选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是 。
(3)写出菱镁矿中MgCO3与稀HCl反应的化学方程式 。
(4)溶液b→溶液c反应的化学方程式为:4FeCl2+ +4HCl=4FeCl3+2H2O(补充完方程式)
(5)溶液c调pH使Fe3+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8﹣ 。
已知:物质沉淀的pH见下表:
| 物质 | Mg(OH)2 | Fe(OH)3 |
| 开始沉淀的pH | 8.9 | 1.5 |
| 完全沉淀的pH | 10.9 | 2.8 |
(6)结合流程中的数据计算。
①菱镁矿中镁元素的质量分数为________(不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量(写出计算过程)。
查看全部题目