下载高清试卷
【2020年湖南省株洲市中考化学试卷】-第1页
试卷格式:2020年湖南省株洲市中考化学试卷.PDF
试卷热词:最新试卷、2020年、湖南试卷、株洲市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.下列过程中一定发生了化学变化的是( )
- A. 花香四溢
- B. 高粱酿酒
- C. 积雪融化
- D. 矿石粉碎
2.存放药品时,某化学实验员不小心将药品标签撕去了一部分(如图),根据所学知识,你判断该药品一定不是( )


- A. 碱
- B. 盐
- C. 氧化物
- D. 酸
3.下列有关化学实验操作的图示中正确的是( )
- A.
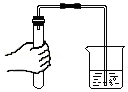 检查装置的气密性
检查装置的气密性 - B.
 熄灭酒精灯
熄灭酒精灯 - C.
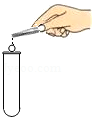 加入块状固体
加入块状固体 - D.
 闻气体气味
闻气体气味
4.人体中含量最高的金属元素是( )
- A. O
- B. Fe
- C. Ca
- D. Na
5.下列不属于中华民族取得的重大化学成就的是( )
- A. 侯德榜发明的联合制碱法
- B. 张青莲精准测量铟的相对原子质量
- C. 道尔顿提出的“原子论”学说
- D. 屠呦呦乙醚冷萃提高了青蒿素的提取率
6.习总书记提出“绿水青山就是金山银山”,强调了保护环境的重要性。下列措施或行为合理的是( )
- A. 使用风能、太阳能等绿色能源
- B. 废旧电池作深埋处理
- C. 废弃塑料制品直接露天焚烧
- D. 工业废水直接灌溉农田
7.下列物质由分子构成的是( )
- A. 铜
- B. 氧气
- C. 氯化钠
- D. 氢氧化钙
8.下列微观示意图中,黑球代表H原子,白球代表Cl原子,其中代表混合物的是( )
- A.

- B.
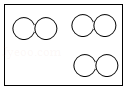
- C.

- D.

9.下列反应属于置换反应的是( )
- A. Fe2O3+3CO2Fe+3CO2
高温 - B. CH4+2O2CO2+2H2O
点燃 - C. 2Na+2H2O═2NaOH+H2↑
- D. Na2CO3+CaCl2═CaCO3↓+2NaCl
10.常温下,一些饮料或食物的近似pH如下:
下列说法中正确的是( )
| 食物 | 柠檬汁 | 橙子汁 | 西瓜汁 | 鸡蛋清 |
| pH | 2.2~2.4 | 3.6~4.3 | 5.3~6.1 | 7.6~8.0 |
下列说法中正确的是( )
- A. 胃酸过多的人应多喝柠檬汁
- B. 西瓜汁和鸡蛋清显碱性
- C. 西瓜汁比柠檬汁酸性强
- D. 柠檬汁和橙子汁显酸性
11.下列说法中不正确的是( )
- A. 铝与氧气反应表面生成致密的氧化膜,从而阻止铝进一步氧化,因此铝制品不易腐蚀
- B. 熔喷布是口罩的核心材料,以聚丙烯为主要原料,其中聚丙烯属于有机高分子材料
- C. 由玻璃纤维和有机高分子材料复合而成的玻璃钢,因其质脆而不能作车船体材料
- D. 波尔多液是一种农业上常用的杀菌剂,是由硫酸铜、生石灰加水配制而成
12.2020年6月23号我国北斗导航组网最后一颗卫星成功发射,开启北斗导航的全新时代。北斗导航卫星系统采用铷原子钟,提供精确时间,如图是铷元素在元素周期表中的相关信息。下列说法中正确的是( )


- A. 铷的元素符号为Rb
- B. 铷的中子数为37
- C. 铷属于非金属元素
- D. 铷的相对原子质量为85.47g
13.下列物质间不能发生反应的是( )
- A. 稀盐酸和镁条
- B. 稀盐酸和铜丝
- C. 稀盐酸和氢氧化镁
- D. 稀盐酸和氢氧化铜
14.化学与生产、生活息息相关,下列说法中不正确的是( )
- A. 洗涤剂使油污乳化,可去除餐具油污
- B. 利用干冰“升华”提升舞台效果
- C. 合理使用无磷洗衣粉,可减少水体污染
- D. 利用明矾对自来水进行杀菌消毒
15.下列说法中正确的是( )
- A. 氟元素(F)是人体必需的微量元素,缺氟会引起贫血
- B. 缺碘会引起甲状腺肿大,所以日常生活中要适量补碘
- C. 维生素可以起到维持身体健康的重要作用,缺乏维生素D会引起夜盲症
- D. 米饭在人体内经酶的催化作用,与水发生一系列反应,最终转化为氨基酸
16.“绿色化学”的理念是“原子利用率为100%”,即原料全部转化为产品。下列反应符合此理念的是( )
- A. 硫与氧气反应:S+O2SO2
点燃 - B. 实验室制氢气:Zn+H2SO4═ZnSO4+H2↑
- C. 氢气还原氧化铜:H2+CuOCu+H2O
△ - D. 煅烧石灰石:CaCO3CaO+CO2↑
高温
17.下列各组固体物质,不能用水鉴别的是( )
- A. KNO3、KCl
- B. CaCO3、CaCl2
- C. CuSO4、Na2SO4
- D. NH4NO3、CaO
18.推理是学习化学时常用的思维方式。以下推理结果正确的是( )
- A. 碱能使无色酚酞试液变红色,能使无色酚酞试液变红色的一定是碱
- B. 中和反应一定有盐和水生成,有盐和水生成的反应一定是中和反应
- C. 化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物
- D. 离子是带电的粒子,所以带电的粒子一定是离子
19.下列实验操作能达到实验目的的是( )
| 实验操作 | 实验目的 | |
| A | 将带火星的木条伸入混合气体中 | 检验二氧化碳中混有的少量氧气 |
| B | 用pH试纸测定肥皂水的酸碱性 | 验证肥皂水呈碱性 |
| C | 加入足量的稀盐酸,蒸发结晶 | 除去碳酸钠固体中混有的氯化钠 |
| D | 分别在放有铜和银的试管中加入稀盐酸 | 比较铜和银的金属活动性强弱 |
- A. A
- B. B
- C. C
- D. D
20.在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
| 物质 | P | Q | R | W |
| 反应前的质量(g) | 5 | 2 | 14 | 18 |
| 反应后的质量(g) | 20 | x | 4 | 13 |
- A. 参加化学反应的P和W的质量比为3:2
- B. 该反应用化学方程式表示为:3P+Q=2R+W
- C. 反应后容器中R与Q的质量比为1:2
- D. Q在反应中可能作催化剂
21.请用化学用语填空:
(1)2个铵根离子: 。
(2)鸡蛋壳的主要成分: 。
(3)“熬胆矾铁釜,久之亦化为铜”,写出此过程涉及的化学方程式 。
(1)2个铵根离子: 。
(2)鸡蛋壳的主要成分: 。
(3)“熬胆矾铁釜,久之亦化为铜”,写出此过程涉及的化学方程式 。
22.青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具。如图是一种照明用台灯。

(1)灯管后面的反光片为铝箔,铝块能形成铝箔是利用铝的 性。
(2)通过观察图片,发现还使用了其他材料,请指出其中的一种材料及它所体现的性质 、 。

(1)灯管后面的反光片为铝箔,铝块能形成铝箔是利用铝的 性。
(2)通过观察图片,发现还使用了其他材料,请指出其中的一种材料及它所体现的性质 、 。
23.如图中A、B、C、D为四种元素原子的结构示意图。请回答下列问题:

(1)A、C两种原子相互结合形成的化合物的化学式为 (任写一种)。
(2)D中x= 。
(3)写出B、C两种原子形成的化合物BC2的名称 。

(1)A、C两种原子相互结合形成的化合物的化学式为 (任写一种)。
(2)D中x= 。
(3)写出B、C两种原子形成的化合物BC2的名称 。
24.如图为甲、乙两种物质(均不含结晶水)的溶解度曲线。据此回答下列问题:

(1)当温度为 ℃时,甲、乙两种物质的溶解度相等。
(2)图中C点对应的乙溶液是 (填“饱和”或“不饱和”)溶液。
(3)当温度为a2℃时,在100g水中加入60g甲,溶液中溶质的质量分数为 (结果保留三位有效数字)。

(1)当温度为 ℃时,甲、乙两种物质的溶解度相等。
(2)图中C点对应的乙溶液是 (填“饱和”或“不饱和”)溶液。
(3)当温度为a2℃时,在100g水中加入60g甲,溶液中溶质的质量分数为 (结果保留三位有效数字)。
25.2019年诺贝尔化学奖授予约翰•古迪纳夫(John B.Goodenough,以下简称约翰)、斯坦利•威廷汉(M.StanleyWhittingham)和吉野彰(AkiraYoshino,以下简称吉野)三人,以表彰他们在锂离子电池领域的贡献。
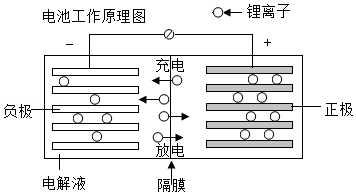
(1)吉野用钴酸锂(LiCoO2)作电池正极,负极使用了石油工业副产品﹣﹣石油焦,制造了首款商业锂离子电池。锂在化合物中常显+1价,则LiCoO2中Co的化合价为 。
(2)约翰用磷酸铁取代钴酸锂,使电池更环保。磷酸铁的化学式为 。

(1)吉野用钴酸锂(LiCoO2)作电池正极,负极使用了石油工业副产品﹣﹣石油焦,制造了首款商业锂离子电池。锂在化合物中常显+1价,则LiCoO2中Co的化合价为 。
(2)约翰用磷酸铁取代钴酸锂,使电池更环保。磷酸铁的化学式为 。
26.如图为一氧化碳还原氧化铁示意图。
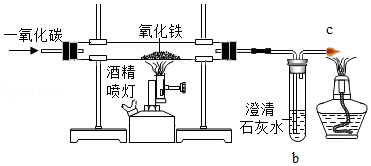
(1)写出试管b中涉及的主要反应的化学方程式 。
(2)c处操作的目的为 。

(1)写出试管b中涉及的主要反应的化学方程式 。
(2)c处操作的目的为 。
27.读取图片信息后回答:

(1)此消毒液的有效成分是什么? 。有效成分的含量为多少? 。
(2)结合化学常识,谈谈你对标签中“密闭,避光保存”和“易燃,应远离火源”的理解 。

(1)此消毒液的有效成分是什么? 。有效成分的含量为多少? 。
(2)结合化学常识,谈谈你对标签中“密闭,避光保存”和“易燃,应远离火源”的理解 。
28.覆铜板是制作印刷线路板的基本材料。覆铜板中的金属Sn占2﹣10%,Cu占90﹣98%.简易工艺流程如图:

(1)将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是 的性质(填字母代号)。
a.溶解性不同 b.密度不同 c.沸点不同
(2)步骤④中涉及的分离操作是 (填操作名称)。
(3)通过步骤⑤和⑥所得洗涤液的pH 7(填“>”、“<”、“=”)。
(4)设计步骤⑦的主要目的是 。
(5)步骤⑨中涉及的主要化学方程式为 。

(1)将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是 的性质(填字母代号)。
a.溶解性不同 b.密度不同 c.沸点不同
(2)步骤④中涉及的分离操作是 (填操作名称)。
(3)通过步骤⑤和⑥所得洗涤液的pH 7(填“>”、“<”、“=”)。
(4)设计步骤⑦的主要目的是 。
(5)步骤⑨中涉及的主要化学方程式为 。
29.在实验室中,我们常用如图所示装置制取和收集某些气体。

(1)写出a、b两种仪器的名称。a ,b为 。
(2)实验室若用KMnO4制取O2,写出其化学方程式 ,相应的发生装置为 (填字母代号)。
(3)若选用装置C制备CO2,则可以选择 (填字母代号)。
a.块状碳酸钙和稀盐酸 b.块状碳酸钙和稀硫酸
(4)经查阅资料,Na2O2(过氧化钠)也能与水迅速反应产生O2.补全下列反应方程式:2Na2O2+2H2O═ +O2↑
(5)收集O2适合选用 装置(填字母代号)。
a.仅D b.仅E c.D和E

(1)写出a、b两种仪器的名称。a ,b为 。
(2)实验室若用KMnO4制取O2,写出其化学方程式 ,相应的发生装置为 (填字母代号)。
(3)若选用装置C制备CO2,则可以选择 (填字母代号)。
a.块状碳酸钙和稀盐酸 b.块状碳酸钙和稀硫酸
(4)经查阅资料,Na2O2(过氧化钠)也能与水迅速反应产生O2.补全下列反应方程式:2Na2O2+2H2O═ +O2↑
(5)收集O2适合选用 装置(填字母代号)。
a.仅D b.仅E c.D和E
30.某化学兴趣小组做粗盐提纯实验,并对粗盐的成分作进一步探究。请回答下列问题:
实验一:粗盐提纯
(1)提纯实验多次用到了玻璃棒,请写出该实验中使用玻璃棒的一个作用① ;
(2)蒸发后所得食盐质量② (读数见图)。

实验二:物质检验
【提出问题】食盐中除含有NaCl外,可能还含有什么溶质?
【查阅资料一】食盐中可能还含有Na2CO3、Na2SO4等。
【作出猜想】猜想一:含有溶质Na2CO3;
猜想二:含有溶质Na2SO4;
猜想三:③ 。
【查阅资料二】Na2CO3溶液、Na2SO4溶液均可以与BaCl2溶液反应生成白色沉淀,且BaCO3可以溶于盐酸,BaSO4不能溶于盐酸。
【讨论交流】小组同学经讨论后认为:选择BaCl2溶液和稀盐酸两种试剂即可验证猜想。若猜想二正确,则发生反应的化学方程式为④ 。
【实验验证】为验证猜想,小组同学设计了如下实验方案。
Ⅰ.取上述食盐样品少量于试管中,加水溶解,得到澄清透明溶液;
Ⅱ.向溶液中滴加过量的BaCl2溶液,生成白色沉淀,静置;
Ⅲ.静置后弃去清液,加入足量稀盐酸,发现沉淀部分溶解,且有气泡产生。
【实验结论】根据上述实验现象判断⑤ 是正确的(填“猜想一”、“猜想二”或“猜想三”)。
【问题与交流】小组同学在实验报告中记录了如下文字:经实验验证,该食盐样品中仅含有NaCl、Na2CO3和Na2SO4,你认为这个观点⑥ (填“正确”或“错误”)。请说明你选择的理由⑦ 。
实验一:粗盐提纯
(1)提纯实验多次用到了玻璃棒,请写出该实验中使用玻璃棒的一个作用① ;
(2)蒸发后所得食盐质量② (读数见图)。

实验二:物质检验
【提出问题】食盐中除含有NaCl外,可能还含有什么溶质?
【查阅资料一】食盐中可能还含有Na2CO3、Na2SO4等。
【作出猜想】猜想一:含有溶质Na2CO3;
猜想二:含有溶质Na2SO4;
猜想三:③ 。
【查阅资料二】Na2CO3溶液、Na2SO4溶液均可以与BaCl2溶液反应生成白色沉淀,且BaCO3可以溶于盐酸,BaSO4不能溶于盐酸。
【讨论交流】小组同学经讨论后认为:选择BaCl2溶液和稀盐酸两种试剂即可验证猜想。若猜想二正确,则发生反应的化学方程式为④ 。
【实验验证】为验证猜想,小组同学设计了如下实验方案。
Ⅰ.取上述食盐样品少量于试管中,加水溶解,得到澄清透明溶液;
Ⅱ.向溶液中滴加过量的BaCl2溶液,生成白色沉淀,静置;
Ⅲ.静置后弃去清液,加入足量稀盐酸,发现沉淀部分溶解,且有气泡产生。
【实验结论】根据上述实验现象判断⑤ 是正确的(填“猜想一”、“猜想二”或“猜想三”)。
【问题与交流】小组同学在实验报告中记录了如下文字:经实验验证,该食盐样品中仅含有NaCl、Na2CO3和Na2SO4,你认为这个观点⑥ (填“正确”或“错误”)。请说明你选择的理由⑦ 。
31.人体摄入锌不足会引起多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌口服液来补锌。已知葡萄糖酸锌的化学式C12H22O14Zn。
(1)葡萄糖酸锌属于 (填“有机物”或者“无机物”),由 种元素组成。
(2)现有一支20mL的葡萄糖酸锌口服液,其中含葡萄糖酸锌45mg,那么这支口服液中Zn的质量是 mg。(结果保留两位有效数字)
(1)葡萄糖酸锌属于 (填“有机物”或者“无机物”),由 种元素组成。
(2)现有一支20mL的葡萄糖酸锌口服液,其中含葡萄糖酸锌45mg,那么这支口服液中Zn的质量是 mg。(结果保留两位有效数字)
32.某工厂利用废铁屑与废硫酸反应制取绿矾(FeSO4•7H2O)。
(1)绿矾中铁原子与氧原子个数比为 。
(2)现有废硫酸4.9t(硫酸的质量分数为20%)与足量的废铁屑反应,理论上可生产出绿矾的质量是多少?(请写出计算过程,结果保留三位有效数字,下同)
(3)若配制100g质量分数为20%的稀硫酸溶液,需质量分数为98%的浓硫酸的体积是多少?(已知:质量分数为98%的浓硫酸的密度为1.84g/cm3)。
(1)绿矾中铁原子与氧原子个数比为 。
(2)现有废硫酸4.9t(硫酸的质量分数为20%)与足量的废铁屑反应,理论上可生产出绿矾的质量是多少?(请写出计算过程,结果保留三位有效数字,下同)
(3)若配制100g质量分数为20%的稀硫酸溶液,需质量分数为98%的浓硫酸的体积是多少?(已知:质量分数为98%的浓硫酸的密度为1.84g/cm3)。
查看全部题目