下载高清试卷
【2018年湖南省娄底市中考化学试卷】-第1页
试卷格式:2018年湖南省娄底市中考化学试卷.PDF
试卷热词:最新试卷、2018年、湖南试卷、娄底市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.生活中变化无处不在。下列变化属于化学变化的是( )
- A. 汽油挥发
- B. 粮食酿酒
- C. 石蜡融化
- D. 木材成椅
2.化学是一门以实验为基础的科学。下列实验操作正确的是( )
- A.
 取固体药品
取固体药品 - B.
 闻气体气味
闻气体气味 - C.
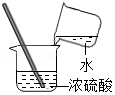 稀释浓硫酸
稀释浓硫酸 - D.
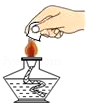 熄灭酒精灯
熄灭酒精灯
3.我们每天都得保证各种营养素的均衡摄入。以下食物主要提供蛋白质的是( )
- A. 鸡蛋
- B. 大米
- C. 黄瓜
- D. 植物油
4.掌握好化学用语,有利于化学学习。下列化学用语使用正确的是( )
- A. 镁原子结构示意图:
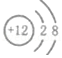
- B. 硝酸根离子:NO3
- C. 两个水分子:2H2O
- D. 氧化铁FeO
5.陕西西安咸新区,记者在一个植树现场看到发放罐装空气。据介绍是秦岭深处的富氧空气,采用压缩罐包装。下列关于压缩罐高氧空气说法正确的是( )
- A. 空气被压缩分子之间间隔减小
- B. 空气被压缩分子本身发生变化
- C. 空气被压缩分子停止运动
- D. 空气被压缩分子变小
6.下列关于实验现象的描述中,正确的是( )
- A. 打开盛有浓盐酸的试剂瓶,在瓶口观察到白烟
- B. 硫在氧气中燃烧,产生蓝紫色的火焰
- C. 木炭在高温下还原氧化铜,固体由红色逐渐变黑
- D. 镁条在空气中燃烧会发出耀眼的白光,生成黑色固体
7.下列关于溶液说法正确的是( )
- A. 将硫酸钠和汽油放入水中,充分搅拌后都能形成溶液
- B. 把30%的硝酸钾溶液均分成两份,每份溶液的溶质质量分数为15%
- C. 向20℃时的蔗糖饱和溶液中加入食盐,食盐不再溶解
- D. 配制100g10%的氯化钠溶液一般经过计算、称量(或量取)、溶解、装瓶存放等步骤
8.2018年3月,国务院总理李克强在政府工作报告中强调:“坚决打好蓝天保卫战”。 各地积极行动,落实措施。下列做法错误的是( )
- A. 积极推广使用新能源公交车
- B. 火力发电厂进行脱硫、控尘处理
- C. 禁止化石燃料的使用
- D. 限制、禁止燃放烟花爆竹
9.同学们通过一年来的化学学习,了解了一些物质的“个性”,小真同学对物质“个性”认识错误的是( )
- A. 氧气有可燃性
- B. 浓硫酸有吸水性
- C. CO有毒性
- D. 石墨有导电性
10.豆浆被称为“植物奶”,其中的异黄酮(C15H10O2)具有防癌功能,下列关于异黄酮的说法错误的是( )
- A. 异黄酮是由分子构成的
- B. 异黄酮中碳、氢、氧三种元素的质量比为15:10:2
- C. 异黄酮是由碳、氢、氧三种元素组成
- D. 异黄酮的相对分子质量为222
11.如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是( )


- A. 20℃时,甲、乙两种物质的溶解度相同
- B. 甲物质溶解度大于乙物质溶解度
- C. 30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为90g
- D. 将20℃时两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大
12.下列实验能达到实验目的是( )
- A.
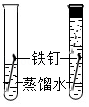 探究铁锈蚀条件
探究铁锈蚀条件 - B.
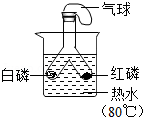 探究燃烧条件
探究燃烧条件 - C.
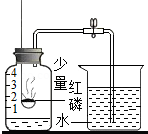 测定空气中氧气含量
测定空气中氧气含量 - D.
 探究分子运动
探究分子运动
13.某有机物在9.6g氧气中恰好完全燃烧,生成8.8g CO2和5.4g H2O,下列说法正确的是( )
- A. 该有机物只含碳、氢两种元素
- B. 该有机物中一定含有碳、氢元素,可能含有氧元素
- C. 该有机物中一定含有碳、氢、氧三种元素
- D. 无法确定
14.化学趣味小组在学习了金属的化学性质后,对金属R的活动性进行探究发现:将金属R放入稀盐酸中,观察到有气泡产生(该反应的化学方程式可表示为:R+2HCl=RCl2+H2↑),将R放入ZnSO4溶液中无任何变化。下列化学方程式书写错误的是( )
- A. R+MgSO4═RSO4+Mg
- B. R+CuSO4═RSO4+Cu
- C. R+H2SO4═RSO4+H2↑
- D. 2Al+3RSO4═Al2(SO4)3+3R
15.提纯是化学实验常用的一种方法。除去下表混合物中的杂质,所选除杂试剂错误的是( )
| 选项 | 混合物(括号内为杂质) | 除杂试剂 |
| A | NaOH溶液(Na2CO3) | 适量的氢氧化钙溶液 |
| B | CaO粉末(CaCO3) | 足量的蒸馏水 |
| C | Cu粉(Fe) | 足量的稀硫酸 |
| D | CuSO4溶液(H2SO4) | 足量的氧化铜粉末 |
- A. A
- B. B
- C. C
- D. D
16.化学与人类生产、生活息息相关,现有以下物质(请选择合适物质的序号填空):
①稀硫酸 ②甲烷③小苏打 ④熟石灰
(1)工业上通常用来除铁锈的是 ;
(2)生活中常用作焙制糕点的发酵粉的主要成分是 ;
(3)可以用来做建筑材料的是 ;
(4)天然气的主要成分是 。
①稀硫酸 ②甲烷③小苏打 ④熟石灰
(1)工业上通常用来除铁锈的是 ;
(2)生活中常用作焙制糕点的发酵粉的主要成分是 ;
(3)可以用来做建筑材料的是 ;
(4)天然气的主要成分是 。
17.化学在保证人类生存并不断提高生活质量方面起着重要作用。
(1)利用化学生产化肥和农药,以增加粮食的产量,下列肥料属于复合肥的是
A、KNO3 B、CO(NH2)2 C、K2SO4 D、Ca3(PO4)2
(2)钛合金与人体具有很好的“相容性”,可以用来制造人造骨。钛合金属于 (填“纯净物”或“混合物”)
(3)家庭里常常使用活性炭净水器来净化水,利用了活性炭的 性。
(1)利用化学生产化肥和农药,以增加粮食的产量,下列肥料属于复合肥的是
A、KNO3 B、CO(NH2)2 C、K2SO4 D、Ca3(PO4)2
(2)钛合金与人体具有很好的“相容性”,可以用来制造人造骨。钛合金属于 (填“纯净物”或“混合物”)
(3)家庭里常常使用活性炭净水器来净化水,利用了活性炭的 性。
18.元素周期表是学习化学的重要工具。如图是元素周期表中的一部分,请回答下列问题:
(1)表中,①所示元素的名称是 ,相对分子质量最小的氧化物的化学式 。
(2)X2﹣与Ar的核外电子排布相同,则X的元素符号是 ,它处在元素周期表中第 周期;
(3)元素周期表中同族和同周期元素具有一定的相似性和变化规律,同族元素化学性质相似的原因是 相同。
| 第一周期 | 1 H | 2 He | ||||||
| 第二周期 | 3 Li | 4 Be | 5 B | 6 C | ① | 8 O | 9 F | 10 Ne |
| 第三周期 | 11 Na | 12 Mg | 13 Al | 14 Si | 15 P | 16 S | 17 Cl | 18 Ar |
(1)表中,①所示元素的名称是 ,相对分子质量最小的氧化物的化学式 。
(2)X2﹣与Ar的核外电子排布相同,则X的元素符号是 ,它处在元素周期表中第 周期;
(3)元素周期表中同族和同周期元素具有一定的相似性和变化规律,同族元素化学性质相似的原因是 相同。
19.分析、归纳、推理是学习化学的重要方法,请同学们根据下面微观粒子反应(在水式溶液中进行反应,水分子已省略)示意图,分析解决下列问题。
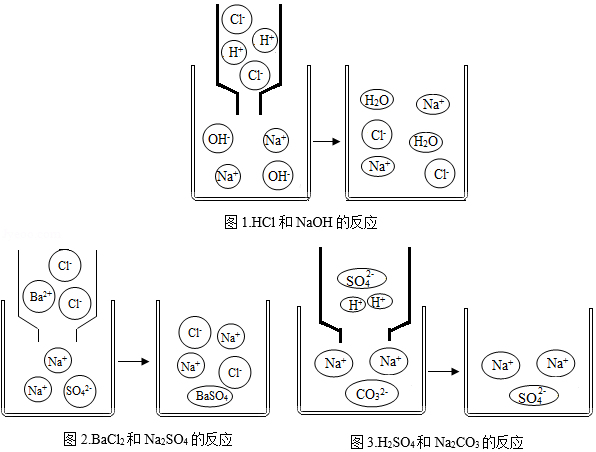
(1)请根据图1、图2、图3任写一个反应的化学方程式 。该反应属于 反应(填基本反应类型);
(2)任选一个反应从微观角度分析该反应的实质 。
(3)请你认真分析图1、图2、图3,从微观角度说明该反应类型发生反应的实质 。

(1)请根据图1、图2、图3任写一个反应的化学方程式 。该反应属于 反应(填基本反应类型);
(2)任选一个反应从微观角度分析该反应的实质 。
(3)请你认真分析图1、图2、图3,从微观角度说明该反应类型发生反应的实质 。
20.2018年5月23日至25日,第九届中国卫星导航年会在哈尔滨拉开帷幕,中海达、华大北斗等一批国内企业先后发布了自主研发的北斗芯片产品。芯片的主要成分是硅,如图是工业上以石英砂(SiO2)为主要原料制取纯硅的种方法,请回答以下问题。
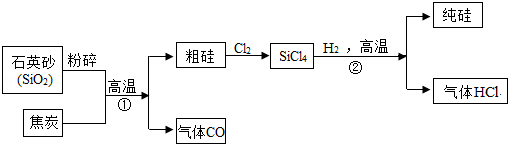
(1)地壳中硅元素的含量仅次于 元素;
(2)写出反应①的化学方程 ;
(3)反应②的基本反应类型是 ;
(4)尾气氯化氢必须收集处理,不能排放到空气中,请简要说明原因 。

(1)地壳中硅元素的含量仅次于 元素;
(2)写出反应①的化学方程 ;
(3)反应②的基本反应类型是 ;
(4)尾气氯化氢必须收集处理,不能排放到空气中,请简要说明原因 。
21.如图是实验室制取和收集气体的常用装置图,请根据所给的装置图回答下列问题:

(1)请写出装置图A中标号①的仪器名称: 。
(2)实验室既能制取氧气,也能制取二氧化碳的发生装置为 (填字母代号),请写出用该装置制取二氧化碳的化学方程式 。
(3)实验室常用氯化铵固体和熟石灰固体混合加热制取极易溶于水的氨气(NH3的相对分子质量为17),请根据以上装置图选择,在实验室制取氨气时的发生装置和收集装置为 (填字母代号)。
(4)实验室里通常用MnO2与浓盐酸在加热条件下制取氯气,同时生成MnCl2和水,请写出该反应的化学方程式 ,如果用F装置收集氯气(Cl2的相对分子质量为71),气体应从 (填“a”或“b”) 端管口通入。

(1)请写出装置图A中标号①的仪器名称: 。
(2)实验室既能制取氧气,也能制取二氧化碳的发生装置为 (填字母代号),请写出用该装置制取二氧化碳的化学方程式 。
(3)实验室常用氯化铵固体和熟石灰固体混合加热制取极易溶于水的氨气(NH3的相对分子质量为17),请根据以上装置图选择,在实验室制取氨气时的发生装置和收集装置为 (填字母代号)。
(4)实验室里通常用MnO2与浓盐酸在加热条件下制取氯气,同时生成MnCl2和水,请写出该反应的化学方程式 ,如果用F装置收集氯气(Cl2的相对分子质量为71),气体应从 (填“a”或“b”) 端管口通入。
22.某实验小组的同学在学习了铁的冶炼后,想探究炼铁高炉排放出的高炉气体中含有污染环境的气体有哪些,请我们共同参与探究并回答下列问题:
【提出问题】高炉气体中含有污染环境的气体是什么?
【作出猜想】猜想一:只有CO;
猜想二:只有SO2;
猜想三:CO和SO2都有;
【查阅资料】二氧化硫能使澄清石灰水变浑浊(与CO2相似),能使品红溶液褪色,可被酸性高锰酸钾溶液吸收。
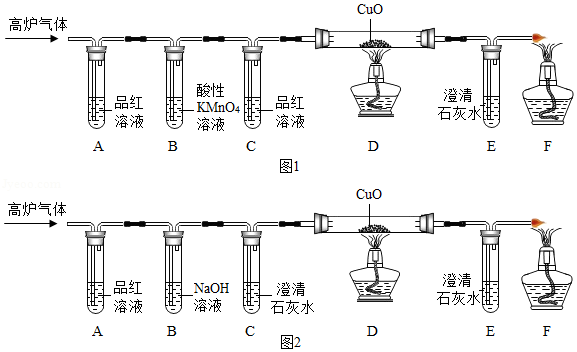
【实验探究】该实验小组的同学组装了如图1装置进行实验。
(1)甲同学在实验中发现A中品红溶液褪色,高炉气体中含有气体 ,B中酸性高锰酸钾溶液的作用是 ,C 中品红溶液的作用是 ;
(2)乙同学发现C中品红溶液没有褪色,E中澄清石灰水变浑浊,得出高炉气体中含有CO。丙同学认为乙同学的结论不正确,理由是 。
(3)该实验小组的同学经过讨论后,改进了实验装置,如图2所示。用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是 ,写出SO2与 NaOH溶液反应的化学方程式 。
【实验结论】炼铁厂排放的高炉气体中含有有害气体CO和SO2,直接排放到空气中会污染环境,需达标后才能排放。
【提出问题】高炉气体中含有污染环境的气体是什么?
【作出猜想】猜想一:只有CO;
猜想二:只有SO2;
猜想三:CO和SO2都有;
【查阅资料】二氧化硫能使澄清石灰水变浑浊(与CO2相似),能使品红溶液褪色,可被酸性高锰酸钾溶液吸收。
【实验探究】该实验小组的同学组装了如图1装置进行实验。
(1)甲同学在实验中发现A中品红溶液褪色,高炉气体中含有气体 ,B中酸性高锰酸钾溶液的作用是 ,C 中品红溶液的作用是 ;
(2)乙同学发现C中品红溶液没有褪色,E中澄清石灰水变浑浊,得出高炉气体中含有CO。丙同学认为乙同学的结论不正确,理由是 。
(3)该实验小组的同学经过讨论后,改进了实验装置,如图2所示。用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是 ,写出SO2与 NaOH溶液反应的化学方程式 。
【实验结论】炼铁厂排放的高炉气体中含有有害气体CO和SO2,直接排放到空气中会污染环境,需达标后才能排放。

23.高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO+2Fe(NO3) 3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
(1)次氯酸钠(NaClO) 中Cl元素的化合价为 ;
(2)高铁酸钠(Na2FeO4)中铁元素和氧元素的质量比为 (填最简比);
(3)现要制得830kg含杂质20%的高铁酸钠,至少需要次氯酸钠的质量是多少?(列式计算)
(1)次氯酸钠(NaClO) 中Cl元素的化合价为 ;
(2)高铁酸钠(Na2FeO4)中铁元素和氧元素的质量比为 (填最简比);
(3)现要制得830kg含杂质20%的高铁酸钠,至少需要次氯酸钠的质量是多少?(列式计算)
查看全部题目