下载高清试卷
【2020年山东省潍坊市市区中考化学二模试卷】-第1页
试卷格式:2020年山东省潍坊市市区中考化学二模试卷.PDF
试卷热词:最新试卷、2020年、山东试卷、潍坊市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.中华民族有着光辉灿烂的文明史。下列变化不属于化学变化的是( )
- A.
 粮食酿酒
粮食酿酒 - B.
 陶瓷烧制
陶瓷烧制 - C.
 东汉炼钢
东汉炼钢 - D.
 淘沙取金
淘沙取金
2.正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是( )
- A.
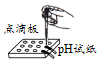 测定溶液pH
测定溶液pH - B.
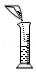 配制溶液
配制溶液 - C.
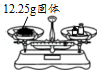 称量固体
称量固体 - D.
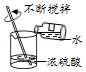 稀释浓硫酸
稀释浓硫酸
3.2020年3月23是第60个世界气象日,今年世界气象日的主旨是呼吁大家关注气候变化,合理利用资源,以下做法不正确的是( )
- A. 外卖、网购等包装用品分类回收,综合利用
- B. 过期食品因为含碳,一律焚烧处理
- C. 推广网络学习和无纸化办公
- D. 用LED灯作为光源照明,少用空调,温控适宜
4.“分类”可以使人们有序地研究物质。以下分类正确的是( )
- A. 碱:苛性钠、纯碱、熟石灰
- B. 合金:硬铝、青铜、18K金
- C. 酸:硝酸、硫酸、碳酸氢钠
- D. 糖类:蔗糖、纤维素、蛋白质
5.我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是( )


- A. 镓元素位于第三周期,属于金属元素
- B. 镓原子核内有31个中子
- C. 镓的相对原子质量是69.72g
- D. 氮化镓的化学式为GaN
6.下列关于燃烧现象的解释或分析正确的是( )
- A.
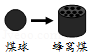 如图中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
如图中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间 - B.
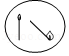 如图中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
如图中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点 - C.
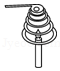 如图中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
如图中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动 - D.
 由如图中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
由如图中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
7.化学是你,化学是我,化学深入我们的生活。下列做法不正确的是( )
- A. 用小苏打作糕点膨松剂
- B. 用甲醛溶液浸泡海鲜食品
- C. 用洗涤剂除去餐桌上的油污
- D. 用活性炭除去冰箱中的异味
8.“宏观﹣微观﹣符号”三重表征是化学独特的表示物质及其变化的方法。某化学反应的微观示意图如图所示,下列说法不正确的是( )
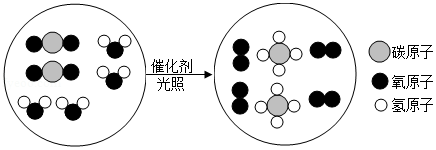

- A. 从反应价值看:该反应能获取清洁能源,延缓温室效应
- B. 从物质分类看:该反应涉及到2种氧化物
- C. 从微观构成看:四种物质均由分子构成
- D. 从表示方法看:该反应的化学方程式为2CO2+4H2O2CH4+4O2
光照 催化剂
9.善于归纳知识,有利于培养素质.下列知识整理的内容不完全正确的一组是( )
| A.安全常识 | B.化学与生活 |
| 假酒中毒﹣﹣由甲醇引起煤矿爆炸﹣﹣由瓦斯引起假盐中毒﹣﹣由NaNO2引起 | 除去餐具油污﹣﹣用洗洁精乳化人体缺乏维生素A﹣﹣引起夜盲症干冰﹣﹣用于人工降雨鉴别羊毛和合成纤维﹣﹣点燃后闻气味 |
| C.化学实验数据记录 | D.化学中常见的“三” |
| 用10 mL量筒量取7.25 mL水用pH试纸测得苹果汁的pH为3.2用托盘天平称取5.6 g铁粉 | 煤、石油、天然气﹣三大化石燃料塑料、合成纤维、合成橡胶﹣三大合成材料分子、原子、离子﹣构成物质的三种粒子 |
- A. A
- B. B
- C. C
- D. D
10.根据下列实验方案进行实验,能达到相应实验目的是( )
- A.
 比较Zn和Fe的金属活动性强弱
比较Zn和Fe的金属活动性强弱 - B.
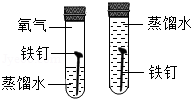 探究铁钉生锈时O2是否参与反应
探究铁钉生锈时O2是否参与反应 - C.
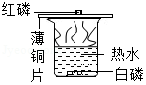 比较红磷和白磷的着火点
比较红磷和白磷的着火点 - D.
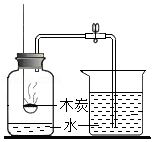 测定空气中O2的含量
测定空气中O2的含量
11.国务院联防联控机制于2020年2月17日召开新闻发布会,药磷酸氯喹在细胞水平上能有效抑制新型冠状病毒的感染。磷酸氯喹的化学式为C18H26ClN3•2H3PO4,关于磷酸氯喹的说法正确的是( )
- A. 磷酸氯喹是由7种元素组成的有机物
- B. 磷酸氯喹分子由64个原子构成
- C. 磷酸氯喹中碳、氢、氧元素的质量比为9:16:4
- D. 磷酸氯喹的相对分子质量是515.5
12.下列各组物质的溶液,不用其他试剂,只用观察和组内物质相互混合的方法,不能将它们一一鉴别的是( )
- A. HCl NaOH FeCl3 NaCl
- B. H2SO4 NaCl Na2CO3 CaCl2
- C. NaNO3 HCl CaCl2 KOH
- D. MgCl2 KOH Cu(NO3)2 Na2SO4
13.化学学习者常用化学思维去认识和理解世界。下列选项正确的是( )
- A. 变化与守恒:依据化学方程式X+2O22CO2+2H2O,可推测X的化学式为C2H4O
点燃 - B. 模型与推理:置换反应中一定有元素化合价变化,则有元素化合价发生变化的反应一定是置换反应
- C. 宏观与微观:CO和CO2虽然元素组成相同,但二者性质不同,原因是分子构成不同
- D. 探究与创新:探究氧化铜是否为过氧化氢分解的催化剂,设计实验证明氧化铜能否改变反应速率即可
14.下列有关物质的鉴别、除杂、分离所用的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 鉴别氯化钾溶液和硝酸钾溶液 | AgNO3溶液 |
| B | 除去氧化钙中的碳酸钙 | 加水,过滤,烘干 |
| C | 除去氯化钠溶液中的硝酸钾 | 降温结晶 |
| D | 分离氯化钾固体与二氧化锰 | 溶解、过滤 |
- A. A
- B. B
- C. C
- D. D
15.甲、乙两工厂排放的污水各含下列离子H+、Cu2+、K+、NO3﹣、OH﹣中的三种(两厂含有一种相同的离子)若将两厂的污水按一定比例混合,沉淀后污水会变成无色澄清中性溶液。下列关于污水的分析,正确的是( )
- A. OH﹣和Cu2+来自同一工厂
- B. H+和OH﹣来自同一工厂
- C. Cu2+和K+来自同一工厂
- D. H+和Cu2+来自同一工厂
16.如图为甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线。下列相关说法中正确的是( )
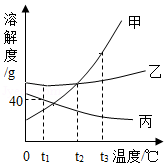

- A. 甲和乙两物质的饱和溶液温度从t3℃降至t2℃时,析出晶体质量甲>乙
- B. 将接近饱和的丙溶液变为饱和溶液,可以采用升高溶液温度的方法
- C. 甲中含少量乙时,采用蒸发溶剂的方法提纯甲
- D. t1℃时,30g丙物质加入到50g水中形成溶液的质量为80g
17.将金属M的粉末放入盛有硝酸铜溶液的烧杯中,充分反应后,溶液呈无色,继续向烧杯中加入一定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液。根据上述实验分析,下列说法错误的是( )
- A. 金属活动性强弱顺序:M>Cu>Ag
- B. 滤渣中可能有金属M
- C. 滤液中至少含有两种溶质
- D. 滤渣中一定有Ag
18.下列图象不能正确反映其对应变化关系的是( )
- A.
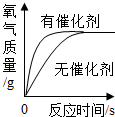 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 - B.
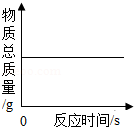 一定质量的红磷在密闭容器中燃烧
一定质量的红磷在密闭容器中燃烧 - C.
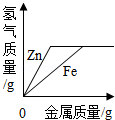 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 - D.
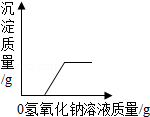 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
19.有一包白色粉末。可能含有Ba(NO3)2,Na2SO4,Na2CO3,NaNO3中的一种或几种,某同学分析其成分做了如下实验。该同学分析正确是( )
| 实验步骤 | 1 | 2 |
| 实验操作 | 取样加足量水,充分振荡,静置 | 过滤后,往滤渣中加过量稀盐酸 |
| 实验现象 | 有白色沉淀产生 | 沉淀部分溶解 |
- A. 该包白色粉末中一定含有Ba(NO3)2、Na2SO4、Na2CO3、NaNO3
- B. 该包白色粉末中一定含有Ba(NO3)2、Na2CO3可能含有Na2SO4
- C. 该包白色粉末中一定含有Ba(NO3)2、Na2SO4可能含有NaNO3、Na2CO3
- D. 该包白色粉末中一定含有Ba(NO3)2、Na2SO4、Na2CO3可能含有NaNO3
20.向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法不正确的是( )
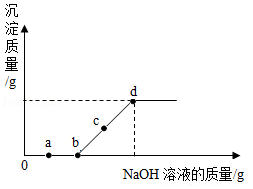

- A. a点溶液中滴入紫色石蕊试液变红
- B. bc段(不含b点)反应的化学方程式为MgCl2+2NaOH═Mg(OH)2↓+2NaCl
- C. 整个变化过程中氯离子数目没有改变
- D. d点溶液中含有两种溶质
21.家庭厨房就是一个化学小世界,“锅碗瓢盆”和“柴米油盐”中包含着许多的化学知识。
(1)如图所示厨房用品的主要材料,属于金属材料的是 (填序号,下同);属于有机合成材料的是 。

(2)均衡膳食,有利于人体健康,小强家某天午饭的食谱如表:
从营养学的角度考虑,你建议食谱中应增加下列中的 (填写序号)。
A.油饼 B.烧豆腐 C.凉拌黄瓜 D.炒鸡蛋
(3)烹煮牛肉汤时,为了解汤的咸味,小强取锅中少量汤品尝。取少量汤进行品尝就可知道整锅汤咸淡如何,是因为溶液具有 (填一条性质)。
(4)食醋中一般含有3%﹣5%的醋酸,醋酸又叫乙酸(CH3COOH),是无色有刺激性气味的液体,能溶于水。乙酸属于 (填“有机化合物”或“无机化合物“)。用铁锅炒菜时,放一点食醋能更好补铁的原因是 。
(1)如图所示厨房用品的主要材料,属于金属材料的是 (填序号,下同);属于有机合成材料的是 。

(2)均衡膳食,有利于人体健康,小强家某天午饭的食谱如表:
| 主食 | 馒头 |
| 副食 | 红烧排骨、花生米、清蒸鱼 |
| 饮料 | 牛奶 |
从营养学的角度考虑,你建议食谱中应增加下列中的 (填写序号)。
A.油饼 B.烧豆腐 C.凉拌黄瓜 D.炒鸡蛋
(3)烹煮牛肉汤时,为了解汤的咸味,小强取锅中少量汤品尝。取少量汤进行品尝就可知道整锅汤咸淡如何,是因为溶液具有 (填一条性质)。
(4)食醋中一般含有3%﹣5%的醋酸,醋酸又叫乙酸(CH3COOH),是无色有刺激性气味的液体,能溶于水。乙酸属于 (填“有机化合物”或“无机化合物“)。用铁锅炒菜时,放一点食醋能更好补铁的原因是 。
22.在环境治理和新能源开发中,化学发挥着不可替代的作用。
(一)保护环境:燃煤容易导致环境污染。其中烟气脱硫是目前控制燃煤污染的重要途径,如钠碱循环法是利用亚硫酸钠(Na2SO3)溶液脱除烟气中的SO2,生成亚硫酸氢钠(NaHSO3),反应的化学方程式为: 。
(二)研制新物质:中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过如图示意的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油(图中c、d是最终制得的汽油中所含物质的分子结构模型)。
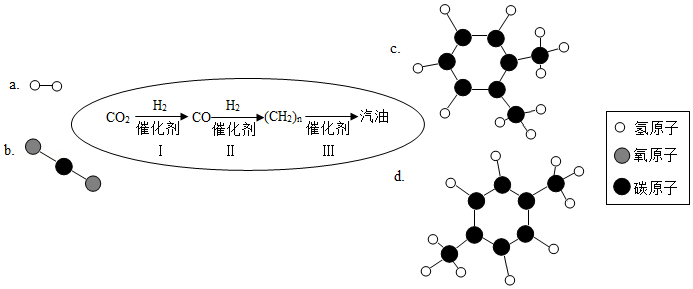
(1)在一定温度、一定压强和催化剂存在的条件下,环节Ⅰ除生成CO外,还生成了一种化合物,则反应的化学方程式为 。
(2)观察图中c和d两种物质的分子结构模型,发现c和d的分子组成完全相同,但其分子结构不同,化学上将其称为同分异构体。你认为c和d的化学性质 (填“是”或“否”)完全相同。
(三)海洋资源开发利用:从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合如图所示流程图(其中部分操作和条件已略去),请回答相关问题:

(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为 (填字母序号)。
a.稍过量的Na2CO3溶液 b、稍过量的BaCl2溶液 c、稍过量的NaOH溶液
(2)母液中有MgCl2,却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是 。
(3)步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是 ,写出该反应的化学方程式 。
(一)保护环境:燃煤容易导致环境污染。其中烟气脱硫是目前控制燃煤污染的重要途径,如钠碱循环法是利用亚硫酸钠(Na2SO3)溶液脱除烟气中的SO2,生成亚硫酸氢钠(NaHSO3),反应的化学方程式为: 。
(二)研制新物质:中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过如图示意的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油(图中c、d是最终制得的汽油中所含物质的分子结构模型)。

(1)在一定温度、一定压强和催化剂存在的条件下,环节Ⅰ除生成CO外,还生成了一种化合物,则反应的化学方程式为 。
(2)观察图中c和d两种物质的分子结构模型,发现c和d的分子组成完全相同,但其分子结构不同,化学上将其称为同分异构体。你认为c和d的化学性质 (填“是”或“否”)完全相同。
(三)海洋资源开发利用:从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合如图所示流程图(其中部分操作和条件已略去),请回答相关问题:

(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为 (填字母序号)。
a.稍过量的Na2CO3溶液 b、稍过量的BaCl2溶液 c、稍过量的NaOH溶液
(2)母液中有MgCl2,却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是 。
(3)步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是 ,写出该反应的化学方程式 。
23.在“宏观一微观一符号”之间建立联系,能帮助我们更好地认识物质变化的本质。
(1)将铝片插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示,(图中微粒未完全画出)回答下列问题。
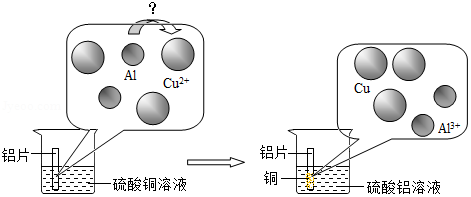
①下列说法中正确的是 。
A.硫酸铜溶液中含有的微粒是Cu2+、SO42﹣
B.硫酸铜溶液能导电
C.反应的实质是Al得电子生成Al3+、Cu2+失电子生成Cu
D.硫酸铜溶液呈蓝色,硫酸铝溶液为无色,说明蓝色与Cu2+有关
②反应过程实质是金属铝与硫酸铜溶液中 (填微粒的化学式)的反应。
(2)如图为Mn和CuSO4溶液反应的示意图,回答下列问题:
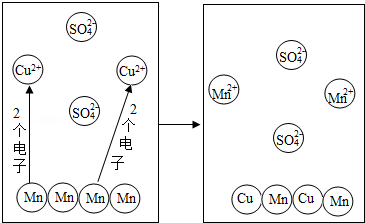
①反应中失去电子的粒子是 。
②由反应可知金属的活泼性:Mn Cu(填“>”或“<”)。
③该反应中化合价没有改变的元素或根是 (填对应选项的字母)。
A.锰元素
B.铜元素
C.硫酸根
(1)将铝片插入硫酸铜溶液中,经研究发现该反应的微观示意图如图所示,(图中微粒未完全画出)回答下列问题。

①下列说法中正确的是 。
A.硫酸铜溶液中含有的微粒是Cu2+、SO42﹣
B.硫酸铜溶液能导电
C.反应的实质是Al得电子生成Al3+、Cu2+失电子生成Cu
D.硫酸铜溶液呈蓝色,硫酸铝溶液为无色,说明蓝色与Cu2+有关
②反应过程实质是金属铝与硫酸铜溶液中 (填微粒的化学式)的反应。
(2)如图为Mn和CuSO4溶液反应的示意图,回答下列问题:

①反应中失去电子的粒子是 。
②由反应可知金属的活泼性:Mn Cu(填“>”或“<”)。
③该反应中化合价没有改变的元素或根是 (填对应选项的字母)。
A.锰元素
B.铜元素
C.硫酸根
24.稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物(Y2O3)广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y2O3约70%,含Fe2O3、CuO、SiO2 等约30%)生产大颗粒氧化钇的一种工艺如图:
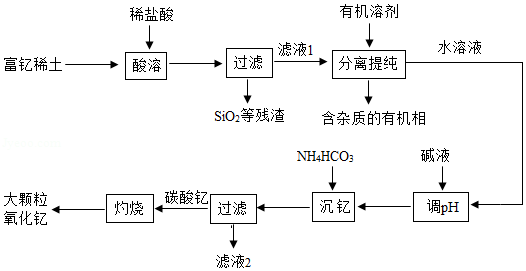
(1)氧化钇(Y2O3)中,Y元素的化合价为 。
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是 。
(3)“分离提纯”是为了除去滤液1中的 (填化学式)。
(4)“调pH”时加入碱液使溶液的pH (填“增大”或“减小”)。
(5)碳酸钇灼烧分解的化学方程式是 。
(6)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如下(D50表示颗粒直径):
分析上表数据,其他条件不变时,若将灼烧温度均升高至1400℃,预期所得氧化钇D50最大的是 (填实验编号)。

(1)氧化钇(Y2O3)中,Y元素的化合价为 。
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是 。
(3)“分离提纯”是为了除去滤液1中的 (填化学式)。
(4)“调pH”时加入碱液使溶液的pH (填“增大”或“减小”)。
(5)碳酸钇灼烧分解的化学方程式是 。
(6)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如下(D50表示颗粒直径):
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 沉淀反应温度/℃ | 60 | 80 | 85 | 93 | 93 | 93 |
| 料液浓度/(g/L) | 30 | 30 | 30 | 30 | 40 | 40 |
| 灼烧温度/℃ | 1100 | 1100 | 1100 | 1100 | 1100 | 1400 |
| 氧化钇D50/um | 6.00 | 21.65 | 35.99 | 38.56 | 35.99 | 61.54 |
分析上表数据,其他条件不变时,若将灼烧温度均升高至1400℃,预期所得氧化钇D50最大的是 (填实验编号)。
25.某兴趣小组的同学探究浓硫酸与铁钉(碳素钢)反应后产生气体的成分。
【查阅资料】
①Fe与浓H2SO4反应,加热,有SO2生成;
②C与浓H2SO4反应,加热,有CO2和SO2生成;
③SO2可使澄清石灰水变浑浊;
④SO2可使品红溶液的红色褪去,而CO2不能;
⑤SO2可与酸性KMnO4溶液反应使其褪色,而CO2不能。
【实验探究】
(1)称取24.0g铁钉放入60.0mL浓硫酸中,加热,充分反应后得到的溶液X并收集到气体Y.甲同学通过实验测定并推知气体Y中SO2气体的体积分数为66.7%.同学们认为气体Y中还可能还有H2和Z气体,则Z气体可能是 。探究实验的主要装置如图1所示:
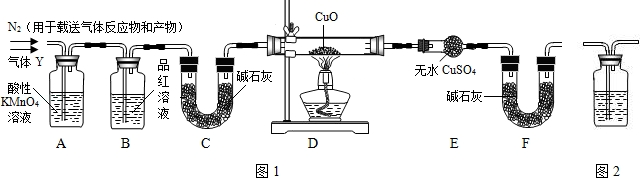
(2)装置A中试剂的作用是 ,装置B中试剂的作用是 。
(3)为确认Z的存在,需要将装置(如图2所示)接入上述装置的(填编号) 之间。装置中的液体名称是 。
(4)实验中,如果观察到 现象可确认Y中还有H2气体。
(5)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞。已知二氧化硅与二氧化碳的化学性质相似。常温下氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,产物使瓶口与瓶塞粘合在一起,写出其中反应的化学方程式: 。
(6)载人航天飞行器的模拟座中,空气更新过程如图所示。
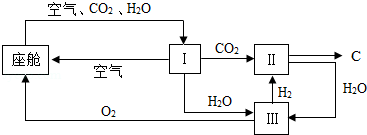
①装置Ⅰ的作用是 。
②装置(Ⅱ)中的CO2和H2在催化剂条件下发生了反应,其反应的化学方程式为 。
③从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,若产生896g O2,消耗1012g CO2,则同时消耗H2O g。
【查阅资料】
①Fe与浓H2SO4反应,加热,有SO2生成;
②C与浓H2SO4反应,加热,有CO2和SO2生成;
③SO2可使澄清石灰水变浑浊;
④SO2可使品红溶液的红色褪去,而CO2不能;
⑤SO2可与酸性KMnO4溶液反应使其褪色,而CO2不能。
【实验探究】
(1)称取24.0g铁钉放入60.0mL浓硫酸中,加热,充分反应后得到的溶液X并收集到气体Y.甲同学通过实验测定并推知气体Y中SO2气体的体积分数为66.7%.同学们认为气体Y中还可能还有H2和Z气体,则Z气体可能是 。探究实验的主要装置如图1所示:

(2)装置A中试剂的作用是 ,装置B中试剂的作用是 。
(3)为确认Z的存在,需要将装置(如图2所示)接入上述装置的(填编号) 之间。装置中的液体名称是 。
(4)实验中,如果观察到 现象可确认Y中还有H2气体。
(5)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞。已知二氧化硅与二氧化碳的化学性质相似。常温下氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,产物使瓶口与瓶塞粘合在一起,写出其中反应的化学方程式: 。
(6)载人航天飞行器的模拟座中,空气更新过程如图所示。

①装置Ⅰ的作用是 。
②装置(Ⅱ)中的CO2和H2在催化剂条件下发生了反应,其反应的化学方程式为 。
③从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,若产生896g O2,消耗1012g CO2,则同时消耗H2O g。
26.高纯MnCO3是制备电信器材高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如图:
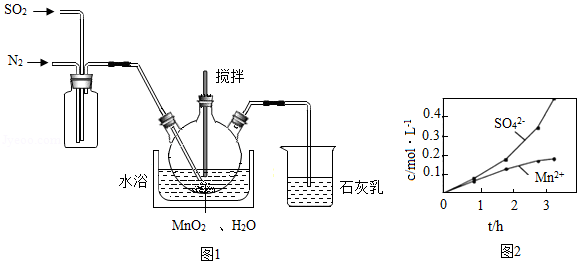
【查阅资料】
①向烧瓶中(见图1)通入过量混合气进行“浸锰”操作,主要反应原理为:SO2+H2O═H2SO3;MnO2+H2SO3═MnSO4+H2O。
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末。
⑧用Na2CO3溶液调节pH为3.5左右,过滤。
④调节滤液pH为6.5~7.2,加入NH4HCO3,观察到有少量气体生成,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。
⑤H2SO3和O2在催化剂的催化作用下生成H2SO4。
【实验探究】
(1)①图1中应该先通入 ,一段时间再通入 ,原因是 ,石灰乳的作用是 (用化学方程式表示)。
②若实验中将N2换成空气,测得反应液中Mn2+、SO42﹣的浓度随反应时间t变化如图2所示,导致溶液中Mn2+、SO42﹣,浓度变化产生明显差异的原因是 ,此时Mn2+的作用是 。
③反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施是 (写出一条即可)。
(2)加入的NH4HCO3与MnSO4溶液发生反应,请写出其化学方程式 。

【查阅资料】
①向烧瓶中(见图1)通入过量混合气进行“浸锰”操作,主要反应原理为:SO2+H2O═H2SO3;MnO2+H2SO3═MnSO4+H2O。
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末。
⑧用Na2CO3溶液调节pH为3.5左右,过滤。
④调节滤液pH为6.5~7.2,加入NH4HCO3,观察到有少量气体生成,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。
⑤H2SO3和O2在催化剂的催化作用下生成H2SO4。
【实验探究】
(1)①图1中应该先通入 ,一段时间再通入 ,原因是 ,石灰乳的作用是 (用化学方程式表示)。
②若实验中将N2换成空气,测得反应液中Mn2+、SO42﹣的浓度随反应时间t变化如图2所示,导致溶液中Mn2+、SO42﹣,浓度变化产生明显差异的原因是 ,此时Mn2+的作用是 。
③反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施是 (写出一条即可)。
(2)加入的NH4HCO3与MnSO4溶液发生反应,请写出其化学方程式 。
27.实验室某混合溶液由硫酸和硫酸铜溶液组成。探究小组同学进行了如下实验:取124.5g该混合溶液于烧杯中,然后将120gNaOH溶液分六次加入其中,每次充分反应后称量所得溶液及沉淀的质量,所测数据如下表所示。
计算:(1)上述表格中产生沉淀的质量:m= ,n=
(2)所加NaOH溶液中溶质的质量分数。
(3)第5次加入NaOH溶液充分反应后所得溶液中溶质的质量分数。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入NaOH溶液的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 反应后溶液的质量/g | 144.5 | 164.5 | 179.6 | 189.8 | 200 | 220 |
| 每次产生沉淀的质量/g | 0 | 0 | m | n | 9.8 | 0 |
计算:(1)上述表格中产生沉淀的质量:m= ,n=
(2)所加NaOH溶液中溶质的质量分数。
(3)第5次加入NaOH溶液充分反应后所得溶液中溶质的质量分数。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解