下载高清试卷
【2019年山西省大同市中考化学一模试卷】-第1页
试卷格式:2019年山西省大同市中考化学一模试卷.PDF
试卷热词:最新试卷、2019年、山西试卷、大同市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.我们生活在不断变化的物质世界中,下列变化属于物理变化的是( )
- A. 纸张燃烧
- B. 湿衣服晾干
- C. 铁钉生锈
- D. 葡萄酿酒
2.化学实验是进行科学探究的重要途径。下列实验操作符合规范要求的是( )
- A. 用燃着的酒精灯引燃另一盏酒精灯
- B. 在点燃氢气之前先检验氢气的纯度
- C. 与滴瓶配套的胶头滴管使用完毕,清洗后放回原瓶
- D. 稀释浓硫酸时,将水沿玻璃棒慢慢注入浓硫酸中,并不断搅拌
3.“青山绿水就是金山银山”。为了实现这一目标,菏泽市多地已经开始实行电动公交出行,推广太阳能路灯,升级改造燃煤锅炉。你认为下列做法与这一理念不相符的是( )
- A. 工业废水经处理达标后排放
- B. 尽量不使用一次性塑料袋购物,减少“白色污染”
- C. 植树造林,增大绿化面积
- D. 加高燃煤锅炉烟囱,将废气排到高空
4.O2和CO2总与我们如影随形,下列关于它们的叙述中不正确的是( )
- A. O2具有助燃性,而CO2可用来灭火
- B. 空气中O2过多无害,而CO2过多会形成酸雨
- C. 它们都可用向上排空气法收集
- D. 自然界里它们可通过光合作用和呼吸作用相互转化
5.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。由此分析下列说法正确的是( )


- A. 反应前后阴、阳离子的总数目不变
- B. 反应前后溶剂质量不变
- C. 反应后溶液呈中性
- D. 反应前后元素种类发生了变化
6.化学与人类的生活密切相关。下列对化学知识的应用归纳完全正确的一组是( )
| A.化学与生活 | B.化学与安全 |
| ①用活性炭包可吸附汽车内的异味②用洗涤剂可以洗掉衣服和餐具上的油污 | ①炒菜时油锅着火可以用锅盖盖灭②在室内放一盆水能防止煤气中毒 |
| C.化学与资源 | D.化学与健康 |
| ①煤、石油、天然气都是可再生能源②我国试采可燃冰成功,为未来使用新能源提供可能 | ①烧烤食品营养丰富,可大量食用②每天食用适量蔬菜,以补充维生素 |
- A. A
- B. B
- C. C
- D. D
7.归纳和演绎是重要的科学方法。下列归纳或演绎合理的是( )
- A. 有机物是一类含碳化合物,所以CH4、CO2都是有机物
- B. 硫酸、盐酸电离时都能产生H+,所以电离能产生H+的化合物是酸
- C. 金属Fe、Zn能与酸反应生成氢气,所以金属都能与酸反应生成氢气
- D. 氧化物是由两种元素组成,其中一种是氧元素的化合物,所以水是氧化物
8.除去下列物质中的少量杂质(括号内为杂质),所选试剂正确的是( )
- A. CaCO3粉末(CaCl2粉末)﹣﹣水
- B. CaO粉末[Ca(OH)2粉末]﹣﹣水
- C. KCl溶液(KOH)﹣﹣稀硝酸
- D. NaOH溶液(Na2CO3)﹣﹣稀盐酸
9.甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )


- A. 20℃时,甲溶液中溶质的质量分数一定比乙溶液的大
- B. 将40℃时甲的一定量饱和溶液降温至20℃,溶液质量不变
- C. 甲的溶解度大于乙的溶解度
- D. 40℃时,分别在100g水中各加入30g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液
10.下列四个图象能正确反映其对应实验操作的是( )
- A.
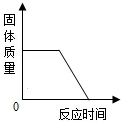 用一氧化碳气体还原一定质量的氧化铁粉末
用一氧化碳气体还原一定质量的氧化铁粉末 - B.
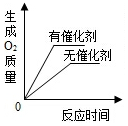 用两份等质量、等浓度的过氧化氢溶液分别制取氧气
用两份等质量、等浓度的过氧化氢溶液分别制取氧气 - C.
 向一定体积的稀盐酸中逐滴加入足量的氢氧化钠溶液
向一定体积的稀盐酸中逐滴加入足量的氢氧化钠溶液 - D.
 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
11.化学源于生活,生活中蕴含着许多化学知识:
(1)用洗涤剂去除油污,是利用洗涤剂的 作用;
(2)邵阳地区的生活用水多是硬水,生活中常用 的方法降低水的硬度;
(3)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随 而减小;
(4)医生给胃酸过多的病人所开处方中,常包括含Al(OH)3的药物,试用化学方程式表示其治疗原理 。
(1)用洗涤剂去除油污,是利用洗涤剂的 作用;
(2)邵阳地区的生活用水多是硬水,生活中常用 的方法降低水的硬度;
(3)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随 而减小;
(4)医生给胃酸过多的病人所开处方中,常包括含Al(OH)3的药物,试用化学方程式表示其治疗原理 。
12.从干冰、铝、烧碱、硫酸、纯碱、生石灰等物质中,选择恰当的物质,完成下列有关问题:
(1)属于碱的是 (填化学式,下同)
(2)可用作制冷剂的氧化物是 。
(1)属于碱的是 (填化学式,下同)
(2)可用作制冷剂的氧化物是 。
13.根据图文回答下列问题。

(1)汽水是常见的饮料,打开瓶盖汽水会自动喷出。
①汽水属于 混合物 (填“纯净物”或“混合物”)。
②汽水中的气体的溶解度随压强减小而 减小 (填“增大”或“减小”)。
③汽水瓶的材质属于 合成 (填“金属”或“合成”)材料。
④汽水的pH范围是2.2~4.9,呈 酸 (填“酸”、“碱”或“中”)性。
(2)在中秋节,人们有食用月饼的习俗。
①营养成分表中的“钠”是指 元素 (填“元素”或“单质”)。
②营养成分表中“蛋白质”属于 有机 (填“无机”或“有机”)物。
③下列制月饼的原料,属于糖类的是 A (填序号)。

(1)汽水是常见的饮料,打开瓶盖汽水会自动喷出。
①汽水属于 混合物 (填“纯净物”或“混合物”)。
②汽水中的气体的溶解度随压强减小而 减小 (填“增大”或“减小”)。
③汽水瓶的材质属于 合成 (填“金属”或“合成”)材料。
④汽水的pH范围是2.2~4.9,呈 酸 (填“酸”、“碱”或“中”)性。
(2)在中秋节,人们有食用月饼的习俗。
①营养成分表中的“钠”是指 元素 (填“元素”或“单质”)。
②营养成分表中“蛋白质”属于 有机 (填“无机”或“有机”)物。
③下列制月饼的原料,属于糖类的是 A (填序号)。
- A. 面粉
- B. 植物油
- C. 鸡蛋
④纸袋内的生石灰的作用是 。
14.二氧化氯(ClO2)是一种环保型杀菌消毒剂。在生活中主要用于饮用水的消毒和食品保鲜。用二氧化氯消毒后的水可以直接饮用。
二氧化氯是一种黄绿色、有刺激性气味的有毒气体,密度比空气大,其熔点为﹣59℃,沸点为11.0℃,易溶于水,且与水反应得到酸性溶液。该气体具有强烈的腐蚀性,吸入高浓度二氧化氯气体会引起咳嗽和呼吸道粘膜的损伤。
二氧化氯极其不稳定,受热或见光易发生爆炸性分解,直接造成氯气泄漏而污染环境,所以只有依靠现场制备。工业上用稍潮湿的氯酸钾(KClO3)和草酸(H2C2O4)在60℃时反应制得。由于制取二氧化氯需要使用的氯酸钾是易爆危险品,所以制备和运输成本很高,因此我国目前还未广泛用其消毒自来水。
请依据上文回答下列问题:
(1)本文介绍了二氧化氯的性质、制法和 等方面的内容。
(2)二氧化氯的化学性质有① ;② 。
(3)请将制备二氧化氯反应的化学方程式填写完整:
2KClO3+2H2C2O4
2ClO2↑+2CO2↑+K2C2O4+ 。
(4)发生二氧化氯泄漏时,最简单的紧急处理方法是 。
二氧化氯是一种黄绿色、有刺激性气味的有毒气体,密度比空气大,其熔点为﹣59℃,沸点为11.0℃,易溶于水,且与水反应得到酸性溶液。该气体具有强烈的腐蚀性,吸入高浓度二氧化氯气体会引起咳嗽和呼吸道粘膜的损伤。
二氧化氯极其不稳定,受热或见光易发生爆炸性分解,直接造成氯气泄漏而污染环境,所以只有依靠现场制备。工业上用稍潮湿的氯酸钾(KClO3)和草酸(H2C2O4)在60℃时反应制得。由于制取二氧化氯需要使用的氯酸钾是易爆危险品,所以制备和运输成本很高,因此我国目前还未广泛用其消毒自来水。
请依据上文回答下列问题:
(1)本文介绍了二氧化氯的性质、制法和 等方面的内容。
(2)二氧化氯的化学性质有① ;② 。
(3)请将制备二氧化氯反应的化学方程式填写完整:
2KClO3+2H2C2O4
| 60℃ |
(4)发生二氧化氯泄漏时,最简单的紧急处理方法是 。
15.下列是钠元素、氯元素在元素周期表中的信息及有关粒子的结构示意图,请回答下列问题: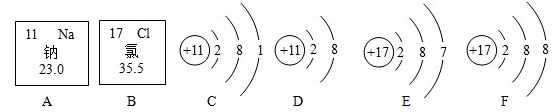
(1)D所表示的粒子是 (填化学符号),氯原子的结构示意图是 (填序号)。
(2)D、F形成化合物的化学式是 。
(3)与元素的化学性质关系最密切的是 (填序号)。
①原子的核外电子数 ②元素的相对原子质量
③元素的原子序数 ④原子的最外层电子数。

(1)D所表示的粒子是 (填化学符号),氯原子的结构示意图是 (填序号)。
(2)D、F形成化合物的化学式是 。
(3)与元素的化学性质关系最密切的是 (填序号)。
①原子的核外电子数 ②元素的相对原子质量
③元素的原子序数 ④原子的最外层电子数。
16.A、B、C、D、E、F是初中化学常见的六种物质,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如图所示(短线“一”相连的物质间能反应,箭头“→”表示能生成)。
(1)A的化学式为 ;A与C的反应属于 反应(填基本反应类型)。
(2)写出下列反应或转化的化学方程式:
B与C反应: ,D转化为E: 。
(3)写出F的一种用途: 。
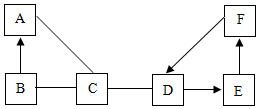
(1)A的化学式为 ;A与C的反应属于 反应(填基本反应类型)。
(2)写出下列反应或转化的化学方程式:
B与C反应: ,D转化为E: 。
(3)写出F的一种用途: 。

17.向K2CO3溶液中滴入Ba(OH)2溶液至恰好完全反应。
(1)可以观察到的实验现象是 。
(2)如图表示该反应前后溶液中存在的主要离子,写出下列图形代表的离子。(填离子符号)● ; 。
。
(3)下列物质能与K2CO3溶液反应产生类似上述实验现象的是 。
A. Ca(OH)2 B. HCl C. BaCl2 D. (NH4)2SO4

(1)可以观察到的实验现象是 。
(2)如图表示该反应前后溶液中存在的主要离子,写出下列图形代表的离子。(填离子符号)● ;
 。
。(3)下列物质能与K2CO3溶液反应产生类似上述实验现象的是 。
A. Ca(OH)2 B. HCl C. BaCl2 D. (NH4)2SO4

18.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下稀盐酸和氢氧化钙发生的中和反应实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是 ;
【查阅资料】CaCl2溶液显中性,
CaCl2+Na2CO3═CaCO3↓+2NaCl
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:
反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2
猜想Ⅱ:有
猜想Ⅲ:有CaCl2和Ca(OH)2
猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是 ;
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
【得出结论】通过探究,全班同学一致确定猜想Ⅲ是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因 ;
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑 。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是 ;
【查阅资料】CaCl2溶液显中性,
CaCl2+Na2CO3═CaCO3↓+2NaCl
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:
反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2
猜想Ⅱ:有
猜想Ⅲ:有CaCl2和Ca(OH)2
猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是 ;
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
| 实验方案 | 滴加紫色石蕊试液 | 通入CO2 | 滴加Na2CO3溶液 |
| 实验操作 | 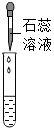 | 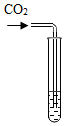 | 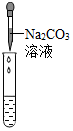 |
| 实验现象 | 产生白色沉淀 | ||
| 实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想Ⅲ是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因 ;
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑 。
19.某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下

请回答下列问题:
(1)滤液可作化肥使用,你认为它属于 肥;
(2)该同学制得氧气的质量 g;
(3)计算滤液中溶质质量分数。

请回答下列问题:
(1)滤液可作化肥使用,你认为它属于 肥;
(2)该同学制得氧气的质量 g;
(3)计算滤液中溶质质量分数。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解