下载高清试卷
【2021年重庆市中考化学试卷(A卷)】-第1页
试卷格式:2021年重庆市中考化学试卷(A卷).PDF
试卷热词:最新试卷、2021年、重庆试卷、化学试卷、九年级试卷、中考试卷、初中试卷

扫码查看解析
试卷题目
1.2021年世界环境日中国主题是“人与自然和谐共生”。下列做法不符合这一理念的是( )
- A. 坚持绿色出行
- B. 野外焚烧垃圾
- C. 教科书循环使用
- D. 废旧电池回收处理
2.铁是目前人类使用最广泛的金属。下列过程中没有发生化学变化的是( )
- A. 铁丝织网
- B. 矿石炼铁
- C. 钢铁生锈
- D. 湿法炼铜
3.分类是学习化学的一种方法,下列物质属于纯净物的是( )
- A. 糖水
- B. 空气
- C. 黄铜
- D. 干冰
4.2021年印度新冠疫情加剧,导致其国内氧气供应严重不足。下列关于氧气的说法错误的是( )
- A. 用于医疗急救
- B. 易溶于水
- C. 能使带火星木条复燃
- D. 可贮存在钢瓶中
5.叶子发黄的水稻易倒伏,专家建议施用含钾的复合肥料。下列肥料符合要求的是( )
- A. NH4NO3
- B. KNO3
- C. NH4H2PO4
- D. K2SO4
6.实验室里,可用火法制备锰的化学方程式为4Al+3MnO2
2Al2O3+3Mn,其中表现出还原性的物质是( )
| 高温 |
- A. Al
- B. MnO2
- C. Al2O3
- D. Mn
7.2021年3月22日是“世界水日”,自来水净水过程中不涉及的环节是( )
- A. 沉淀
- B. 蒸馏
- C. 吸附
- D. 消毒
8.生产生活中常用氮气作保护气,主要是因为氮气( )
- A. 无色无味
- B. 密度与空气接近
- C. 熔沸点低
- D. 化学性质不活泼
9.从中草药中提取的calebin A(化学式为C21H20O7)可用于治疗阿尔茨海默症。下列关于calebin A的说法错误的是( )
- A. 属于有机物
- B. 由碳、氢、氧三种元素组成
- C. 一个分子由48个原子构成
- D. 其中氧元素的质量分数最小
10.“火锅”当选为“重庆十大文化符号”之首。下列做法合理的是( )
- A. 清洗用过的筷子并高温消毒
- B. 用甲醛溶液处理毛肚
- C. 在门窗紧闭的家里吃炭火火锅
- D. 吃清洗过的霉变苕粉
11.实验室制取二氧化碳部分操作如图所示,其中错误的是( )
- A.
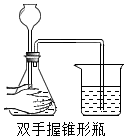 检查气密性
检查气密性 - B.
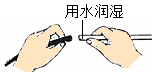 仪器连接
仪器连接 - C.
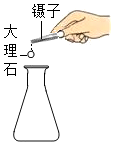 加入药品
加入药品 - D.
 收集气体
收集气体
12.2020年科学家开发出新型催化剂,光照下能将二氧化碳转化为甲烷,微观示意图如图,下列关于该反应的说法正确的是( )
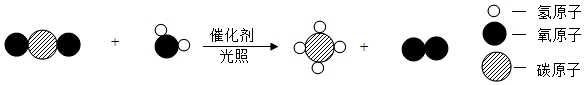

- A. 属于置换反应
- B. 反应前后原子种类改变
- C. 反应中涉及2种氧化物
- D. 参加反应的反应物分子个数比为1:1
13.我国“天问一号”探测器成功着陆火星,发现火星地表被赤铁矿覆盖,平均温度约为﹣56℃,火星大气中含有CO2(体积分数为95.3%)、O2、H2O等物质,下列说法正确的是( )
- A. 火星上白磷无法自燃
- B. 火星上缺少金属资源
- C. 火星大气组成与空气相似
- D. 火星地表不存在固态水
14.石油古称“洧水”,《汉书》中“高奴县洧水可燃”、《梦溪笔谈》中“予知其烟可用,试扫其烟为墨,黑光如漆”,下列关于“洧水”的说法错误的是( )
- A. 具有可燃性
- B. 是一种黏稠状液体
- C. 是可再生能源
- D. “其烟”的主要成分为炭黑
15.下列实验目的通过对应实验操作能达到的是( )
| 序号 | 实验目的 | 实验操作 |
| A | 除去CO中的H2 | 通过灼热CuO |
| B | 鉴别MnO2粉末和木炭粉 | 分别加水搅拌 |
| C | 除去KNO3溶液中的KCl | 加入过量AgNO3溶液后过滤 |
| D | 鉴别化肥NH4Cl和KNO3 | 分别加入熟石灰研磨后闻气味 |
- A. A
- B. B
- C. C
- D. D
16.向盛有硫酸和硫酸铜混合溶液的烧杯中滴入Ba(OH)2溶液,烧杯中溶质的质量与加入的Ba(OH)2溶液的质量关系如图所示。下列有关说法正确的是( )
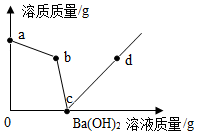

- A. a→b段溶液的质量一定减小
- B. b→c段有水生成
- C. b点溶液溶质为硫酸铜
- D. d点沉淀质量与b点沉淀质量相等
17.糖尿病检验原理之一是将含有葡萄糖(C6H12O6)的尿液与新制Cu(OH)2共热,产生砖红色沉淀,该沉淀为氧化亚铜,请用化学用语填空。
(1)2个铜原子 ,3个氢氧根离子 。
(2)铜元素常显0、+1、+2价,氧化亚铜的化学式为 。
(3)葡萄糖在人体内缓慢氧化生成CO2和 ,并释放能量。
(1)2个铜原子 ,3个氢氧根离子 。
(2)铜元素常显0、+1、+2价,氧化亚铜的化学式为 。
(3)葡萄糖在人体内缓慢氧化生成CO2和 ,并释放能量。
18.人体中质量分数在0.01%以下的元素称为微量元素。如图表示部分元素在人体中的质量分数及有关元素信息。
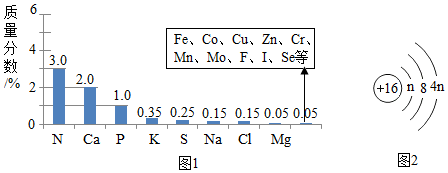
(1)图1中钙元素为 (填“常量”或“微量”)元素。
(2)图2为某粒子的结构示意图,其最外层电子数为 。
(3)以铁元素为主要成分的生铁比纯铁硬度 (填“大”或“小”)。
(4)钾在空气中加热发生化合反应生成超氧化钾(KO2)的化学方程式为 。

(1)图1中钙元素为 (填“常量”或“微量”)元素。
(2)图2为某粒子的结构示意图,其最外层电子数为 。
(3)以铁元素为主要成分的生铁比纯铁硬度 (填“大”或“小”)。
(4)钾在空气中加热发生化合反应生成超氧化钾(KO2)的化学方程式为 。
19.NaOH、KNO3和Na2CO3在不同温度下的溶解度如下表所示。
下列实验过程中不考虑化学变化、水的热发和结晶水合物等因素。
(1)10℃时,KNO3的溶解度 (填“>”、“<”或“=”)Na2CO3的溶解度。
(2)20℃时,将129g NaOH固体加入到100g水中,搅拌后固体全部消失,放置到t1时刻开始析出固体,到t2时刻析出10g固体。
①t1时刻为 (填“饱和”或“不饱和”)溶液。
②t2时刻溶液的温度为 ℃。
(3)40℃时,将等质量的三种物质的饱和溶液冷却到30℃,所得溶液中溶剂质量最多的是 (填序号)。
A.Na2CO3溶液 B.KNO3溶液 C.NaOH溶液
| 物质溶解度/g温度℃ | 0 | 10 | 20 | 30 | 40 |
| NaOH | 42.0 | 51.0 | 109.0 | 119.0 | 129.0 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
| Na2CO3 | 6.0 | 16.0 | 18.0 | 36.5 | 50.0 |
下列实验过程中不考虑化学变化、水的热发和结晶水合物等因素。
(1)10℃时,KNO3的溶解度 (填“>”、“<”或“=”)Na2CO3的溶解度。
(2)20℃时,将129g NaOH固体加入到100g水中,搅拌后固体全部消失,放置到t1时刻开始析出固体,到t2时刻析出10g固体。
①t1时刻为 (填“饱和”或“不饱和”)溶液。
②t2时刻溶液的温度为 ℃。
(3)40℃时,将等质量的三种物质的饱和溶液冷却到30℃,所得溶液中溶剂质量最多的是 (填序号)。
A.Na2CO3溶液 B.KNO3溶液 C.NaOH溶液
20.“嫦娥五号“上使用的记忆合金、SiC颗粒增强铝基复合材料、高性能芳纶纤维等材料引起了全世界的关注。
(1)下列属于有机合成材料的是 (填序号)。
A.记忆合金 B.羊毛 C.芳纶纤维
(2)硬度非常大的SiC,其结构类似金刚石,则构成SiC的基本粒子为 (填序号)。
A.分子 B.原子 C.离子
(3)工业制取记忆合金中的钛,先用热浓硫酸处理钛铁矿(主要成分为FeTiO3)反应中元素化合价不变,得到硫酸钛[Ti(SO4)2]、硫酸亚铁和一种氧化物,FeTiO3中钛元素的化合价为 ,化学方程式为 。
(1)下列属于有机合成材料的是 (填序号)。
A.记忆合金 B.羊毛 C.芳纶纤维
(2)硬度非常大的SiC,其结构类似金刚石,则构成SiC的基本粒子为 (填序号)。
A.分子 B.原子 C.离子
(3)工业制取记忆合金中的钛,先用热浓硫酸处理钛铁矿(主要成分为FeTiO3)反应中元素化合价不变,得到硫酸钛[Ti(SO4)2]、硫酸亚铁和一种氧化物,FeTiO3中钛元素的化合价为 ,化学方程式为 。
21.某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图所示(部分产物略去)
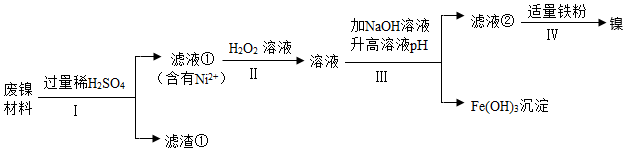
查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+。
b.Fe3+、Ni2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)步骤Ⅰ的操作为 。
(2)滤渣①的成分为 。
(3)单质Fe参与反应的化学方程式为 (任写一个)。
(4)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为 (填序号)。
A.pH=1 B.pH=2 C.pH=6 D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为 。

查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+。
b.Fe3+、Ni2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)步骤Ⅰ的操作为 。
(2)滤渣①的成分为 。
(3)单质Fe参与反应的化学方程式为 (任写一个)。
(4)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为 (填序号)。
A.pH=1 B.pH=2 C.pH=6 D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为 。
22.氧气的制取和性质是初中化学的重要内容,根据如图所示的装置回答问题。
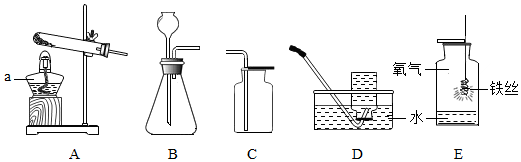
(1)仪器a常用 (填“内焰”“外焰”或“焰心”)加热。
(2)用H2O2溶液和MnO2制取O2的化学方程式为 。实验室里欲制取和收集一瓶干燥的O2,需选用的装置是 (填序号)。
(3)装置E中水的作用是 。
(4)若将铁丝改为少量木炭进行实验,为了检验产物,可将水换成 (填名称)。

(1)仪器a常用 (填“内焰”“外焰”或“焰心”)加热。
(2)用H2O2溶液和MnO2制取O2的化学方程式为 。实验室里欲制取和收集一瓶干燥的O2,需选用的装置是 (填序号)。
(3)装置E中水的作用是 。
(4)若将铁丝改为少量木炭进行实验,为了检验产物,可将水换成 (填名称)。
23.某兴趣小组查阅资料发现除去泥沙等杂质的粗盐,可能还含有CaCl2、MgCl2、Na2SO4等杂质。他们将该粗盐配成溶液,并对粗盐溶液进行探究和除杂。
(1)配制溶液时,加速粗盐溶解的玻璃仪器是 。
【探究过程】
(2)步骤1:向粗盐溶液中加入过量NaOH溶液,未出现明显现象,说明溶液中有 杂质;向溶液中继续滴加过量Na2CO3溶液,产生白色沉淀CaCO3固体。反应的化学方程式为 。
(3)步骤2:向步骤1的滤液中滴加过量BaCl2溶液,产生白色沉淀,过滤;向滤液中滴加稀盐酸至溶液呈中性即得NaCl溶液。加稀盐酸除去的物质是 。
【初步结论】杂质成分已确定,且已完全除去。
【反思交流】
(4)小东认为Na2SO4还不能确定是否存在,可向步骤2的沉淀中滴加过量稀盐酸,若观察到 的现象,证明粗盐中确实存在Na2SO4。
(5)小红认为杂质也未完全除去,可按照步骤1和步骤2重新实验,并对调其中两种试剂的位置就能达到除杂目的,这两种试剂为 (填序号)。
A.Na2CO3溶液、BaCl2溶液
B.稀盐酸、BaCl2溶液
C.NaOH溶液、Na2CO3溶液
(1)配制溶液时,加速粗盐溶解的玻璃仪器是 。
【探究过程】
(2)步骤1:向粗盐溶液中加入过量NaOH溶液,未出现明显现象,说明溶液中有 杂质;向溶液中继续滴加过量Na2CO3溶液,产生白色沉淀CaCO3固体。反应的化学方程式为 。
(3)步骤2:向步骤1的滤液中滴加过量BaCl2溶液,产生白色沉淀,过滤;向滤液中滴加稀盐酸至溶液呈中性即得NaCl溶液。加稀盐酸除去的物质是 。
【初步结论】杂质成分已确定,且已完全除去。
【反思交流】
(4)小东认为Na2SO4还不能确定是否存在,可向步骤2的沉淀中滴加过量稀盐酸,若观察到 的现象,证明粗盐中确实存在Na2SO4。
(5)小红认为杂质也未完全除去,可按照步骤1和步骤2重新实验,并对调其中两种试剂的位置就能达到除杂目的,这两种试剂为 (填序号)。
A.Na2CO3溶液、BaCl2溶液
B.稀盐酸、BaCl2溶液
C.NaOH溶液、Na2CO3溶液
24.二氧化氯(ClO2)常用于自来水消毒,工业制取原理为:2NaClO3+4HCl(浓)═2ClO2↑+2NaCl+Cl2↑+2H2O。某工厂将30kg NaClO3固体加到100kg浓盐酸中,反应一段时间后,生成13.5kg ClO2(生成的气体全部逸出,其它物质全部形成溶液)。
已知:NaClO3和ClO2的相对分子质量分别为106.5和67.5。
试计算:
(1)NaClO3中钠元素和氧元素的质量比为 。
(2)参加反应的NaClO3的质量。
(3)所得溶液中NaClO3的质量分数(计算结果精确到1%)
已知:NaClO3和ClO2的相对分子质量分别为106.5和67.5。
试计算:
(1)NaClO3中钠元素和氧元素的质量比为 。
(2)参加反应的NaClO3的质量。
(3)所得溶液中NaClO3的质量分数(计算结果精确到1%)
查看全部题目