下载高清试卷
【2021年河南省中考化学试卷】-第1页
试卷格式:2021年河南省中考化学试卷.PDF
试卷热词:最新试卷、2021年、河南试卷、化学试卷、九年级试卷、中考试卷、初中试卷

扫码查看解析
试卷题目
1.河南博物院馆藏丰富。下列相关制作过程中一定发生了化学变化的是( )
- A. 玉柄雕琢
- B. 骨笛打孔
- C. 彩陶烧制
- D. 金简刻字
2.日常生活中,用得最多的材料是有机合成材料。下列不属于有机合成材料的是( )
- A. 合金
- B. 塑料
- C. 合成橡胶
- D. 合成纤维
3.侯德榜是我国制碱工业的先驱。侯氏制碱法中的“碱”是指其化学式为( )
- A. Na2CO3
- B. NaHCO3
- C. NaOH
- D. NaCl
4.“84”消毒液的主要成分是次氯酸钠(NaClO)。NaClO中氯元素的化合价为( )
- A. ﹣1
- B. +1
- C. +5
- D. +7
5.下列物质在氧气里燃烧,能生成有刺激性气味气体的是( )
- A. 木炭
- B. 硫粉
- C. 铁丝
- D. 镁条
6.古籍记载“曾青得铁则化为铜”,指可溶性的铜的化合物与铁反应得到铜,该反应为( )
- A. 化合反应
- B. 分解反应
- C. 置换反应
- D. 复分解反应
7.规范的操作方法是实验安全和成功的保证。下列图示的实验操作正确的是( )
A.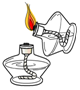 点燃酒精灯B.
点燃酒精灯B.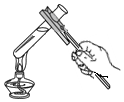 加热液体C.
加热液体C. 收集氢气D.
收集氢气D.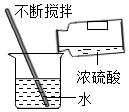 稀释浓硫酸
稀释浓硫酸
A.
 点燃酒精灯B.
点燃酒精灯B. 加热液体C.
加热液体C. 收集氢气D.
收集氢气D. 稀释浓硫酸
稀释浓硫酸- A. A
- B. B
- C. C
- D. D
8.2021年世界水日的主题是“珍惜水、爱护水”。下列说法正确的是( )
- A. 地球上的淡水资源十分丰富
- B. 部分结冰的蒸馏水属于混合物
- C. 水是由氢分子和氧原子构成的
- D. 硬水中含有较多可溶性钙、镁化合物
9.黑火药爆炸时的反应为S+2KNO3+3C
X+N2↑+3CO2↑。则X是( )
| 点燃 |
- A. K2S
- B. K2SO3
- C. K2SO4
- D. K2S2O3
10.如图是KNO3和NaCl的溶解度曲线。下列说法正确的是( )
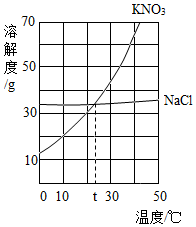

- A. KNO3的溶解度大于NaCl的溶解度
- B. t℃时,两种物质的饱和溶液中溶质的质量分数相等
- C. 30℃时,30g NaCl加入到100g水中可得到饱和溶液
- D. 将40℃时一定质量的KNO3的饱和溶液降温到20℃,该溶液中溶质的质量保持不变
11.现有下列反应:①2KMnO4
K2MnO4+MnO2+O2↑;②KClO3
2KCl+3O2↑;③2NH4NO3
4H2O+2NO2↑+O2↑。其中适用于实验室制取氧气的是( )
| △ |
| MnO2 |
| △ |
| △ |
- A. ①②
- B. ②③
- C. ①③
- D. ①②③
12.下列根据某些性质区分一些常见物质的方法错误的是( )
- A. 羊毛和涤纶:灼烧闻气味
- B. 硫酸铵和氯化铵:加熟石灰研磨
- C. 铜片和黄铜片:相互刻画
- D. 氧气和二氧化碳:伸入燃着的木条
13.下列四个图像分别与选项中的操作相对应,其中可能合理的是( )
- A.
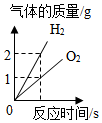 电解一定质量的水
电解一定质量的水 - B.
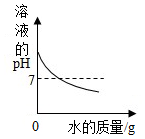 向一定质量的氢氧化钠溶液中滴加水
向一定质量的氢氧化钠溶液中滴加水 - C.
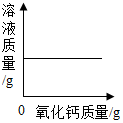 向一定质量的饱和氢氧化钙溶液中加入氧化钙
向一定质量的饱和氢氧化钙溶液中加入氧化钙 - D.
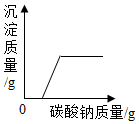 向一定质量的盐酸和氯化钙混合溶液中滴加碳酸钠溶液
向一定质量的盐酸和氯化钙混合溶液中滴加碳酸钠溶液
14.现将含有某一种氯化物杂质的MgCl2粉末95g溶于水后,与足量的AgNO3溶液反应,可生成AgCl沉淀290g。则该MgCl2粉末中含有的杂质可能是( )
- A. NaCl
- B. CaCl2
- C. AlCl3
- D. KCl
15.空气中含量多且常用作保护气的是 ;人体中含量最高的元素是 。
16.大米、面粉中含有的糖类物质主要是淀粉,淀粉的化学式为 [填“C2H5OH”“C6H12O6”或(C6H10O5)n];施用化肥是农业增产的重要手段,尿素[CO(NH)2]属于 (填“氮肥”“磷肥”或“钾肥”)。
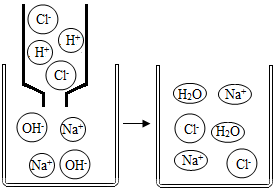
17.氢氧化钠溶液与盐酸反应的化学方程式为 。如图是该反应的微观示意图,则该反应前后没有发生变化的离子有 ;从微观角度看,该化学反应的实质是 。

18.实验室除去粗食盐中难溶性杂质的主要实验步骤有溶解、 、蒸发;除去粗食盐水中的杂质CaCl2、MgCl2、Na2SO4可依次加入过量NaOH、 、Na2CO3溶液,分离出沉淀后,再加入适量盐酸,其作用是 。
19.开发利用清洁高效的新能源,减少CO2的排放,有利于实现“碳中和”。
(1)氢气是一种理想的新能源。氢气燃烧的化学方程式为 ;实验室用锌与稀硫酸反应制取氢气的化学方程式为 。
(2)某有机物与N2O4反应释放能量,可以作高能能源。该有机物18g与一定质量的N2O4恰好完全反应,可以生成26.4g CO2、21.6g H2O和25.2g N2,实验得其相对分子质量为60,则该有机物的化学式为 。
(1)氢气是一种理想的新能源。氢气燃烧的化学方程式为 ;实验室用锌与稀硫酸反应制取氢气的化学方程式为 。
(2)某有机物与N2O4反应释放能量,可以作高能能源。该有机物18g与一定质量的N2O4恰好完全反应,可以生成26.4g CO2、21.6g H2O和25.2g N2,实验得其相对分子质量为60,则该有机物的化学式为 。
20.A、B、C、D、E均含同一种金属元素,它们之间的转化关系如图所示(“→”表示反应可一步实现,部分物质和反应条件略去)。已知:A为氧化物,其中金属元素显+3价,且其质量分数为70%;B为单质;E为难溶性碱;A→B是工业制取B的主要原理。
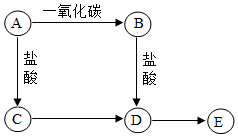
(1)A的化学式为 ;
(2)D→E的化学方程式为 ;
(3)C与B可发生化合反应生成D,该反应的化学方程式为 。

(1)A的化学式为 ;
(2)D→E的化学方程式为 ;
(3)C与B可发生化合反应生成D,该反应的化学方程式为 。
21.请从分子的角度解释下列生产、生活中的现象。
(1)湿衣服在太阳下晾晒比在阴凉处干得更快。
(2)加压时,3000L氧气可装入容积为20L的钢瓶中。
(1)湿衣服在太阳下晾晒比在阴凉处干得更快。
(2)加压时,3000L氧气可装入容积为20L的钢瓶中。
22.某化学小组用如图所示的装置进行探究实验。
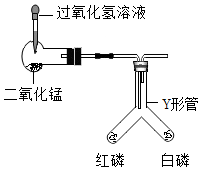
(1)请写出滴加过氧化氢溶液时发生反应的化学方程式。
(2)用80℃的水加热Y形管,白磷燃烧而红磷不燃烧,说明燃烧需要什么条件?

(1)请写出滴加过氧化氢溶液时发生反应的化学方程式。
(2)用80℃的水加热Y形管,白磷燃烧而红磷不燃烧,说明燃烧需要什么条件?
23.实验室选用下列仪器配制50g质量分数为6%的氯化钠溶液。
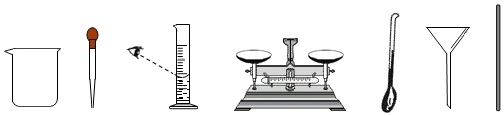
(1)所需氯化钠固体的质量为 g。
(2)完成该实验,如图中有一种仪器不必用到,请写出该仪器的名称 。
(3)若其他操作正确,量取水时俯视量筒读数,对结果会造成什么影响? 。

(1)所需氯化钠固体的质量为 g。
(2)完成该实验,如图中有一种仪器不必用到,请写出该仪器的名称 。
(3)若其他操作正确,量取水时俯视量筒读数,对结果会造成什么影响? 。
24.从废旧手机的某些部件中可以回收银和铜,其操作流程如图所示。

(1)请写出步骤Ⅰ中发生反应的化学方程式。(写出一个即可)
(2)步骤Ⅱ中,加入硝酸银溶液的作用是什么?
(3)步骤Ⅲ中,若溶液乙的质量大于溶液甲,确定M后写出发生反应的化学方程式。

(1)请写出步骤Ⅰ中发生反应的化学方程式。(写出一个即可)
(2)步骤Ⅱ中,加入硝酸银溶液的作用是什么?
(3)步骤Ⅲ中,若溶液乙的质量大于溶液甲,确定M后写出发生反应的化学方程式。
25.碳及其化合物与生产、生活密切相关,是化学学习和研究的重要内容。
(1)请将如图虚线框内碳原子的结构示意图补画完整。

(2)金刚石和石墨都属于碳单质,它们的化学性质相似,物理性质却有很大差异,其原因是 (填字母代号)。
a.构成它们的原子大小不同
b.两种物质由不同种原子构成
c.构成它们的原子数目不同
d.两种物质里碳原子的排列方式不同
(3)某同学用如图装置(铁架台等略去)制取纯净、干燥的CO2并探究CO2的性质。
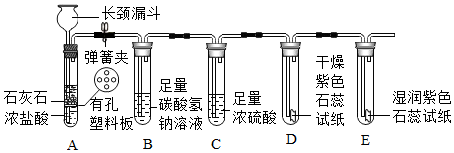
①A装置能控制反应的发生和停止,请简述使反应停止的原理 。
②B装置中可能发生反应的化学方程式为 。
③证明CO2与水发生了反应的实验现象为 。
(4)制取CO2后的酸性废液需处理后再排放,除去CO2常采用碱液吸收法。
①检验某废液是否呈酸性,可选用的一种试剂(或用品)是 。
②为探究足量NaOH溶液吸收CO2后溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入足量Ca(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH。请指出该方案中的错误并加以改正 。
(5)某温室大棚需用到440L CO2(按标准状况计算,CO2密度为1.964g/L),用足量盐酸与含CaCO3 80%的石灰石反应制取,需要这种石灰石的质量是多少?
(1)请将如图虚线框内碳原子的结构示意图补画完整。

(2)金刚石和石墨都属于碳单质,它们的化学性质相似,物理性质却有很大差异,其原因是 (填字母代号)。
a.构成它们的原子大小不同
b.两种物质由不同种原子构成
c.构成它们的原子数目不同
d.两种物质里碳原子的排列方式不同
(3)某同学用如图装置(铁架台等略去)制取纯净、干燥的CO2并探究CO2的性质。

①A装置能控制反应的发生和停止,请简述使反应停止的原理 。
②B装置中可能发生反应的化学方程式为 。
③证明CO2与水发生了反应的实验现象为 。
(4)制取CO2后的酸性废液需处理后再排放,除去CO2常采用碱液吸收法。
①检验某废液是否呈酸性,可选用的一种试剂(或用品)是 。
②为探究足量NaOH溶液吸收CO2后溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入足量Ca(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH。请指出该方案中的错误并加以改正 。
(5)某温室大棚需用到440L CO2(按标准状况计算,CO2密度为1.964g/L),用足量盐酸与含CaCO3 80%的石灰石反应制取,需要这种石灰石的质量是多少?
查看全部题目