下载高清试卷
【2020-2021学年湖南省岳阳市城区九年级(上)期末化学试卷】-第1页
试卷格式:2020-2021学年湖南省岳阳市城区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2021年、湖南试卷、岳阳市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷
扫码查看解析
试卷题目
1.下列选项不属于化学这门学科研究范畴的是( )
- A. 物质的组成与结构
- B. 物质的性质与变化
- C. 物质的运动状态
- D. 物质的用途与制取
2.下列实验室中的交流,属于化学变化的是( )
- A. 试管:“同学们不爱惜,我被摔碎了”
- B. 铁架台:“好难受!我在潮湿的空中生锈了”
- C. 酒精灯:“帽子呢?我的燃料越来越少了”
- D. 干冰:“我一到云层,云朵就化雨了”
3.规范化学实验操作是实验成败的关键。下列实验操作正确的是( )
- A.
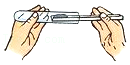 取用“铜绿”
取用“铜绿” - B.
 滴加稀盐酸
滴加稀盐酸 - C.
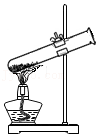 加热“铜绿”
加热“铜绿” - D.
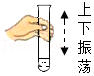 洗涤试管
洗涤试管
4.下列有关空气中各种成分的用途说法错误的是( )
- A. 稀有气体通电会发出有色的光
- B. 氮气可用作保护气
- C. 氧气可用作火箭发射的燃料
- D. 二氧化碳是植物进行光合作用必需的物质
5.下列有关实验现象说法正确的是( )
- A. 红磷在空气中燃烧产生大量白色烟雾
- B. 铁丝在氧气中燃烧,火星四射,生成一种红色固体
- C. 将10mL酒精和10mL水混合,并充分振荡,液体体积小于20mL
- D. 电解水时正极附近产生气体与负极附近产生气体的体积比为2:1
6.对于下列几种化学符号,有关说法正确的是( )
①H ②Fe2+③Ne ④CO2⑤Fe3+
①H ②Fe2+③Ne ④CO2⑤Fe3+
- A. 能表示一个分子的是①④
- B. 能表示物质化学式的是③④
- C. ②⑤的质子数相同,化学性质也相同
- D. ④中的数字“2”表示2个氧原子
7.在日常生活中,如果将深颜色的衣服和浅颜色的衣服浸泡在一起,可能会使浅色衣服染上深颜色,这其中的主要原因是由于深色染料中的( )
- A. 分子本身发生了改变
- B. 分子是在不断地运动的
- C. 分子间的间隔增大
- D. 分子在化学变化中可分
8.下列关于燃烧和灭火的说法中,不正确的是( )
- A. 液化石油气泄漏,立即关闭阀门并开窗通风
- B. 逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面逃离
- C. 将木柴架空燃烧,目的是增大可燃物与氧气的接触面积,促进燃烧
- D. 实验室酒精着火,用湿布覆盖在上面,是为了降低可燃物的着火点
9.构建化学基本观念是学好化学的基础,下列对化学基本观念的认识错误的是( )
- A. 元素观:一氧化碳、二氧化碳都是由碳元素和氧元素组成的
- B. 微粒观:金刚石、石墨、C60物理性质差异很大的原因是碳原子的排列方式不同
- C. 转化观:氧化汞在一定条件下可生成金属汞
- D. 守恒观:化学反应前后分子的种类不发生变化
10.如图所示,某同学为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水,发现石灰水没有变化。据此,你认为该同学应该( )
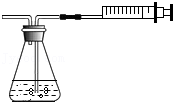

- A. 得出空气中没有二氧化碳的结论
- B. 得出空气中含有少量二氧化碳的结论
- C. 继续用大针筒向澄清石灰水压入空气
- D. 撤去大针筒,用嘴向澄清石灰水吹气
11.分类是研究物质的常用方法。如图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )
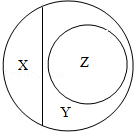

- A. 红磷
- B. 干冰
- C. 氯酸钾
- D. 食盐水
12.洁厕灵、84消毒液是生活中两种常见的清洁、消毒用品,混合使用时会发生如图所示的化学反应。下列说法正确的是( )


- A. 该反应的生成物均由分子构成
- B. 有毒气体是Cl2
- C. 反应前后元素化合价不变
- D. 洁厕灵、84消毒液能混合使用
13.对比实验是实验探究的重要方法。下列对比实验设计不能实现相应实验目的的是( )
- A.
 鉴别H2与CH4
鉴别H2与CH4 - B.
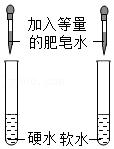 区分硬水与软水
区分硬水与软水 - C.
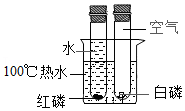 探究空气是燃烧的必要条件
探究空气是燃烧的必要条件 - D.
 探究分子的运动
探究分子的运动
14.容器内有甲、乙、丙、丁四种物质,一定条件下发生了化学反应,各物质的质量变化如图。下列说法正确的是( )
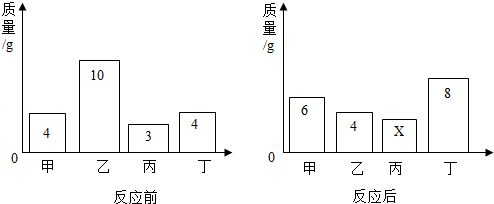

- A. 该反应中,乙、丁的质量比为3:2
- B. X=0
- C. 甲和丁的相对分子质量之比为1:2
- D. 该反应为化合反应
15.下列图象能正确反映对应变化关系的是( )
- A.
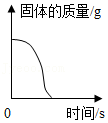 表示加热KClO3(含少量MnO2)固体制取氧气时剩余固体的质量
表示加热KClO3(含少量MnO2)固体制取氧气时剩余固体的质量 - B.
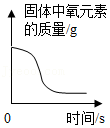 表示加热KClO3(含少量MnO2)固体制取氧气时固体中氧元素的质量
表示加热KClO3(含少量MnO2)固体制取氧气时固体中氧元素的质量 - C.
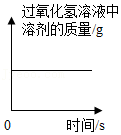 表示双氧水(含少量MnO2)分解时溶剂的质量
表示双氧水(含少量MnO2)分解时溶剂的质量 - D.
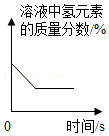 表示双氧水(含少量MnO2)分解时氢元素的质量分数
表示双氧水(含少量MnO2)分解时氢元素的质量分数
16.(1)编写元素周期表的科学家是19世纪俄国科学家 (填写字母序号)。
A.拉瓦锡
B.门捷列夫
C.波尔
(2)如图是钠、氯元素在元素周期表中的信息及有关粒子的结构示意图。请回答下列问题:
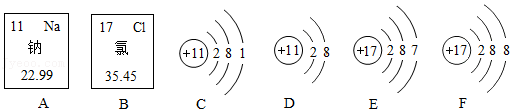
①从图A中可获取的信息正确的是 (填写字母序号)。
A.该元素属于非金属元素
B.该元素的相对原子质量为11
C.该元素的原子结构示意图可由C表示
D.该元素原子在化学反应中易得到电子
②D、F形成化合物的化学式是 。
③与元素的化学性质关系最密切的是 (填写字母序号)。
A.原子的核外电子数
B.元素的相对原子质量
C.原子的最外层电子数
A.拉瓦锡
B.门捷列夫
C.波尔
(2)如图是钠、氯元素在元素周期表中的信息及有关粒子的结构示意图。请回答下列问题:

①从图A中可获取的信息正确的是 (填写字母序号)。
A.该元素属于非金属元素
B.该元素的相对原子质量为11
C.该元素的原子结构示意图可由C表示
D.该元素原子在化学反应中易得到电子
②D、F形成化合物的化学式是 。
③与元素的化学性质关系最密切的是 (填写字母序号)。
A.原子的核外电子数
B.元素的相对原子质量
C.原子的最外层电子数
17.能源利用和环境保护是人类共同关注的问题。
(1)下列说法中正确的是 (填写所有正确答案的字母序号)。
A.煤、石油和天然气都属于可再生能源
B.从环境保护角度考虑,最理想的燃料是汽油
C.可燃冰将成为未来新能源,其中主要含有甲烷水合物
D.若在开采可燃冰时引起甲烷泄漏,可能会引起温室效应
(2)煤燃烧时排放出的 、二氧化氮等污染物,可能导致酸雨。
(3)为减缓温室效应,我们可采取的措施为 。
(4)天然气可以在一定条件下合成甲醇。
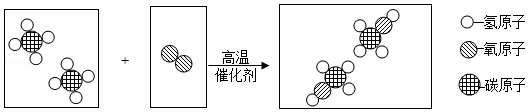
该反应的化学方程式为 ,基本反应类型为 。
(1)下列说法中正确的是 (填写所有正确答案的字母序号)。
A.煤、石油和天然气都属于可再生能源
B.从环境保护角度考虑,最理想的燃料是汽油
C.可燃冰将成为未来新能源,其中主要含有甲烷水合物
D.若在开采可燃冰时引起甲烷泄漏,可能会引起温室效应
(2)煤燃烧时排放出的 、二氧化氮等污染物,可能导致酸雨。
(3)为减缓温室效应,我们可采取的措施为 。
(4)天然气可以在一定条件下合成甲醇。

该反应的化学方程式为 ,基本反应类型为 。
18.新冠疫情期间小宇量体温时不小心将体温表滑落摔碎,地上散落许多银珠,应该怎样清理?经网络搜寻,获得以下有关水银的资料,依据相关信息回答问题:
打碎温度计,水银掉落在地面马上会形成很多小汞珠。由于汞的沸点低,容易挥发,汞撒落后会蒸发,很快会污染室内空气,还可能会通过呼吸道吸收进入血液,使人发生中毒。汞可与硫反应生成不易溶于水的无毒物质硫化汞(HgS),红色的硫化汞称为丹砂。
(1)我国晋代炼丹家、医学家葛洪所著《抱扑子》一书中记载有“丹砂烧之成水银,积变又还成丹砂”。这句话中所发生的变化是 (填“物理”或“化学”)变化。
(2)硫化汞化学式为HgS,其中Hg的化合价为 。
(3)小宇关掉屋内所有热源,开窗透风,这一处置方法说明汞具有的物理性质是 。
(4)小宇戴上手套用小勺把水银收集到盛有水的玻璃瓶中,又向不易收集的细小水银珠上撒硫颗粒降低危害,他的依据是 (用化学方程式表示)。
打碎温度计,水银掉落在地面马上会形成很多小汞珠。由于汞的沸点低,容易挥发,汞撒落后会蒸发,很快会污染室内空气,还可能会通过呼吸道吸收进入血液,使人发生中毒。汞可与硫反应生成不易溶于水的无毒物质硫化汞(HgS),红色的硫化汞称为丹砂。
(1)我国晋代炼丹家、医学家葛洪所著《抱扑子》一书中记载有“丹砂烧之成水银,积变又还成丹砂”。这句话中所发生的变化是 (填“物理”或“化学”)变化。
(2)硫化汞化学式为HgS,其中Hg的化合价为 。
(3)小宇关掉屋内所有热源,开窗透风,这一处置方法说明汞具有的物理性质是 。
(4)小宇戴上手套用小勺把水银收集到盛有水的玻璃瓶中,又向不易收集的细小水银珠上撒硫颗粒降低危害,他的依据是 (用化学方程式表示)。
19.某兴趣小组在实验室模拟水厂将洞庭湖的水净化成自来水,并最终制成蒸馏水,其实验流程如图1所示:
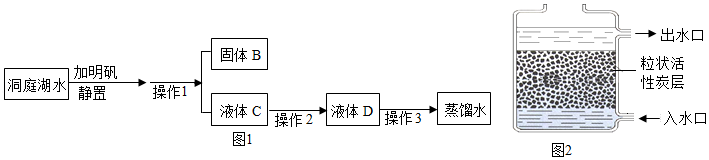
请回答下列问题:
(1)向水样中加入明矾,经静置及 (填写操作1的名称)可除去不溶杂质。
(2)利用图2所示的装置进行操作2,此操作中粒状活性炭可达到的目的有 (填写字母序号)。
A.杀菌消毒
B.除去臭味
C.将硬水软化
(3)通过操作3可以得到净化程度较高的蒸馏水,操作3的名称是 。
(4)水是生命之源,每个人都要爱护,请你提出一条保护水资源的合理化建议: 。

请回答下列问题:
(1)向水样中加入明矾,经静置及 (填写操作1的名称)可除去不溶杂质。
(2)利用图2所示的装置进行操作2,此操作中粒状活性炭可达到的目的有 (填写字母序号)。
A.杀菌消毒
B.除去臭味
C.将硬水软化
(3)通过操作3可以得到净化程度较高的蒸馏水,操作3的名称是 。
(4)水是生命之源,每个人都要爱护,请你提出一条保护水资源的合理化建议: 。
20.如图是实验室制取气体的一些装置,据图请回答问题。
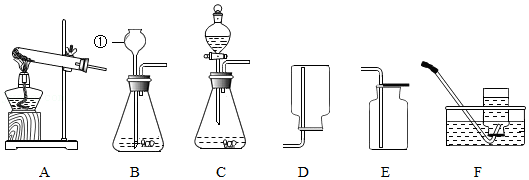
(1)写出标号①仪器的名称 。
(2)用高锰酸钾制取和收集较纯净的氧气,选择的装置组合是 (填字母)。
(3)实验室用B装置制取二氧化碳的化学方程式为 ;与B相比,C作为制取二氧化碳的发生装置,优点是 。

(1)写出标号①仪器的名称 。
(2)用高锰酸钾制取和收集较纯净的氧气,选择的装置组合是 (填字母)。
(3)实验室用B装置制取二氧化碳的化学方程式为 ;与B相比,C作为制取二氧化碳的发生装置,优点是 。
21.化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
(1)请写出镁条燃烧的化学方程式 ;实验现象是 。
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是: ;
(3)小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】①氮化镁中氮元素的化合价是 ;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是: 。
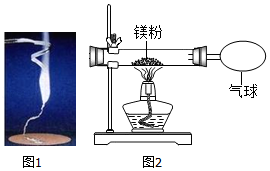
(1)请写出镁条燃烧的化学方程式 ;实验现象是 。
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是: ;
(3)小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
【反思与交流】①氮化镁中氮元素的化合价是 ;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是: 。

22.某化学课外活动小组为了测定石灰石中碳酸钙的含量,把20g石灰石固体样品进行高温煅烧,发生反应的化学方程式为CaCO3
CaO+CO2↑。完全反应后,冷却、称量,残留固体质量15.6g。计算:(假设杂质不参加反应)
(1)固体质量减少了 g;
(2)石灰石样品中碳酸钙的质量分数是多少?(要求写出计算过程)
| 高温 |
(1)固体质量减少了 g;
(2)石灰石样品中碳酸钙的质量分数是多少?(要求写出计算过程)
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解