下载高清试卷
【2021年北京市中考化学试卷】-第1页
试卷格式:2021年北京市中考化学试卷.PDF
试卷热词:最新试卷、2021年、北京试卷、化学试卷、九年级试卷、中考试卷、初中试卷

扫码查看解析
试卷题目
1.空气中体积分数约为78%的气体是( )
- A. 氮气
- B. 氧气
- C. 二氧化碳
- D. 稀有气体
2.下列物质在O2中燃烧,火星四射,生成黑色固体的是( )
- A. 木炭
- B. 镁条
- C. 蜡烛
- D. 铁丝
3.将CO2通入下列液体中,能产生白色沉淀的是( )
- A. 水
- B. 稀硫酸
- C. 食盐水
- D. 澄清石灰水
4.下列物质能用作氮肥的是( )
- A. KCl
- B. K2CO3
- C. NH4Cl
- D. Ca3(PO4)2
5.下列物质属于氧化物的是( )
- A. O2
- B. CaO
- C. H2SO4
- D. KMnO4
6.下列仪器不能加热的是( )
- A. 烧杯
- B. 试管
- C. 量筒
- D. 燃烧匙
7.下列物质含有氢分子的是( )
- A. Ca(OH)2
- B. H2CO3
- C. H2O2
- D. H2
8.下列物质能除铁锈的是( )
- A. 盐酸
- B. 植物油
- C. NaOH溶液
- D. 食盐水
9.电解水实验如图,下列说法不正确的是( )
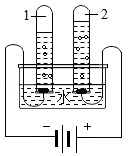

- A. 试管1中得到H2
- B. 水由H2、O2构成
- C. 水发生了分解反应
- D. 水由氢、氧元素组成
10.下列元素中,人体摄入过低会引起贫血的是( )
- A. 铁
- B. 碘
- C. 锌
- D. 钙
11.如图所示的图标表示( )


- A. 禁止吸烟
- B. 禁止燃放鞭炮
- C. 禁止带火种
- D. 禁止堆放易燃物
12.下列H2的性质中,属于化学性质的是( )
- A. 难溶于水
- B. 无色气体
- C. 能燃烧
- D. 熔点低
13.如表列出了某果仁的营养分,其中含量最高的营养素是( )
| 项目 | 每100g |
| 蛋白质 | 13.2g |
| 脂肪 | 70.1g |
| 碳水化合物 | 13.0g |
| 钠 | 216mg |
- A. 蛋白质
- B. 糖类
- C. 油脂
- D. 无机盐
14.一些物质的pH范围如下,其中呈碱性的是( )
- A. 柠檬汁(2﹣3)
- B. 酱油(4﹣5)
- C. 西瓜汁(5﹣6)
- D. 洗发水(8﹣9)
15.下列物质属于有机化合物的是( )
- A. NaCl
- B. NaOH
- C. HCl
- D. CH4
16.我国冶炼金属的历史悠久。回答16~18问题。
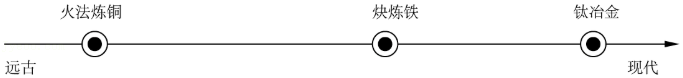
远古时期火法炼铜的原料是孔雀石【主要成分为Cu2(OH)2CO3】,组成Cu2(OH)2CO3的元素种类为( )

远古时期火法炼铜的原料是孔雀石【主要成分为Cu2(OH)2CO3】,组成Cu2(OH)2CO3的元素种类为( )
- A. 3种
- B. 4种
- C. 5种
- D. 6种
17.块炼铁以炭和铁矿石为原料,反应之一为Fe2O3+3CO
2Fe+3CO2,该反应中,化合价降低的元素是( )
| 高温 |
- A. 铁元素
- B. 碳元素
- C. 氧元素
- D. 铁元素和碳元素
18.冶炼钛(Ti)的反应之一为2Mg+TiCl4
Ti+2MgCl2,该反应属于( )
| 一定条件 |
- A. 化合反应
- B. 分解反应
- C. 置换反应
- D. 复分解反应
19.制作景泰蓝的釉料中常含钴元素。钴元素在元素周期表中的信息如图。回答19~20问题。
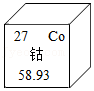
下列有关钴元素的说法不正确的是( )

下列有关钴元素的说法不正确的是( )
- A. 原子序数是27
- B. 属于非金属元素
- C. 元素符号是Co
- D. 相对原子质量为58.93
20.钴原子的核外电子数是( )


- A. 27
- B. 32
- C. 59
- D. 86
21.用MgCl2溶液喷洒路面可融雪、防尘。20℃时,按下表数据配制溶液,回答21~23题。
(已知:20℃时,MgCl2的溶解度为54.6g)
所得溶液中,溶质与溶剂的质量比为1:2的是( )
| 序号 | ① | ② | ③ | ④ |
| MgCl2的质量/g | 30 | 40 | 50 | 60 |
| 水的质量/g | 100 | 100 | 100 | 100 |
(已知:20℃时,MgCl2的溶解度为54.6g)
所得溶液中,溶质与溶剂的质量比为1:2的是( )
- A. ①
- B. ②
- C. ③
- D. ④
22.
(已知:20℃时,MgCl2的溶解度为54.6g)
①中溶质的质量分数约为( )
| 序号 | ① | ② | ③ | ④ |
| MgCl2的质量/g | 30 | 40 | 50 | 60 |
| 水的质量/g | 100 | 100 | 100 | 100 |
(已知:20℃时,MgCl2的溶解度为54.6g)
①中溶质的质量分数约为( )
- A. 23%
- B. 30%
- C. 35%
- D. 43%
23.
(已知:20℃时,MgCl2的溶解度为54.6g)
所得溶液中,属于饱和溶液的是( )
| 序号 | ① | ② | ③ | ④ |
| MgCl2的质量/g | 30 | 40 | 50 | 60 |
| 水的质量/g | 100 | 100 | 100 | 100 |
(已知:20℃时,MgCl2的溶解度为54.6g)
所得溶液中,属于饱和溶液的是( )
- A. ①
- B. ②
- C. ③
- D. ④
24.用如图装置可验证空气中O2的含量。下列现象能表明O2含量的是( )


- A. 集气瓶中产生大量白烟
- B. 红磷燃烧一段时间后熄灭
- C. 烧杯中的水倒吸进入集气瓶
- D. 集气瓶中水面最终上升至1处
25.实验研究铁锈蚀影响因素,记录如下。下列分析不正确的是( )
| 实验装置 | 序号 | 其他试剂 | 200s时O2的含量 |
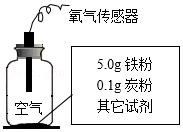 | ① | 干燥剂 | 21% |
| ② | 10滴水 | 15% | |
| ③ | 10滴水和1.0g食盐 | 8% |
- A. ②③中O2含量减少表明铁已锈蚀
- B. ①②证明水对铁锈蚀有影响
- C. ②③证明食盐能加快铁锈蚀
- D. ①②③证明炭粉对铁锈蚀有影响
26.从A或B两题中任选一个作答,若两题均作答,按A计分。
| A.NaHCO3的用途之一是 。 | B.NaHCO3的俗名是 。 |
27.我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。
(1)现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、 和天然气。
(2)下列燃料在O2中燃烧时,不会产生CO2的是 (填序号)。
A.天然气
B.氢气
C.肼(N2H4)
(3)捕集、利用和封存CO2是实现碳中和的一种途径。矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,该反应的化学方程式为 。
(1)现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、 和天然气。
(2)下列燃料在O2中燃烧时,不会产生CO2的是 (填序号)。
A.天然气
B.氢气
C.肼(N2H4)
(3)捕集、利用和封存CO2是实现碳中和的一种途径。矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,该反应的化学方程式为 。
28.H2O2溶液常用作的消毒剂。
(1)H2O2溶液属于 (填“混合物”或“纯净物”)。
(2)H2O2不稳定,易分解。H2O2分解的化学方程式为 。
(3)用3%的H2O2溶液对不同金属进行腐蚀性实验,结果如下:
下列金属制品用该溶液浸泡消毒时,最易被腐蚀的是 (填序号)。
A.不锈钢锅
B.铝盆
C.铜火锅
(1)H2O2溶液属于 (填“混合物”或“纯净物”)。
(2)H2O2不稳定,易分解。H2O2分解的化学方程式为 。
(3)用3%的H2O2溶液对不同金属进行腐蚀性实验,结果如下:
| 金属种类 | 不锈钢片 | 铝片 | 铜片 |
| 腐蚀速度(mg/h) | 0.001 | 0.010 | 0.404 |
下列金属制品用该溶液浸泡消毒时,最易被腐蚀的是 (填序号)。
A.不锈钢锅
B.铝盆
C.铜火锅
29.阅读下面科普短文。
碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过液态碳和晶形碳三大类,如图1。

石墨是制铅笔芯的原料之一,在16世纪被发现后,曾被误认为是含铅的物质。直到18世纪,化学家将石墨与KNO3共熔后产生CO2,才确定了它是含碳的物质。
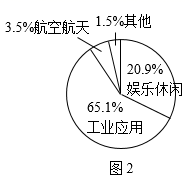
碳纤维既有碳材料的固有本质特性,又有纺织纤维的柔软可加工性,综合性能优异。目前,我国已形成碳纤维生产、碳纤维复合材料成型,应用等产业链,碳纤维复合材料应用领域分布如图2。
科学界不断研发出新型碳材料,碳气凝胶就是其中一种。碳气凝胶具有优良的吸附性能,在环境净化中发挥重要作用。我国科研人员在不同温度下制备了三种碳气凝胶样品,比较其对CO2的选择性吸附性能。他们在不同压强下测定了上述样品对混合气体中CO2吸附的选择性值,实验结果如图3。图中选择性值越高,表明碳气凝胶对CO2的选择性吸附性能越好。

随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。
依据文章内容回答下列问题:
(1)金刚石属于 (填序号)。
A.无定形碳
B.过渡态碳
C.晶形碳
(2)石墨与KNO3共熔,能发生如下反应,配平该反应的化学方程式:5C+4KNO3
K2O+ N2↑+ CO2↑。
(3)由图2可知,我国碳纤维复合材料应用占比最高的领域是 。
(4)判断下列说法是否正确(填“对”或“错”)。
①石墨是一种含铅的物质 。
②碳材料其有广阔的应用和发展前景 。
(5)对比图3中三条曲线,得到的实验结论是 。
碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过液态碳和晶形碳三大类,如图1。

石墨是制铅笔芯的原料之一,在16世纪被发现后,曾被误认为是含铅的物质。直到18世纪,化学家将石墨与KNO3共熔后产生CO2,才确定了它是含碳的物质。
碳纤维既有碳材料的固有本质特性,又有纺织纤维的柔软可加工性,综合性能优异。目前,我国已形成碳纤维生产、碳纤维复合材料成型,应用等产业链,碳纤维复合材料应用领域分布如图2。
科学界不断研发出新型碳材料,碳气凝胶就是其中一种。碳气凝胶具有优良的吸附性能,在环境净化中发挥重要作用。我国科研人员在不同温度下制备了三种碳气凝胶样品,比较其对CO2的选择性吸附性能。他们在不同压强下测定了上述样品对混合气体中CO2吸附的选择性值,实验结果如图3。图中选择性值越高,表明碳气凝胶对CO2的选择性吸附性能越好。


随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。
依据文章内容回答下列问题:
(1)金刚石属于 (填序号)。
A.无定形碳
B.过渡态碳
C.晶形碳
(2)石墨与KNO3共熔,能发生如下反应,配平该反应的化学方程式:5C+4KNO3
| 高温 |
(3)由图2可知,我国碳纤维复合材料应用占比最高的领域是 。
(4)判断下列说法是否正确(填“对”或“错”)。
①石墨是一种含铅的物质 。
②碳材料其有广阔的应用和发展前景 。
(5)对比图3中三条曲线,得到的实验结论是 。
30.真空热还原法生产钙的主要转化过程如图:
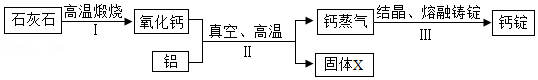
(1)石灰石的主要成分是 。
(2)Ⅱ中反应有两种产物,固体X一定含有氧元素和铝元素,从元素守恒角度说明理由 。
(3)装置Ⅲ中发生的是 (填“物理”或“化学”)变化。

(1)石灰石的主要成分是 。
(2)Ⅱ中反应有两种产物,固体X一定含有氧元素和铝元素,从元素守恒角度说明理由 。
(3)装置Ⅲ中发生的是 (填“物理”或“化学”)变化。
31.高纯CO可用于半导体领域某些芯片的刻蚀,利用甲酸(HCOOH)制取高纯CO的主要流程如图:
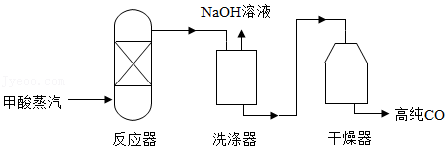
(1)甲酸中碳元素和氧元素的质量比为 。
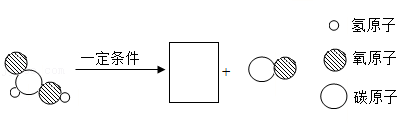
(2)反应塔中甲酸分解的微现示意图如图,在方框中补全另一种产物的微粒图示 。
(3)反应塔中发生副反应产生微量CO2。洗涤器中加入NaOH溶液的目的是中和未反应的甲酸蒸气,并除去CO2,NaOH与CO2反应的化学方程式为 。

(1)甲酸中碳元素和氧元素的质量比为 。
(2)反应塔中甲酸分解的微现示意图如图,在方框中补全另一种产物的微粒图示 。

(3)反应塔中发生副反应产生微量CO2。洗涤器中加入NaOH溶液的目的是中和未反应的甲酸蒸气,并除去CO2,NaOH与CO2反应的化学方程式为 。
32.根据如图回答问题。

(1)仪器a的名称是 。
(2)加热KMnO4制取O2的化学方程式为 。
(3)收集O2的装置是 (填序号)。
(4)将带火星的木条放在瓶口,若观察到 ,说明瓶中已充满O2。

(1)仪器a的名称是 。
(2)加热KMnO4制取O2的化学方程式为 。
(3)收集O2的装置是 (填序号)。
(4)将带火星的木条放在瓶口,若观察到 ,说明瓶中已充满O2。
33.用如图实验(夹持仪器已略去)研究铁的性质。
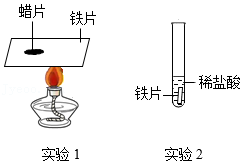
(1)实验1,观察到蜡片熔化,说明铁具有的性质是 。
(2)实验2,反应的化学方程式为 。

(1)实验1,观察到蜡片熔化,说明铁具有的性质是 。
(2)实验2,反应的化学方程式为 。
34.如图是去除粗盐中难溶性杂质实验的三步操作。
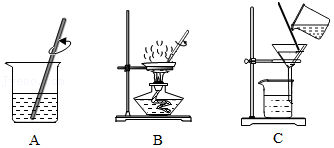
(1)三步操作的正确顺序是 (填序号)。
(2)B中,用玻璃棒不断搅拌的目的是 。

(1)三步操作的正确顺序是 (填序号)。
(2)B中,用玻璃棒不断搅拌的目的是 。
35.用如图装置研究酸、碱的性质。
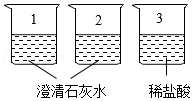
(1)向1中滴加Na2CO3溶液,观察到的现象是 。
(2)向2、3中滴加无色酚酞溶液,溶液变红的是 (填序号);再向3中滴加NaOH溶液,NaOH与盐酸反应的化学方程式为 。

(1)向1中滴加Na2CO3溶液,观察到的现象是 。
(2)向2、3中滴加无色酚酞溶液,溶液变红的是 (填序号);再向3中滴加NaOH溶液,NaOH与盐酸反应的化学方程式为 。
36.用如图实验验证可燃物燃烧的条件,已知:白磷的着火点为40℃。
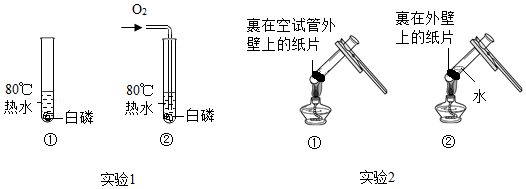
(1)实验1,能验证可燃物燃烧需要O2的现象是 。
(2)实验2,①中纸片燃烧,②中纸片未燃烧,②中纸片未燃烧的原因是 。

(1)实验1,能验证可燃物燃烧需要O2的现象是 。
(2)实验2,①中纸片燃烧,②中纸片未燃烧,②中纸片未燃烧的原因是 。
37.用如图实验验证CO2的性质。

(1)实验室制取CO2的化学方程式为 。
(2)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是 。
(3)观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是 。

(1)实验室制取CO2的化学方程式为 。
(2)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是 。
(3)观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是 。
38.硬水加热时易产生水垢,很多工业用水需要对硬水进行软化处理。小组同学利用1.5%的肥皂水比较水的硬度。
【查阅资料】硬水含较多可溶性钙、镁化合物;软水不含或含较少可溶性钙,镁化合物。
Ⅰ、探究水的硬度、肥皂水的用量与产生泡沫量的关系
【进行实验】向蒸馏水中加入CaCl2和MgCl2的混合溶液,配制两种不问硬度的硬水。
用蒸馏水和两种硬水完成三组实验,记录如下:
【解释与结论】
(1)对比②和⑧可知,肥皂水能区分软水和硬水,依据的现象是 。
(2)设计第2组实验时,为控制水的硬度相同,⑤中x应为 。
(3)第2组实验的目的是 。
(4)由上述三组实验得到的结论是 。
Ⅱ、比较不同水样的硬度
【进行实验】用四种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
【解释与结论】
(5)硬度最大的水样是 。
(6)由上述实验可知,能将自来水硬度降低的方法有 。
(7)继续实验,发现山泉水的硬度大于自来水的硬度,其实验方案为 。
【查阅资料】硬水含较多可溶性钙、镁化合物;软水不含或含较少可溶性钙,镁化合物。
Ⅰ、探究水的硬度、肥皂水的用量与产生泡沫量的关系
【进行实验】向蒸馏水中加入CaCl2和MgCl2的混合溶液,配制两种不问硬度的硬水。
用蒸馏水和两种硬水完成三组实验,记录如下:
| 组别 | 第1组 | 第2组 | 第3组 | ||||||
| 实验操作 |  | 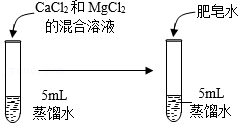 | |||||||
| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 混合溶液用量/滴 | 0 | 0 | 0 | 1 | x | 1 | 2 | 2 | 2 |
| 肥皂水用量/滴 | 5 | 10 | 20 | 5 | 10 | 20 | 5 | 10 | 20 |
| 产生泡沫量 | 少 | 多 | 很多 | 无 | 少 | 多 | 无 | 无 | 少 |
【解释与结论】
(1)对比②和⑧可知,肥皂水能区分软水和硬水,依据的现象是 。
(2)设计第2组实验时,为控制水的硬度相同,⑤中x应为 。
(3)第2组实验的目的是 。
(4)由上述三组实验得到的结论是 。
Ⅱ、比较不同水样的硬度
【进行实验】用四种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
| 实验操作 | 水样 | 肥皂水用量/滴 |
 | 市售纯净水 | 2 |
| 煮沸后的自来水 | 6 | |
| 自来水 | 9 | |
| 湖水 | 14 |
【解释与结论】
(5)硬度最大的水样是 。
(6)由上述实验可知,能将自来水硬度降低的方法有 。
(7)继续实验,发现山泉水的硬度大于自来水的硬度,其实验方案为 。
39.《天工开物》中记载了金属的冶炼技术。在锌的冶炼方法中,主要反应之一为ZnO+CO
Zn+CO2。若制得65kgZn,计算参加反应的ZnO的质量(写出计算过程及结果)。
| 高温 |
查看全部题目