下载高清试卷
【2020-2021学年广东省东莞市九年级(上)期中化学试卷】-第1页
试卷格式:2020-2021学年广东省东莞市九年级(上)期中化学试卷.PDF
试卷热词:最新试卷、2021年、广东试卷、东莞市试卷、化学试卷、九年级上学期试卷、期中试卷、初中试卷

扫码查看解析
试卷题目
1.下列实验操作涉及化学变化的是( )
- A.
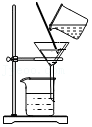 过滤
过滤 - B.
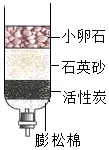 利用简易净水器净化水
利用简易净水器净化水 - C.
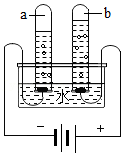 电解水
电解水 - D.
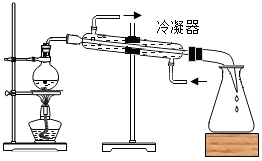 水的蒸馏
水的蒸馏
2.下列物质排放到空气中,不会造成大气污染的是( )
- A. 二氧化碳
- B. 二氧化氮
- C. 一氧化碳
- D. 可吸入颗粒物
3.市场上有“葡萄糖酸锌”、“高钙牛奶”、“绿色碘盐”等商品,这里的“锌、钙、碘”指的是( )
- A. 元素
- B. 分子
- C. 单质
- D. 原子
4.下列实验操作不正确的是( )
- A.
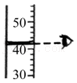 读取液体体积
读取液体体积 - B.
 称量NaOH固体
称量NaOH固体 - C.
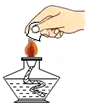 熄灭酒精灯
熄灭酒精灯 - D.
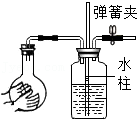 检查装置的气密性
检查装置的气密性
5.依据如图有关信息判断,下列说法正确的是( )


- A. 在元素周期表中,镁元素与氟元素属于同一周期
- B. 镁离子与氟离子核外电子数相等
- C. 镁原子与氟原子形成的化合物的化学式为Mg2F
- D. 氟原子的核内有9个中子
6.关于金刚石、石墨、C60的叙述,正确的是( )
- A. 都属于碳单质
- B. 都由碳原子构成
- C. 都具有导电性
- D. 完全燃烧产物不同
7.“宏观解识与微观探析”是化学学科核心素养之”,下列微观解释正确的是( )
| 选项 | 客观事实 | 微观解释 |
| A | 水银温度计测温度 | 原子的质量和体积都很小 |
| B | Ca、Ca2+化学性质不同 | 微粒中的质子数不同 |
| C | 氧气(O2)和臭氧(O3)性质不同 | 构成物质的分子不同 |
| D | 碘受热升华 | 分子的体积变大 |
- A. A
- B. B
- C. C
- D. D
8.下列关于实验的说法正确的是( )
- A. 用氯酸钾分解制氧气收集完成后,先停止加热后撤离导管
- B. 收集一试管氢气,点燃后听到尖锐爆鸣声,说明氢气不纯
- C. 将表面光滑的铁钉放在硫酸铜溶液中,铁钉表面生成银白色固体
- D. 实验室不能用稀硫酸和大理石反应制取二氧化碳,因为它们不发生反应
9.下列描述与化学用语对应正确的是( )
- A. 2个铁离子:Fe3+
- B. 2个O原子:O2
- C. Na2SeO4中Se的化合价:Na2O4
+6 Se - D. 氧化铝:AlO
10.根据化学方程式不能获得的信息是( )
- A. 该反应中的反应物和生成物
- B. 各反应物和生成物的质量比
- C. 反应发生所需的条件
- D. 化学反应的快慢
11.碳可以与浓硫酸在加热的条件下发生如下反应:C+2H2SO4(浓)
CO2↑+2X↑+2H2O其中X的化学式为( )
| △ |
- A. O2
- B. SO3
- C. SO2
- D. H2S
12.密闭容器中有一定质量的甲、乙、丙、丁四种物质,在一定条件下反应一段时间后,测得各物质的质量如表所示:有关说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 8.0 | 16.8 | 3.4 | 2.0 |
| 反应后的质量/g | 11.4 | 10 | x | 2.0 |
- A. 该反应中甲与乙的质量比是57:50
- B. x=3.4
- C. 该反应属于分解反应
- D. 丁一定是催化剂
13.按如图进行实验,下列分析或结论正确的是( )
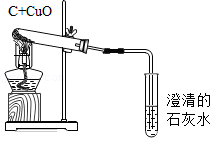

- A. 澄清石灰水的作用只是为了隔绝空气
- B. 实验结束应立即倒出试管内的粉末
- C. 本实验主要体现了木炭的可燃性
- D. 为提高火焰温度,应在酒精灯火焰周围罩一个网罩
14.一氧化碳是一种无色、无味但有剧毒的气体,其密度与空气很接近,难溶于水。现要收集一瓶一氧化碳气体,可采用的方法是( )
- A. 向下排空气法
- B. 向上排空气法
- C. 排水法
- D. 向上排空气法或排水法
15.下列四个图象中能正确反应其对应实验操作的是( )
- A.
 将水通电电解一段时间
将水通电电解一段时间 - B.
 碳在含有氧气的密闭容器中燃烧,容器中碳元素的质量变化
碳在含有氧气的密闭容器中燃烧,容器中碳元素的质量变化 - C.
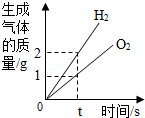
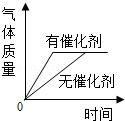 用两份相同的过氧化氢溶液分别制取氧气,生成气体质量的变化
用两份相同的过氧化氢溶液分别制取氧气,生成气体质量的变化 - D.
 加热一定量的高锰酸钾,生成的氧气质量的变化
加热一定量的高锰酸钾,生成的氧气质量的变化
16.生活处处离不开水。
(1)下列做法有利于节约水资源或减少水体污染的是 。
①农业和园林浇灌改为喷灌、滴灌
②工业废水直接排入江河中
③生活污水集中处理和排放
④为提高农作物产量,大量使用化肥农药
(2)一种净水机可以将水厂原水直接净化为饮用水,其中处理流程如图所示:

a.①中超滤膜可起到过滤不溶性杂质的作用,实验室过滤所需要的仪器有带铁圈的铁架台、烧杯、漏斗(含滤纸)和 (填仪器名称),该仪器在过滤过程中的作用是 。
b.步骤②对应的作用是 ;步骤③对应的作用是 。
c.家中可以用 鉴别硬水和软水,实验室可通过 的方法降低水的硬度。
(3)下列实验能证明水是由氢元素和氧元素组成的是 (填字母序号)。
A. 氢气在氧气中燃烧
B. 水的蒸发
C. 水的电解
D. 水的净化
请写出以上A选项涉及到的化学方程式 。
(1)下列做法有利于节约水资源或减少水体污染的是 。
①农业和园林浇灌改为喷灌、滴灌
②工业废水直接排入江河中
③生活污水集中处理和排放
④为提高农作物产量,大量使用化肥农药
(2)一种净水机可以将水厂原水直接净化为饮用水,其中处理流程如图所示:

a.①中超滤膜可起到过滤不溶性杂质的作用,实验室过滤所需要的仪器有带铁圈的铁架台、烧杯、漏斗(含滤纸)和 (填仪器名称),该仪器在过滤过程中的作用是 。
b.步骤②对应的作用是 ;步骤③对应的作用是 。
c.家中可以用 鉴别硬水和软水,实验室可通过 的方法降低水的硬度。
(3)下列实验能证明水是由氢元素和氧元素组成的是 (填字母序号)。
A. 氢气在氧气中燃烧
B. 水的蒸发
C. 水的电解
D. 水的净化
请写出以上A选项涉及到的化学方程式 。
17.(1)高纯硅是制造手机CPU芯片的材料,工业上利用四氯化硅(SiCl4)为原料制高纯硅,此工艺流程简化示意图如图:

图中属于化合物的是 (填“甲”、“乙”、“丙“或“丁”),该反应的化学方程式为 ,请标出SiCl4中硅元素的化合价 。
(2)食醋的主要成分是乙酸,乙酸的分子结构模型如图所示,其 代表碳原子,〇代表氢原子,
代表碳原子,〇代表氢原子, 代表氧原子。
代表氧原子。
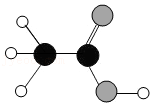
①乙酸中碳、氢、氧元素的最简质量比为 ,其中氧元素在地壳中含量排第 位。
②60g乙酸中碳元素的质量为 g。

图中属于化合物的是 (填“甲”、“乙”、“丙“或“丁”),该反应的化学方程式为 ,请标出SiCl4中硅元素的化合价 。
(2)食醋的主要成分是乙酸,乙酸的分子结构模型如图所示,其
 代表碳原子,〇代表氢原子,
代表碳原子,〇代表氢原子, 代表氧原子。
代表氧原子。
①乙酸中碳、氢、氧元素的最简质量比为 ,其中氧元素在地壳中含量排第 位。
②60g乙酸中碳元素的质量为 g。
18.如图所示是实验室制取气体的一些装置,据图回答有关问。(提示:以下所选装置均填装置的字母序号)

(1)写出指定仪器的名称:② 。
(2)装置C中试管口略向下倾斜的原因是 ;在不添加任何仪器的情况下,利用C装置制取氧气,涉及到的化学方程式为: 。
(3)若需收集(2)中所得气体供铁丝在氧气中燃烧的实验使用,应选用气体收集装置中的 装置,理由是 ;利用该装置 (填“能/不能”)用于收集CO2气体。
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放出大量的热使发生装置炸裂。你认为图中最适合制取乙炔气体的发生装置是 ;用该装置也能制取二氧化碳,请写出实验室制取二氧化碳的化学方程式 。

(1)写出指定仪器的名称:② 。
(2)装置C中试管口略向下倾斜的原因是 ;在不添加任何仪器的情况下,利用C装置制取氧气,涉及到的化学方程式为: 。
(3)若需收集(2)中所得气体供铁丝在氧气中燃烧的实验使用,应选用气体收集装置中的 装置,理由是 ;利用该装置 (填“能/不能”)用于收集CO2气体。
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放出大量的热使发生装置炸裂。你认为图中最适合制取乙炔气体的发生装置是 ;用该装置也能制取二氧化碳,请写出实验室制取二氧化碳的化学方程式 。
19.为验证质量守恒定律,某学习小组做了镇条在空气中燃烧的实验(图1)。
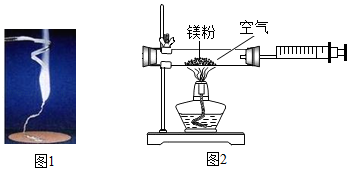
(1)请写出镁条燃烧的化学方程式 。
(2)镁条完全燃烧后,称量发现石棉网上的燃烧产物的质量反而比反应前镁条的质量小,其主导原因可能有 。
A.燃烧增加了氧元素的质量
B.有部分白烟逸散在空气中
C.部分产物粘在坩埚钳上
故探究化学反应前后物质的总质量关系时,如反应过程中有气体参加或生成,需要在 容器中进行。
(3)小红按图2装置改进实验,验证了质量守恒定律,最终得出结论是:参加化学反应的各物质的质量总和 (填“<”、“>”或“=”)反应后生成的各物质的质量总和。
(微观解释)从微观角度分析,在化学反应前后一定不变的是 (选填序号)。
①原子种类
②分子种类
③原子数目
④分子质量
⑤分子数目
⑥原子质量
(4)小红结束图2实验后发现产物中还有一些黄色固体。
【查阅资料】①氧化镁为白色固体;②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【提出问题】黄色固体是什么呢?
【做出猜想】黄色固体为Mg3N2
【实验探究】
【反思与交流】
①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,请给出合理的解释 。
②如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,结合注射器的刻度显示,最终测得氧气体积分数
(填“大于”、“小于”或“等于”)。注射器在本实验中还具备的优点为: 。

(1)请写出镁条燃烧的化学方程式 。
(2)镁条完全燃烧后,称量发现石棉网上的燃烧产物的质量反而比反应前镁条的质量小,其主导原因可能有 。
A.燃烧增加了氧元素的质量
B.有部分白烟逸散在空气中
C.部分产物粘在坩埚钳上
故探究化学反应前后物质的总质量关系时,如反应过程中有气体参加或生成,需要在 容器中进行。
(3)小红按图2装置改进实验,验证了质量守恒定律,最终得出结论是:参加化学反应的各物质的质量总和 (填“<”、“>”或“=”)反应后生成的各物质的质量总和。
(微观解释)从微观角度分析,在化学反应前后一定不变的是 (选填序号)。
①原子种类
②分子种类
③原子数目
④分子质量
⑤分子数目
⑥原子质量
(4)小红结束图2实验后发现产物中还有一些黄色固体。
【查阅资料】①氧化镁为白色固体;②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【提出问题】黄色固体是什么呢?
【做出猜想】黄色固体为Mg3N2
【实验探究】
| 实验操作 | 实验现象及结论 |
如图,取燃烧产物中的黄色固体于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B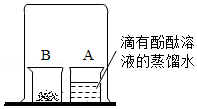 | 现象: 结论:燃烧产物中含Mg3N2 |
【反思与交流】
①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,请给出合理的解释 。
②如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,结合注射器的刻度显示,最终测得氧气体积分数
| 1 |
| 5 |
20.空气是一种宝贵资源,如利用制得的氢气(H2)和空气中分离出的氮气(N2)合成氨气(NH3),下列是合成氨的工艺流程图1:

(1)上述流程中可以回收利用的物质是 和 。
(2)将沸点不同的气体分离开,常采用液化分离法。如,控制温度在﹣183℃时,可将空气中氮气与氧气分离,这一过程是 变化(填“物理”或“化学”)。根据下表中物质的沸点判断,要将产物NH3与N2、H2分离开来,温度应该控制在 以下。
(3)用“ ”分别表示N2、H2、NH3,观察下列微观图:
”分别表示N2、H2、NH3,观察下列微观图:

①请写出该反应的化学方程式及反应类型 ,反应类型 。
②请补充完整图2反应前后的微观示意图。

(1)上述流程中可以回收利用的物质是 和 。
(2)将沸点不同的气体分离开,常采用液化分离法。如,控制温度在﹣183℃时,可将空气中氮气与氧气分离,这一过程是 变化(填“物理”或“化学”)。根据下表中物质的沸点判断,要将产物NH3与N2、H2分离开来,温度应该控制在 以下。
| 物质 | H2 | N2 | NH3 |
| 沸点 | ﹣252℃ | ﹣195.8℃ | ﹣33.35℃ |
(3)用“
 ”分别表示N2、H2、NH3,观察下列微观图:
”分别表示N2、H2、NH3,观察下列微观图:
①请写出该反应的化学方程式及反应类型 ,反应类型 。
②请补充完整图2反应前后的微观示意图。
21.工业上,在高温的条件下煅烧石灰石(主要成分是CaCO3)可生成氧化钙和二氧化碳。现利用该反应制取得到5.6t的氧化钙,请计算参与反应的CaCO3的质量是多少?
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解