下载高清试卷
【2020年四川省攀枝花市西区中考化学一模试卷】-第1页
试卷格式:2020年四川省攀枝花市西区中考化学一模试卷.PDF
试卷热词:最新试卷、2020年、四川试卷、攀枝花市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.下列物质不属于合金的是( )
- A. 生铁
- B. 硬铝
- C. 黄铜
- D. C60
2.把少量的下列物质分别放入水中,充分搅拌,能形成溶液的是( )
- A. 面粉
- B. 蔗糖
- C. 花生油
- D. 泥土
3.下列应用只涉及物质的物理性质的是( )
- A. 煤用作燃料
- B. 铜用作电线
- C. 盐酸用于除铁锈
- D. 生石灰用作干燥剂
4.下列洗涤或除污过程应用乳化原理的是( )
- A. 用钢丝球刷除抄菜锅上的污垢
- B. 用酒精除去衣服上的碘
- C. 用汽油除去衣服上的油污
- D. 用洗洁精洗去餐具上的油脂
5.下列有关实验现象的描述正确的是( )
- A. 将少量高锰酸钾放入装有汽油的试管中,振荡,得到紫红色溶液
- B. 硫在空气中燃烧发出淡蓝色火焰,生成二氧化硫气体
- C. 打开盛有浓盐酸的试剂瓶瓶盖,瓶口上方出现白雾
- D. 硝酸铵固体溶于水放出大量的热
6.明代宋应星所著的《天工开物》中记载的炼锡方法,用化学方程式表示为:SnO2+2C
Sn+2CO↑,该反应属于( )
| 高温 |
- A. 置换反应
- B. 分解反应
- C. 化合反应
- D. 复分解反应
7.实验室用氯化钠配制50g质量分数为6%的氯化钠溶液。下列说法中不正确的是( )
- A. 所需氯化钠的质量为3g
- B. 氯化钠放在托盘天平的左盘称量
- C. 俯视量筒读数会使所配溶液偏稀
- D. 所需玻璃仪器有烧杯、玻璃棒、量筒等
8.“操作千万条,安全第一条”。下列做法符合安全要求的是( )
- A. 用NaOH溶液清洗手上的油污
- B. CO还原Fe2O3时先通CO再加热
- C. 熄灭酒精灯时用嘴吹灭
- D. 稀释浓硫酸时将水注入浓硫酸中
9.为了探究铁制品锈蚀的条件,小明用普通铁钉、纯铁钉同时进行如图的四组实验,一段时间后只在实验Ⅰ中观察到了红褐色锈斑,其他均无明显变化。下列说法错误的是( )


- A. Ⅰ和Ⅱ说明铁制品锈蚀需要O2
- B. Ⅰ和Ⅲ说明铁制品锈蚀需要H2O
- C. Ⅰ和Ⅳ说明H2O和O2同时存在,铁制品不一定发生锈蚀
- D. Ⅲ和Ⅳ说明铁制品锈蚀跟铁制品内部结构有关
10.如图所示的实验装置,试管中盛有水,向试管中加入下列哪种物质,U型管中的液面无明显发生变化( )
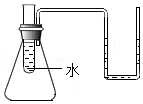

- A. 食盐固体
- B. 浓硫酸
- C. 氢氧化钠固体
- D. 硝酸铵固体
11.现有甲、乙、丙三种金属,甲在常温下就能与氧气反应,乙、丙在常温下几乎不与氧气反应:如果将乙、丙分别放入硫酸铜溶液中,过一会儿,在丙的表面有红色固体析出,而乙表面没有变化,则甲、乙、丙三种金属的活动性由弱到强的顺序是( )
- A. 甲 乙 丙
- B. 乙 甲 丙
- C. 乙 丙 甲
- D. 甲 丙 乙
12.如图为一氧化碳还原氧化铁实验。下列说法中正确的是( )
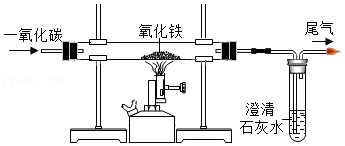

- A. 开始时应先预热玻璃管,后通入一氧化碳
- B. 实验中玻璃管里粉末由黑色逐渐变成红棕色
- C. 参加反应的氧化铁和一氧化碳质量比为40:7
- D. 将尾气点燃或收集,可防止一氧化碳污染空气
13.下列物质的性质与用途均正确并相对应的是( )
| 性质 | 用途 | |
| A | 铝在空气中与氧气反应生成致密氧化膜 | 铝合金用于制作卫生间的置物架 |
| B | 钨的导电性好 | 钨用于制作灯泡里的灯丝 |
| C | CO2水溶液显酸性 | CO2用作大棚蔬菜的气体肥料 |
| D | 浓硫酸具有脱水性 | 浓硫酸用作干燥剂 |
- A. A
- B. B
- C. C
- D. D
14.下列有关物质混合后的现象描述中,正确的是( )
- A. CO通过灼热的氧化铁粉末,粉末由红色变为黑色
- B. 把生石灰加入到饱和的熟石灰溶液中,固体完全溶解
- C. 铜丝浸入硫酸锌溶液中,溶液由无色变为蓝色,铜丝表面有一层银白色物质析出
- D. 将过量的NaOH溶液逐渐滴入混有石蕊的稀盐酸中,溶液颜色由红色逐渐变为无色
15.将一定量的铁粉加入到含有Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是( )
- A. 滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2
- B. 滤渣中一定不含Fe,滤液中一定含有Fe(NO3)2和Cu(NO3)2
- C. 滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3
- D. 滤渣中一定含有Ag和Cu,滤液中可能含有Cu(NO3)2和AgNO3
16.现有9.3g NaOH与Na2CO3的固体混合物,测得其中钠元素与碳元素的质量比为23:3.在室温下,将该混合物与50g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为57.1g,则原固体混合物中含有钠元素的质量为下列的( )
- A. 1.15g
- B. 2.3g
- C. 4.6g
- D. 6.9g
17.请用化学用语填空:
(1)铝合金中铝的元素符号是 ,生石灰的化学式是 。
(2)酸有一些相似的化学性质,是因为不同的酸溶液中都含有 。
(3)某种硫单质的一个分子中含有6个硫原子,这种硫单质的化学式是 。
(4)碘酒溶液中的溶剂是 。
(1)铝合金中铝的元素符号是 ,生石灰的化学式是 。
(2)酸有一些相似的化学性质,是因为不同的酸溶液中都含有 。
(3)某种硫单质的一个分子中含有6个硫原子,这种硫单质的化学式是 。
(4)碘酒溶液中的溶剂是 。
18.化学与人们的生产生活密切相关。
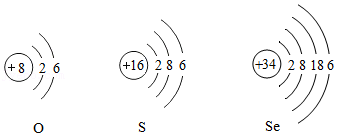
(1)硒元素能增强人体免疫力,延缓衰老,山药等食物中常含硒元素。硒(Se)在氧气中燃烧生成二氧化硒。回答下列问题:
①硒原子的核电荷数为 。
②硒、氧、硫元素的化学性质相似,是因为它们原子的 相同。
③写出硒在氧气中燃烧反应的化学方程式 。
(2)黄铁矿(主要成分是FeS2),是生产H2SO4的重要原料。利用黄铁矿生产H2SO4的第一步反应为:4FeS2+11O2═2Fe2O3+8X,所得产物Fe2O3是冶炼铁的重要原料。
①已知FeS2中Fe的化合价为+2,则S的化合价为 ;
②X的化学式是 ;
③写出高炉中Fe2O3转化成铁的化学方程式 。

(1)硒元素能增强人体免疫力,延缓衰老,山药等食物中常含硒元素。硒(Se)在氧气中燃烧生成二氧化硒。回答下列问题:
①硒原子的核电荷数为 。
②硒、氧、硫元素的化学性质相似,是因为它们原子的 相同。
③写出硒在氧气中燃烧反应的化学方程式 。
(2)黄铁矿(主要成分是FeS2),是生产H2SO4的重要原料。利用黄铁矿生产H2SO4的第一步反应为:4FeS2+11O2═2Fe2O3+8X,所得产物Fe2O3是冶炼铁的重要原料。
①已知FeS2中Fe的化合价为+2,则S的化合价为 ;
②X的化学式是 ;
③写出高炉中Fe2O3转化成铁的化学方程式 。
19.用粗木棍在涂有蜡的锌板上写“明”“和”两个字,露出下面的锌板。向“明”字上滴加CuSO4溶液,向“和”字上滴加盐酸。

(1)“明”字上的现象是 。
(2)“和”字上产生气泡,用化学方程式解释: 。

(1)“明”字上的现象是 。
(2)“和”字上产生气泡,用化学方程式解释: 。
20.如图是a、b、c三种物质的溶解度曲线,据图回答:
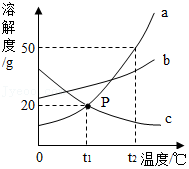
(1)t2℃时a、b、c三种物质的溶解度按由大到小的顺序是 。
(2)t2℃时30g a物质加入到50g水中不断搅拌,形成溶液的溶质质量分数为 。
(3)t1℃时,a的饱和溶液中溶质与溶剂的质量比为 。
(4)t2℃时,相同质量的a、b饱和溶液中,a的饱和溶液中所含水的质量 b的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)。
(5)从a与b的混合溶液中提取出固体a可采用的方法为 。

(1)t2℃时a、b、c三种物质的溶解度按由大到小的顺序是 。
(2)t2℃时30g a物质加入到50g水中不断搅拌,形成溶液的溶质质量分数为 。
(3)t1℃时,a的饱和溶液中溶质与溶剂的质量比为 。
(4)t2℃时,相同质量的a、b饱和溶液中,a的饱和溶液中所含水的质量 b的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)。
(5)从a与b的混合溶液中提取出固体a可采用的方法为 。
21.回答下列与金属有关的问题:
(1)生铁和纯铁,硬度较大的是 。
(2)铝制品其有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的 (用名称或化学式填空)薄膜。
(3)铁锅用来炒菜,主要是利用铁的 性(填“导热”或“导电”)。
(4)图为洁净铁钉的有关实验。
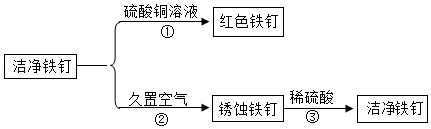
①中铁与硫酸铜反应的化学方程式为 。
②中铁钉锈蚀主要是铁与空气中的氧气和 发生化学反应。
③中铁锈与稀硫酸反应的化学方程式为 。
(1)生铁和纯铁,硬度较大的是 。
(2)铝制品其有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的 (用名称或化学式填空)薄膜。
(3)铁锅用来炒菜,主要是利用铁的 性(填“导热”或“导电”)。
(4)图为洁净铁钉的有关实验。

①中铁与硫酸铜反应的化学方程式为 。
②中铁钉锈蚀主要是铁与空气中的氧气和 发生化学反应。
③中铁锈与稀硫酸反应的化学方程式为 。
22.用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。

(1)先推入的溶液是 。
(2)bc段压强不变,原因是 。
(3)cd段压强变大,用化学方程式解释: 。

(1)先推入的溶液是 。
(2)bc段压强不变,原因是 。
(3)cd段压强变大,用化学方程式解释: 。
23.木炭还原氧化铜实验后的混合粉末中含有铜、氧化铜、木炭粉,某化学实验小组设计回收铜的方案如下:
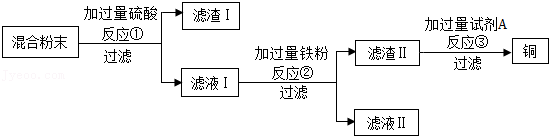
(1)过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(2)反应①的化学方程式为 。
(3)滤液Ⅱ中的溶质为 。
(4)试剂A最好选用下列 溶液(填序号)。
①H2SO4②CuSO4③MgSO4
(5)为了完善实验方案,可对滤渣Ⅰ中的 进行回收。

(1)过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(2)反应①的化学方程式为 。
(3)滤液Ⅱ中的溶质为 。
(4)试剂A最好选用下列 溶液(填序号)。
①H2SO4②CuSO4③MgSO4
(5)为了完善实验方案,可对滤渣Ⅰ中的 进行回收。
24.为了探究碱的化学性质,同学们进行了如图所示的实验。

(1)【实验操作】
夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中。锥形瓶中发生反应的化学方程式为 。反应一段时间后,打开弹簧夹,观察到的现象为 ,锥形瓶底部有白色沉淀生成。
【废液处理】
(2)将反应后锥形瓶内的物质全部倒入烧杯B中,然后滴入几滴无色酚酞溶液,充分混合后,烧杯内的液体为 色。
(3)再向烧杯中倒入一定量的稀盐酸,充分反应后,烧杯内得到无色澄清溶液,则该无色溶液中一定含有的溶质是 。请写出该烧杯内发生中和反应的化学方程式 (写一个)。
(4)最后烧杯内的无色溶液能否直接排放,请阐述你的观点并说明理由 。
【反思交流】上述实验活动验证了碱可以与某些物质发生化学反应。

(1)【实验操作】
夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中。锥形瓶中发生反应的化学方程式为 。反应一段时间后,打开弹簧夹,观察到的现象为 ,锥形瓶底部有白色沉淀生成。
【废液处理】
(2)将反应后锥形瓶内的物质全部倒入烧杯B中,然后滴入几滴无色酚酞溶液,充分混合后,烧杯内的液体为 色。
(3)再向烧杯中倒入一定量的稀盐酸,充分反应后,烧杯内得到无色澄清溶液,则该无色溶液中一定含有的溶质是 。请写出该烧杯内发生中和反应的化学方程式 (写一个)。
(4)最后烧杯内的无色溶液能否直接排放,请阐述你的观点并说明理由 。
【反思交流】上述实验活动验证了碱可以与某些物质发生化学反应。
25.我国钢铁产量多年居世界第一位,每年要进口大量的铁矿石,赤铁矿(主要成分是氧化铁)是其中的一种。
(1)氧化铁中铁元素的质量分数为 。
(2)1000t含氧化铁80%的赤铁矿石中,氧化铁的质量是 t,用这些赤铁矿石理论上可以炼出含杂质4%的生铁 t(计算结果保留整数)。
(1)氧化铁中铁元素的质量分数为 。
(2)1000t含氧化铁80%的赤铁矿石中,氧化铁的质量是 t,用这些赤铁矿石理论上可以炼出含杂质4%的生铁 t(计算结果保留整数)。
26.化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入100g稀硫酸,恰好完全反应后。测得烧杯内所有物质的总质量为109.8g。
请完成下列分析及计算:
(1)反应中共生成气体 g。
(2)计算合金中铜的质量分数。
请完成下列分析及计算:
(1)反应中共生成气体 g。
(2)计算合金中铜的质量分数。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解