下载高清试卷
【2021年湖南省郴州市中考化学二模试卷】-第1页
试卷格式:2021年湖南省郴州市中考化学二模试卷.PDF
试卷热词:最新试卷、2021年、湖南试卷、郴州市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.下列物质的用途与物质的物理性质有关的是( )
- A. 用硫酸除去金属表面的锈
- B. 用一氧化碳冶炼生铁
- C. 用氢气作高能燃料
- D. 用干冰进行人工降雨
2.规范的操作是实验成功的基本保证,下列实验操作规范的是( )
- A.
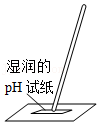 测溶液的pH
测溶液的pH - B.
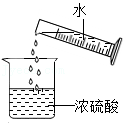 稀释浓硫酸
稀释浓硫酸 - C.
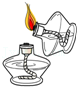 点燃酒精灯
点燃酒精灯 - D.
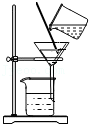 过滤
过滤
3.用分子的相关知识解释下列生活中的现象,其中不正确的是( )
- A. 一滴水中约含有1021个水分子,说明水分子的体积和质量都很小
- B. 警犬可以根据气味来追踪嫌犯,是因为不同种分子性质不同
- C. 变瘪的乒乓球在热水中会重新鼓起来,说明分子体积随温度升高而变大
- D. 湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快
4.吸烟有害健康,香烟的烟气中含有几百种对人体有害的物质,尼古丁是其中的一种,其化学式为C10H14N2,下列关于尼古丁的说法正确的是( )
- A. 尼古丁中氮元素质量分数最大
- B. 尼古丁是由10个碳原子、14个氢原子、2个氮原子构成
- C. 尼古丁由三种元素组成
- D. 尼古丁中含有氮分子
5.舌尖上的安全是各级政府义不容辞之责,下列做法中不会危及人体健康的是( )
- A. 食品腌制时大量使用亚硝酸盐
- B. 用碳酸钡代替硫酸钡做钡餐
- C. 烘焙蛋糕时添加少量小苏打
- D. 用硫酸铜溶液作自来水生产过程中的净水剂
6.3月22日是“世界水日”,下列关于水的说法正确的是( )
- A. 生活中用肥皂水鉴别硬水和软水,利用活性炭的吸附性来降低水的硬度
- B. 自来水厂净水的过程有静置沉淀、过滤、吸附、蒸馏
- C. 自然界水的循环过程中实现了水的自身净化
- D. 从电解水得到氢气和氧气,可知水是由氢原子和氧原子构成的
7.逻辑推理是化学学习的重要思维方法,下列说法合理的是( )
- A. 碱性溶液能使酚酞溶液变红,所以能使酚酞溶液变红的溶液一定显碱性
- B. 单质由同种元素组成,所以由同种元素组成的物质一定是单质
- C. 中和反应有盐和水生成,所以生成盐和水的反应一定是中和反应
- D. 一定温度下的不饱和溶液还能溶解该溶质,则一定温度下还能溶解某物质的溶液为不饱和溶液
8.如图是我们生活中一些物质的pH,下列说法中正确的是( )
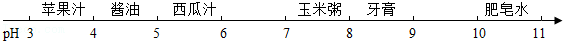
- A. 酱油呈碱性
- B. 皮肤被蚂蚁蜇入蚁酸,可用牙膏涂抹消肿
- C. 西瓜汁的酸性比苹果汁的酸性强
- D. 肥皂水能使无色酚酞试液变蓝
9.某兴趣小组利用如图装置对二氧化碳的性质进行探究,下列说法错误的是( )
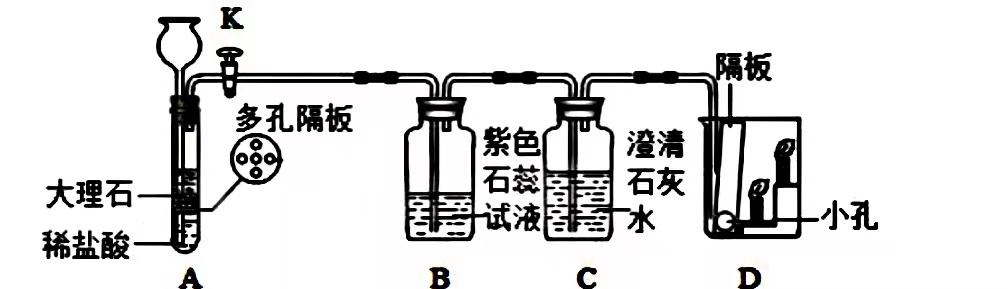

- A. B处现象说明二氧化碳能使紫色石蕊变红
- B. C处溶液变浑浊,是因为生成了不溶于水的碳酸钙
- C. D处的实验现象是下层蜡烛先熄灭,上层蜡烛后熄灭
- D. D处现象说明二氧化碳不可燃,不助燃,密度比空气大
10.下列有关说法正确的是( )
- A. 氧气能参与燃烧,它是高能燃料
- B. 铝丝与硝酸银溶液充分反应后,有银白色固体析出,溶液为无色,则溶液中一定无硝酸银
- C. 利用Fe、CuSO4溶液、Ag能够验证Fe、Cu、Ag金属活动性强弱顺序
- D. 催化剂在化学反应前后质量和性质都不变
11.下列中的物质、主要成分的化学式及用途三者对应关系不正确的是( )
- A. 石灰浆 CaO 可改良酸性土壤
- B. 食盐 NaCl 可作食品调味剂
- C. 大理石 CaCO3 可作建筑材料
- D. 小苏打 NaHCO3 可作发酵剂
12.下列物质是某食品配料中的主要成分,其中属于无机化合物的是( )
- A. 淀粉
- B. 食盐
- C. 食用油
- D. 白砂糖
13.在①氧化铁②金属锌③氢氧化钙④硝酸银溶液四种物质中跟稀盐酸都能发生反应,且反应中表现了H+的性质的组合是( )
- A. ①②③④
- B. ①②③
- C. ①③④
- D. ②③④
14.如图图象能正确反映对应变化关系的是( )
- A.
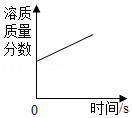 将浓硫酸露置在空气中一段时间
将浓硫酸露置在空气中一段时间 - B.
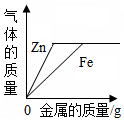 向等质量、等质量分数的稀硫酸中,分别加入足量的铁粉和锌粉
向等质量、等质量分数的稀硫酸中,分别加入足量的铁粉和锌粉 - C.
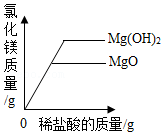 向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量
向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量 - D.
 向一定量盐酸和CaCl2的混合溶液中滴加入Na2CO3溶液
向一定量盐酸和CaCl2的混合溶液中滴加入Na2CO3溶液
15.现有Na2CO3和Na2SO4的混合物共12.4g,溶于水并加入过量的BaCl2溶液后,生成BaCO3和BaSO4沉淀共21.5g,则原混合物中含钠元素的质量为( )
- A. 2.3g
- B. 4.6g
- C. 6.9g
- D. 9.2g
16.请用化学用语填空:
(1)3个氧离子: 。
(2)保持水化学性质的最小粒子: 。
(3)标出二氧化碳中碳元素的化合价: 。
(4)生理盐水中的溶质: 。
(5)可用于填充探空气球和作焊接金属保护气的物质是: 。
(1)3个氧离子: 。
(2)保持水化学性质的最小粒子: 。
(3)标出二氧化碳中碳元素的化合价: 。
(4)生理盐水中的溶质: 。
(5)可用于填充探空气球和作焊接金属保护气的物质是: 。
17.化学与生产、生活、能源、环境息息相关。
(1)目前,人类使用的燃料大多来自化石燃料,如煤、 和天然气,它们都属于 (填“可再生”或“不可再生”)能源。
(2)化石燃料燃烧会产生SO2、CO2、NO2、CO、可吸入颗粒物等,其中没有计入空气质量日报中空气污染指数项目的是 。随着化石燃料的日益减少,开发和利用新能源成为越来越迫切的要求。请列举出一种新能源 。
(3)埋藏于海底,将来可能会代替化石燃料的新能源是 (填序号)。
A.氢气
B.汽油
C.乙醇
D.可燃冰
(4)要使甲烷燃烧,除了要与空气接触,还需要具备的条件是 ,其燃烧的化学方程式为 。
(1)目前,人类使用的燃料大多来自化石燃料,如煤、 和天然气,它们都属于 (填“可再生”或“不可再生”)能源。
(2)化石燃料燃烧会产生SO2、CO2、NO2、CO、可吸入颗粒物等,其中没有计入空气质量日报中空气污染指数项目的是 。随着化石燃料的日益减少,开发和利用新能源成为越来越迫切的要求。请列举出一种新能源 。
(3)埋藏于海底,将来可能会代替化石燃料的新能源是 (填序号)。
A.氢气
B.汽油
C.乙醇
D.可燃冰
(4)要使甲烷燃烧,除了要与空气接触,还需要具备的条件是 ,其燃烧的化学方程式为 。
18.硝酸钾和氯化钾两种物质的溶解度曲线见图1,这两种物质的溶解度见表。

请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质甲是指 (填写化学式)。
(2)60℃时,饱和KNO3溶液中混有少量KCl,应采用 的方法提纯KNO3固体。
(3)60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至t℃,析出晶体的质量关系为:KNO3 KCl(填写“>”、“=”、“<”或“无法确定”)。
(4)如图2所示,20℃时将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解向烧杯的水中加入某物质后试管内固体能完全溶解。则加入的物质可以是 (填序号)。
①冰块
②生石灰固体
③硝酸铵固体
④氢氧化钠固体
(5)在20℃下配制甲物质的溶液,溶质的质量分数最大值为 (计算结果保留整数)。

| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 |
| 甲溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| 乙溶解度/g | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质甲是指 (填写化学式)。
(2)60℃时,饱和KNO3溶液中混有少量KCl,应采用 的方法提纯KNO3固体。
(3)60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至t℃,析出晶体的质量关系为:KNO3 KCl(填写“>”、“=”、“<”或“无法确定”)。
(4)如图2所示,20℃时将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解向烧杯的水中加入某物质后试管内固体能完全溶解。则加入的物质可以是 (填序号)。
①冰块
②生石灰固体
③硝酸铵固体
④氢氧化钠固体
(5)在20℃下配制甲物质的溶液,溶质的质量分数最大值为 (计算结果保留整数)。
19.化学实验室中有失去标签的四瓶无色溶液,分别是稀盐酸、氢氧化钙溶液、碳酸钠溶液、酚酞试液中的某一种,现将其任意编号为A、B、C、D,然后两两组合进行实验,其中部分现象如表:
(1)酚酞试液是 (填编号);B的化学式是 。
(2)B与C发生的化学反应属于基本反应类型的 。
(3)写出D的用途所对应的任一个化学方程式 。
| 实验 | A+B | A+C | B+C | B+D |
| 现象 | 溶液变红 | 溶液变红 | 产生沉淀 | 产生气体 |
(1)酚酞试液是 (填编号);B的化学式是 。
(2)B与C发生的化学反应属于基本反应类型的 。
(3)写出D的用途所对应的任一个化学方程式 。
20.在“宏观一微观一符号”之间建立联系,是化学学科特有的思维方式。
(1)图1是四种粒子的结构示意图。
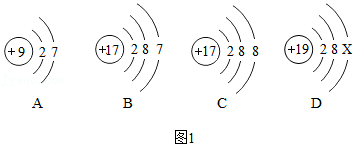
①D表示阳离子,则X= 。
②A、B、C、D中属于同种元素的粒子是 (选填序号)。
③A和B两种粒子具有相似的化学性质,是因为 。
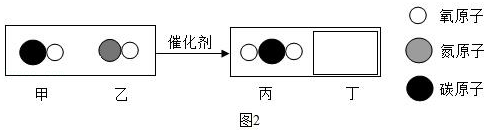
(2)汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图2所示。已知丁是一种单质,则该反应的化学方程式是 。
(1)图1是四种粒子的结构示意图。

①D表示阳离子,则X= 。
②A、B、C、D中属于同种元素的粒子是 (选填序号)。
③A和B两种粒子具有相似的化学性质,是因为 。
(2)汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图2所示。已知丁是一种单质,则该反应的化学方程式是 。

21.孔雀石的主要成分是CuCO3•Cu(OH)2及少量不溶性杂质(杂质不与酸反应),某同学按如图实验步骤制取了少量氧化铜。
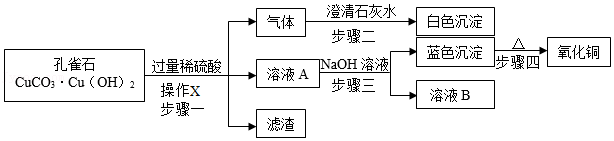
(1)步骤一中加入过量稀硫酸的目的是 ,产生的气体是 ,操作X用到的仪器有:铁架台、烧杯、玻璃棒、 。
(2)蓝色沉淀受热分解生成2种氧化物,写出该反应的化学方程式是 。

(1)步骤一中加入过量稀硫酸的目的是 ,产生的气体是 ,操作X用到的仪器有:铁架台、烧杯、玻璃棒、 。
(2)蓝色沉淀受热分解生成2种氧化物,写出该反应的化学方程式是 。
22.兴趣小组在探究铝和稀盐酸反应的实验时,小明无意中加入几滴硫酸铜溶液,发现铝片表面产生气泡速率明显加快,对此他产生了兴趣。
【提出问题】:硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
【设计并实验】:室温下,小明向5支洁净的试管中分别放入打磨后等质量、大小相同的铝片,再向试管中加水、3%硫酸铜溶液和10mL 10%稀盐酸,试剂用量如表所示,测量时间30秒,收集气体的体积。
(1)写出铝和稀盐酸反应的化学方程式 。
(2)定量收集氢气体积可用如图 (填写字母序号)装量。装量内的空气对测量结果 (选填“有影响”或“无影响”)。

【实验现象】:随着硫酸铜溶液体积的增加,产生氢气的速率先加快后明显减慢,且铝片表附着的红色物质逐渐增加。
【结论与解释】:
(3)随着硫酸铜溶液体积的增加反应速率明显变慢可能的原因是 。
(4)根据实验现象你认为硫酸铜溶液是不是此反应的催化剂 (选填“是”或“不是”)。
【实验拓展】
(5)已知一种金属加入比它弱的两种金属化合物溶液的混合液中,先置换出最弱的金属。实验后,小明又取一定量的铝片放入盛有Cu(NO3)2和AgNO3混合溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。同学们对滤液中成分(除水外)做了如下猜想:
猜想一:只有Al(NO3)3
猜想二:Cu(NO3)2和Al(NO3)3
猜想三:AgNO3、Cu(NO3)2和Al(NO3)3
小贝和小华分别设计了下列实验进行验证。
【提出问题】:硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
【设计并实验】:室温下,小明向5支洁净的试管中分别放入打磨后等质量、大小相同的铝片,再向试管中加水、3%硫酸铜溶液和10mL 10%稀盐酸,试剂用量如表所示,测量时间30秒,收集气体的体积。
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 3%硫酸铜溶液(mL) | 0 | 0.5 | 2.5 | 5 | 15 |
| 水(mL) | 20 | 19.5 | 17.5 | 15 | 5 |
| 收集的氢气体积(mL) | 12 | 15 | 18 | 24 | 10 |
(1)写出铝和稀盐酸反应的化学方程式 。
(2)定量收集氢气体积可用如图 (填写字母序号)装量。装量内的空气对测量结果 (选填“有影响”或“无影响”)。

【实验现象】:随着硫酸铜溶液体积的增加,产生氢气的速率先加快后明显减慢,且铝片表附着的红色物质逐渐增加。
【结论与解释】:
(3)随着硫酸铜溶液体积的增加反应速率明显变慢可能的原因是 。
(4)根据实验现象你认为硫酸铜溶液是不是此反应的催化剂 (选填“是”或“不是”)。
【实验拓展】
(5)已知一种金属加入比它弱的两种金属化合物溶液的混合液中,先置换出最弱的金属。实验后,小明又取一定量的铝片放入盛有Cu(NO3)2和AgNO3混合溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。同学们对滤液中成分(除水外)做了如下猜想:
猜想一:只有Al(NO3)3
猜想二:Cu(NO3)2和Al(NO3)3
猜想三:AgNO3、Cu(NO3)2和Al(NO3)3
小贝和小华分别设计了下列实验进行验证。
| 实验操作 | 现象 | 结论 |
| 小贝向所得滤渣中滴加稀盐酸 | 观察到有气泡产生 | 猜想 成立 |
| 小华将铜丝插入所得滤液中 | 猜想三成立 |
23.(1)某化学兴趣小组在进行酸碱中和反应的实验探究时,向盛有氢氧化钠溶液的烧杯中滴加稀盐酸后,发现忘记滴加无色酚酞溶液。该实验中反应的化学方程式 。
某同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液不变色。针对此溶液的成分,化学兴趣小组的同学进行了如下探究:
(2)【猜想与假设】:
猜想一:反应后氢氧化钠过量,溶液呈碱性;
猜想二:氢氧化钠与盐酸恰好完全中和,溶液呈中性;
猜想三: 。
(3)同学们经过讨论后觉得猜想一不正确,其理由是: 。
(4)【实验探究】:
【实验反思】:
(5)另有同学提出上述实验能证明NaOH溶液与稀盐酸恰好完全反应,其原因是 。
(6)除以上实验方案外,下列哪些物质单独使用,也能证明“NaOH溶液与稀盐酸是否恰好完全反应” (填序号)。
A.铜片
B.碳酸钠
C.氧化铜
D.紫色石蕊试液
(7)从微观的角度分析,该反应的实质是 。
某同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液不变色。针对此溶液的成分,化学兴趣小组的同学进行了如下探究:
(2)【猜想与假设】:
猜想一:反应后氢氧化钠过量,溶液呈碱性;
猜想二:氢氧化钠与盐酸恰好完全中和,溶液呈中性;
猜想三: 。
(3)同学们经过讨论后觉得猜想一不正确,其理由是: 。
(4)【实验探究】:
| 实验步骤 | 实验现象 | 结论 |
| 取一支试管,加入2小段镁条,再向试管中加入2mL上述溶液,观察现象。 | 若 | 稀盐酸过量 |
| 若没有明显现象 | NaOH溶液与稀盐酸恰好完全反应 |
【实验反思】:
(5)另有同学提出上述实验能证明NaOH溶液与稀盐酸恰好完全反应,其原因是 。
(6)除以上实验方案外,下列哪些物质单独使用,也能证明“NaOH溶液与稀盐酸是否恰好完全反应” (填序号)。
A.铜片
B.碳酸钠
C.氧化铜
D.紫色石蕊试液
(7)从微观的角度分析,该反应的实质是 。
24.N(NO2)3是科学家2011年发现的一种新型火箭燃料。计算:
(1)N(NO2)3中氮元素和氧元素的质量比为 (填最简比)。
(2)下列化合物中,氮元素质量分数最小的是 (填字母)。
A.N(NO2)3
B.N2O4
C.N2O5
(3)该材料304克中含氧元素的质量为 克。
(1)N(NO2)3中氮元素和氧元素的质量比为 (填最简比)。
(2)下列化合物中,氮元素质量分数最小的是 (填字母)。
A.N(NO2)3
B.N2O4
C.N2O5
(3)该材料304克中含氧元素的质量为 克。
25.取氯化钙和氯化钠的混合物10g,加入40g水使其完全溶解,再加入50g碳酸钠溶液恰好完全反应,过滤,得95g滤液(不考虑实验过程中质量损失),计算:
(1)所加碳酸钠溶液的溶质质量分数;
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%)。
(1)所加碳酸钠溶液的溶质质量分数;
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%)。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解