下载高清试卷
【2021年浙江省杭州市中考化学模拟试卷】-第1页
试卷格式:2021年浙江省杭州市中考化学模拟试卷.PDF
试卷热词:最新试卷、2021年、浙江试卷、杭州市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.2021年4月,我国科学家首次合成的铀﹣214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数是92。则铀﹣214原子的核外电子数为( )
- A. 92
- B. 122
- C. 214
- D. 306
2.如图表示治理汽车尾气所涉及反应的微观过程。下列说法不正确的是( )
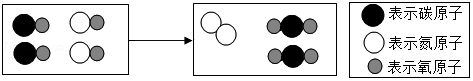

- A. 图中单质的化学式为N2
- B. 该反应使有害气体转化为无害气体
- C. 该反应属于置换反应
- D. 生成单质与化合物的质量比为7:22
3.分离、除杂、提纯和检验是化学实验的重要环节。下面实验设计能够达到目的的是( )
| 实验内容 | 实验设计 | |
| A | 除去H2中少量水蒸气、HCl | 先通过浓H2SO4,再通过NaOH溶液 |
| B | 分离CO2、CO混合物 | 先用NaOH溶液吸收掉CO2分离出CO,再向该NaOH溶液加足量稀硫酸“释放”出CO2 |
| C | 验证某溶液为稀盐酸 | 先测溶液的pH<7,再加入锌粒,观察 |
| D | 提纯部分变质的NaOH溶液 | 加入足量CaCl2溶液,充分反应后,过滤 |
- A. A
- B. B
- C. C
- D. D
4.KCl与KNO3在不同温度的溶解度数据如表。则下列说法不正确的是( )
| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
- A. 20℃时,KCl溶解度大于KNO3的溶解度
- B. 两物质溶解度相等的温度在20~30℃之间
- C. 40℃时,5g KCl加10g水可得到33.3%的溶液
- D. 50℃时,10g KNO3中加20g水,充分溶解,再降温到30℃,有KNO3固体析出
5.如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是( )

| 甲 | 乙 | |
| A. | 稀硫酸和铜片 | 水和硝酸铵固体 |
| B. | 水和氢氧化钠固体 | AgNO3溶液和稀盐酸 |
| C. | 双氧水和MnO2 | NaOH溶液和CO2 |
| D. | Na2CO3溶液和稀硫酸 | 水和浓硫酸 |

- A. A
- B. B
- C. C
- D. D
6.向一定质量的Mg(NO3)2和Cu(NO3)2混合溶液中加入a克锌粉和铁粉的混合物,充分反应后过滤,得到不饱和的滤液和滤渣,将滤渣洗涤、干燥后再称量,得到的固体质量仍为a克。下列分析合理的是( )
①滤渣中可能有铜
②向滤渣中加稀盐酸,可能有气泡产生
③滤液中一定有Mg(NO3)2、Zn(NO3)2和Fe(NO3)2,可能有Cu(NO3)2
④若忽略过滤操作中溶液损失,滤液中溶质的质量一定大于原混合溶液溶质的质量
①滤渣中可能有铜
②向滤渣中加稀盐酸,可能有气泡产生
③滤液中一定有Mg(NO3)2、Zn(NO3)2和Fe(NO3)2,可能有Cu(NO3)2
④若忽略过滤操作中溶液损失,滤液中溶质的质量一定大于原混合溶液溶质的质量
- A. ①②
- B. ①③
- C. ②③
- D. ②④
7.向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与
加入氢氧化钠溶液的质量关系如图所示。
(1)ob段发生反应的化学方程式为 。
(2)a点溶液中含有的溶质是 。
(3)加入的氢氧化钠的质量分数为 。
(4)d点时溶液呈 。(选填“酸性”、“碱性”或“中性”)

加入氢氧化钠溶液的质量关系如图所示。
(1)ob段发生反应的化学方程式为 。
(2)a点溶液中含有的溶质是 。
(3)加入的氢氧化钠的质量分数为 。
(4)d点时溶液呈 。(选填“酸性”、“碱性”或“中性”)

8.碘是人体必须的微量元素,海带因富含碘元素而成为补碘的常用食物之一。小李想设计实验验证海带中含有碘元素。他查阅了相关资料,得到以下信息:
①碘化钠(NaI)与氯化钠性质相似,两者的溶液都是盐溶液,碘化银为黄色难溶于水的固体。
②工业上将适量氯气通入无色碘化钠溶液就能置换出单质碘,溶液变为棕黄色。
③少量碘(I2)溶于水的溶液,能使淀粉溶液变蓝,碘的化合物不能使淀粉溶液变蓝。
④灼烧海带后残留的灰烬中含有可溶性碘化钠、氯化钠等化合物。
小李的实验步骤如下:
将海带灰用蒸馏水充分浸泡后过滤,得滤液;然后用以下3种方法,去检验海带灰中是否含有碘元素。
方法一:取滤液,通入适量氯气后与淀粉糊混合,观察是否变蓝。
方法二:取滤液,通入适量的氯气,观察溶液有无颜色变化。
方法三:取滤液,和淀粉糊混合,观察是否变蓝。
请回答下列问题:
(1)氯气和碘化钠反应的化学方程式: 。
(2)上述3种方法中,方法 是一定不可行的,说出不可行的理由:
(3)取滤液,滴入硝酸银溶液,若观察到 ,则证明滤液中含碘离子。
①碘化钠(NaI)与氯化钠性质相似,两者的溶液都是盐溶液,碘化银为黄色难溶于水的固体。
②工业上将适量氯气通入无色碘化钠溶液就能置换出单质碘,溶液变为棕黄色。
③少量碘(I2)溶于水的溶液,能使淀粉溶液变蓝,碘的化合物不能使淀粉溶液变蓝。
④灼烧海带后残留的灰烬中含有可溶性碘化钠、氯化钠等化合物。
小李的实验步骤如下:
将海带灰用蒸馏水充分浸泡后过滤,得滤液;然后用以下3种方法,去检验海带灰中是否含有碘元素。
方法一:取滤液,通入适量氯气后与淀粉糊混合,观察是否变蓝。
方法二:取滤液,通入适量的氯气,观察溶液有无颜色变化。
方法三:取滤液,和淀粉糊混合,观察是否变蓝。
请回答下列问题:
(1)氯气和碘化钠反应的化学方程式: 。
(2)上述3种方法中,方法 是一定不可行的,说出不可行的理由:
(3)取滤液,滴入硝酸银溶液,若观察到 ,则证明滤液中含碘离子。
9.为测定空气中氧气的体积分数,小徐查询资料后进行如下实验。
实验药品:四硫化钠(Na2S4)固体、水
实验原理:2Na2S4+O2+2H2O═8S↓+4NaOH
实验步骤:
a、足量的四硫化钠固体置于试管中,加入适量的水并迅速塞紧橡胶塞,测量液面至橡胶塞的距离,记录数据h1,如图甲。
b、再充分振荡后,将该试管倒插入水中,取出橡胶塞,观察到试管内液面上升,如图乙。
c、当管内液面稳定时塞紧橡胶塞,将试管取出正放,测量液面至橡胶塞的距离,记录数据h2,如图丙。

(1)步骤b中将试管进行充分振荡的目的是 。
(2)实验测得空气中氧气的体积分数为 (用h1,h2表示)。
(3)四硫化钠固体可用于本实验的原因是 (写出一条即可)。
实验药品:四硫化钠(Na2S4)固体、水
实验原理:2Na2S4+O2+2H2O═8S↓+4NaOH
实验步骤:
a、足量的四硫化钠固体置于试管中,加入适量的水并迅速塞紧橡胶塞,测量液面至橡胶塞的距离,记录数据h1,如图甲。
b、再充分振荡后,将该试管倒插入水中,取出橡胶塞,观察到试管内液面上升,如图乙。
c、当管内液面稳定时塞紧橡胶塞,将试管取出正放,测量液面至橡胶塞的距离,记录数据h2,如图丙。

(1)步骤b中将试管进行充分振荡的目的是 。
(2)实验测得空气中氧气的体积分数为 (用h1,h2表示)。
(3)四硫化钠固体可用于本实验的原因是 (写出一条即可)。
10.有一包红色粉末,可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种,为确定该粉末的成分,同学们利用下图进行了探究。
[提出猜想]甲:可能是铜粉;乙:可能是氧化铁粉末;丙:可能是铜粉和氧化铁粉末。
[设计实验]方案1:取少量红色粉末放入试管中,滴加足量的稀硫酸,充分反应。如观察到实验现象为 时,则乙猜想正确。
方案2:取m克红色粉末放入硬质玻璃管中,先通入CO,再用酒精喷灯加热(图所示),完全反应后,停止加热并继续通入CO至装置冷却,称得剩余固体质量为n克。
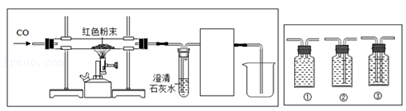
实验时要先通CO再加热的目的是 。
[数据处理]若丙猜想正确,则根据方案2所测数据,红色粉末中氧化铁的质量分数是 。
[实验反思]图虚线框内的装置是用于吸收CO2并收集CO,请从图(广口瓶内均为氢氧化钠溶液)中选择最合适的装置 (填序号)。
[提出猜想]甲:可能是铜粉;乙:可能是氧化铁粉末;丙:可能是铜粉和氧化铁粉末。
[设计实验]方案1:取少量红色粉末放入试管中,滴加足量的稀硫酸,充分反应。如观察到实验现象为 时,则乙猜想正确。
方案2:取m克红色粉末放入硬质玻璃管中,先通入CO,再用酒精喷灯加热(图所示),完全反应后,停止加热并继续通入CO至装置冷却,称得剩余固体质量为n克。

实验时要先通CO再加热的目的是 。
[数据处理]若丙猜想正确,则根据方案2所测数据,红色粉末中氧化铁的质量分数是 。
[实验反思]图虚线框内的装置是用于吸收CO2并收集CO,请从图(广口瓶内均为氢氧化钠溶液)中选择最合适的装置 (填序号)。
11.称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示。试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4↓+2NaCl)
(1)完全反应后生成BaSO4沉淀 g。
(2)恰好完全反应时消耗Na2SO4溶液的质量是多少克?
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)

(1)完全反应后生成BaSO4沉淀 g。
(2)恰好完全反应时消耗Na2SO4溶液的质量是多少克?
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)

12.生活离不开科学,科学与生活息息相关。
(1)均衡膳食有益健康、下列食物中,富含维生素的是 (填字母序号)。
A.蔬菜
B.鸡蛋
C.牛奶
D.土豆
(2)图甲所示为我国研发的“柔性、可裁剪碲化铋(Bi2Te3)/纤维素复合热点薄膜电池”,它能充分贴合人体体表,实现利用体表散热为智能手环供电。在碲化铋(Bi2Te3)中,碲元素的化合价为﹣2价,则铋元素的化合价为 价,此电池的能量转化是 。

(3)为解决日益加剧的温室效应问题,科学家研究建立上图所示的二氧化碳新循环体系:根据上述关系图,下列说法正确的是 (填序号)
①化学变化中元素种类守恒
②燃烧时化学能只转化为光能
③无机物和有机物可以相互转化
④二氧化碳也是一种重要的资源
(1)均衡膳食有益健康、下列食物中,富含维生素的是 (填字母序号)。
A.蔬菜
B.鸡蛋
C.牛奶
D.土豆
(2)图甲所示为我国研发的“柔性、可裁剪碲化铋(Bi2Te3)/纤维素复合热点薄膜电池”,它能充分贴合人体体表,实现利用体表散热为智能手环供电。在碲化铋(Bi2Te3)中,碲元素的化合价为﹣2价,则铋元素的化合价为 价,此电池的能量转化是 。

(3)为解决日益加剧的温室效应问题,科学家研究建立上图所示的二氧化碳新循环体系:根据上述关系图,下列说法正确的是 (填序号)
①化学变化中元素种类守恒
②燃烧时化学能只转化为光能
③无机物和有机物可以相互转化
④二氧化碳也是一种重要的资源
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解