下载高清试卷
【2021年甘肃省兰州市中考化学试卷(B卷)】-第1页
试卷格式:2021年甘肃省兰州市中考化学试卷(B卷).PDF
试卷热词:最新试卷、2021年、甘肃试卷、兰州市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.下列变化中,发生化学变化的是( )
- A. 滴水成冰
- B. 矿石粉碎
- C. 汽油挥发
- D. 粮食酿酒
2.兰州牛肉面享有“中华第一面”的美誉。下列食材富含蛋白质的是( )
- A. 牛肉
- B. 面条
- C. 萝卜
- D. 辣椒油
3.下列实验操作正确的是( )
- A.
 闻气味
闻气味 - B.
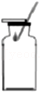 二氧化碳验满
二氧化碳验满 - C.
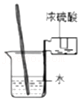 浓硫酸稀释
浓硫酸稀释 - D.
 测定溶液pH
测定溶液pH
4.如表为某同学用pH试纸测定的生活中一些物质的pH。其中酸性最强的是( )
| 物质 | 醋 | 酱油 | 牙膏 | 牛奶 |
| pH | 2 | 5 | 9 | 6 |
- A. 醋
- B. 酱油
- C. 牙膏
- D. 牛奶
5.下列关于水的说法不正确的是( )
- A. 可以用肥皂水鉴别软水和硬水
- B. 蒸馏对水的净化程度最高
- C. 农业上,改漫灌为滴灌可以节约水资源
- D. 电解水实验中,正极产生的气体可以燃烧
6.如图为硒元素在周期表中的信息及原子结构示意图。下列有关硒的说法错误的是( )
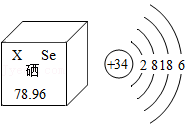

- A. X等于34
- B. 硒元素属于非金属元素
- C. 硒元素的相对原子质量为78.96g
- D. 硒原子在化学反应中易得电子形成Se2﹣
7.某同学学习了氯元素的部分内容后绘制了如图所示的类价二维图。下列有关认识不正确的是( )
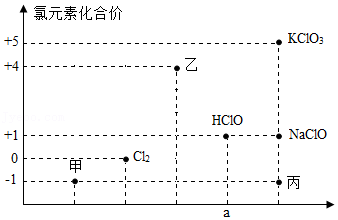

- A. 甲的水溶液可以用于金属表面除锈
- B. 乙的化学式为Cl2O
- C. a处物质类别为酸
- D. 丙物质可以是生活中一种常用的调味品
8.下列物质之间的转化不能通过化合反应一步实现的是( )
- A. H2O→Ca(OH)2
- B. H2→H2O
- C. CO2→CO
- D. BaCl2→BaSO4
9.物质的用途主要由其性质决定。下列说法中用途与化学性质无关的是( )
- A. CO用来炼铁
- B. 小苏打治疗胃酸过多
- C. 石墨用作电极
- D. 熟石灰改良酸性
10.化学与人类生活联系密切。下列有关说法正确的是( )
- A. 利用汽油的乳化作用可以除去衣服上的油污
- B. 煤、石油、天然气是不可再生能源
- C. 人体适当补充铁元素可预防骨质疏松
- D. 硝酸钾属于钾肥
11.如图是某化学变化的微观示意图,A、B、C分别表示不同类别的原子。下列说法正确的是( )
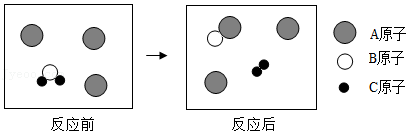

- A. A微粒构成的物质是该反应的催化剂
- B. 该反应中生成物的分子个数比1:1
- C. 反应前后分子和原子的种类均不变
- D. 反应物和生成物中只有一种单质
12.下列实验不能达到实验目的的是( )
- A.
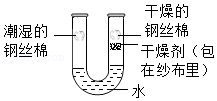 实验探究铁锈蚀是否与水有关
实验探究铁锈蚀是否与水有关 - B.
 实验探究二氧化碳是否与水发生反应
实验探究二氧化碳是否与水发生反应 - C.
 实验测定空气中氧气的含量
实验测定空气中氧气的含量 - D.
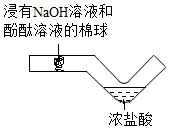 实验探究氢氧化钠与盐酸能否发生反应
实验探究氢氧化钠与盐酸能否发生反应
13.下列图像与所对应操作相符的是( )
- A.
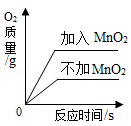 用两份等质量的氯酸钾制取氧气
用两份等质量的氯酸钾制取氧气 - B.
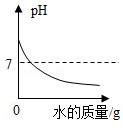 向一定量的氢氧化钠溶液中滴加水
向一定量的氢氧化钠溶液中滴加水 - C.
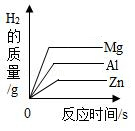 向足量相同溶质质量分数的稀硫酸中分别加入等质量Zn粉、Al粉、Mg粉
向足量相同溶质质量分数的稀硫酸中分别加入等质量Zn粉、Al粉、Mg粉 - D.
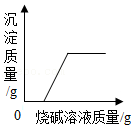 向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
14.下列实验操作能达到实验目的的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去NaNO3溶液中的MgCl2 | 加入适量NaOH溶液,过滤 |
| B | 除去氨气中混有的少量水蒸气 | 通入装有浓硫酸的洗气瓶 |
| C | 鉴别黄铜片和铜片 | 相互刻画 |
| D | 鉴别CO2和CO | 闻气味 |
- A. A
- B. B
- C. C
- D. D
15.在密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,在不同时刻测得各物质的质量(单位为克)如表所示。下列说法不正确的是( )
| 甲 | 乙 | 丙 | 丁 | |
| 反应前 | 20 | 64 | 6 | 10 |
| 反应中 | a | 48 | c | 19 |
| 反应后 | 4 | b | 50 | 46 |
- A. 丙和丁为生成物
- B. b=0
- C. 甲和丙的质量变化量之比为4:11
- D. 若乙和丙的相对分子质量为32和44,则乙和丙的化学计量系数之比为1:1
16.“奋斗者号”载人潜水器在2020年11月10日创造了中国潜入马里亚纳海沟10909米的新记录。其外壳和载人舱由强度高、抗压力强的钛合金制造。
(1)钛合金属于 。
A.合成材料
B.金属材料
C.天然材料
D.复合材料
(2)工业上通常是在高温条件下,在氩气保护的环境中,用四氯化钛(TiCl4)与金属镁反应获得钛和氯化镁,该反应的化学方程式为 。
(3)“奋斗者号”使用的锂电池正极材料为磷酸亚铁锂(LiFePO4),其中锂元素的化合价为+1价,则磷酸亚铁锂中磷元素的化合价为 价。
(4)碳酸二甲酯(C3H6O3)是锂电池电解液的一种成分,下列关于碳酸二甲酯的说法不正确的是 。
A.碳酸二甲酯属于有机物
B.碳酸二甲酯中碳、氧元素的质量比为3:4
C.碳酸二甲酯由三种元素组成
D.碳酸二甲酯分子由3个碳原子、6个氢原子和3个氧原子构成
(1)钛合金属于 。
A.合成材料
B.金属材料
C.天然材料
D.复合材料
(2)工业上通常是在高温条件下,在氩气保护的环境中,用四氯化钛(TiCl4)与金属镁反应获得钛和氯化镁,该反应的化学方程式为 。
(3)“奋斗者号”使用的锂电池正极材料为磷酸亚铁锂(LiFePO4),其中锂元素的化合价为+1价,则磷酸亚铁锂中磷元素的化合价为 价。
(4)碳酸二甲酯(C3H6O3)是锂电池电解液的一种成分,下列关于碳酸二甲酯的说法不正确的是 。
A.碳酸二甲酯属于有机物
B.碳酸二甲酯中碳、氧元素的质量比为3:4
C.碳酸二甲酯由三种元素组成
D.碳酸二甲酯分子由3个碳原子、6个氢原子和3个氧原子构成
17.甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:

(1)P点的含义是 。
(2)t2℃时,50g H2O与50g X混合,所得溶液中溶质质量分数为 。
(3)将t1℃时X、Y和Z三种物质的饱和溶液分别升温至t2℃,有晶体析出的是 。
(4)欲使Y的饱和溶液变为不饱和溶液,可以采取的措施是 (任写一种)。

(1)P点的含义是 。
(2)t2℃时,50g H2O与50g X混合,所得溶液中溶质质量分数为 。
(3)将t1℃时X、Y和Z三种物质的饱和溶液分别升温至t2℃,有晶体析出的是 。
(4)欲使Y的饱和溶液变为不饱和溶液,可以采取的措施是 (任写一种)。
18.阅读下面科普短文,回答有关问题。
甲醛(CH2O)在常温下是无色、有刺激性气味的气体,极易溶于水,是重要的工业原料。由于甲醛具有较高毒性,影响人体健康,因此刚装修好的房屋不宜立即入住,需开窗通风一段时间。
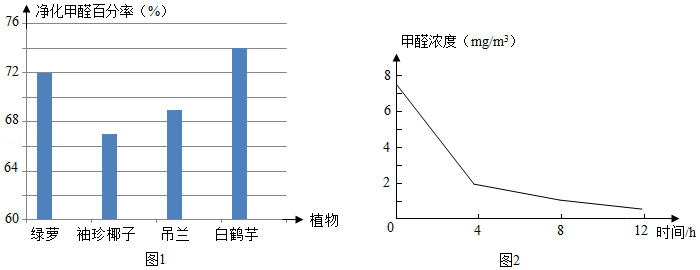
某实验小组在4个密闭仓中分别研究了绿萝、白鹤芋、吊兰、袖珍椰子4种观叶植物0﹣12h内净化甲醛的能力(图1)和绿萝在0﹣4h、4﹣8h、8﹣12h不同时间段净化甲醛的趋势(图2)。从图2中可以看出不同时间段植物净化甲醛的速率不同。造成这种现象的原因可能有两点,一是甲醛初始浓度高,对植物形成胁迫作用,植物为了缓解这种胁迫而调动自身某些快速反应机制将甲醛吸收代谢,当密闭仓中甲醛浓度降低到一定值时,植物感到胁迫降低,就放慢了代谢速率;二是植物的根系及盆土起到一定的净化作用,在较短时间内降低密闭仓中的甲醛浓度。
(原文作者:宋岚)
(1)活性炭对甲醛也有一定的净化能力,是因为活性炭具有 性。
(2)由图1可知,4种观叶植物净化甲醛百分率由大到小的顺序是 。
(3)根据图2分析,绿萝在 时间段内净化甲醛的速率最高。
(4)下列说法正确的是 。
A.用大量甲醛给海产品保鲜
B.甲醛是重要的工业原料,但使用时需考虑其对环境的影响
C.在甲醛浓度较高的初始阶段,根系和盆土没有起到净化作用
D.通风换气不能降低室内甲醛含量
甲醛(CH2O)在常温下是无色、有刺激性气味的气体,极易溶于水,是重要的工业原料。由于甲醛具有较高毒性,影响人体健康,因此刚装修好的房屋不宜立即入住,需开窗通风一段时间。
某实验小组在4个密闭仓中分别研究了绿萝、白鹤芋、吊兰、袖珍椰子4种观叶植物0﹣12h内净化甲醛的能力(图1)和绿萝在0﹣4h、4﹣8h、8﹣12h不同时间段净化甲醛的趋势(图2)。从图2中可以看出不同时间段植物净化甲醛的速率不同。造成这种现象的原因可能有两点,一是甲醛初始浓度高,对植物形成胁迫作用,植物为了缓解这种胁迫而调动自身某些快速反应机制将甲醛吸收代谢,当密闭仓中甲醛浓度降低到一定值时,植物感到胁迫降低,就放慢了代谢速率;二是植物的根系及盆土起到一定的净化作用,在较短时间内降低密闭仓中的甲醛浓度。
(原文作者:宋岚)

(1)活性炭对甲醛也有一定的净化能力,是因为活性炭具有 性。
(2)由图1可知,4种观叶植物净化甲醛百分率由大到小的顺序是 。
(3)根据图2分析,绿萝在 时间段内净化甲醛的速率最高。
(4)下列说法正确的是 。
A.用大量甲醛给海产品保鲜
B.甲醛是重要的工业原料,但使用时需考虑其对环境的影响
C.在甲醛浓度较高的初始阶段,根系和盆土没有起到净化作用
D.通风换气不能降低室内甲醛含量
19.工业上生产电路板及处理废液的工艺流程如图:
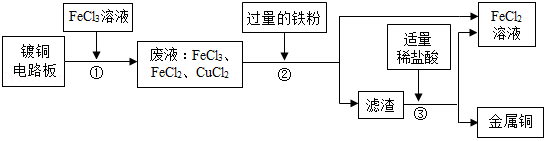
已知:Fe+2FeCl3═3FeCl2
(1)由步骤①可到断FeCl3与铜反应生成的两种产物是 。
(2)步骤②中发生置换反应的化学方程式为 ,说明金属的活动性:铁 铜。
(3)步骤③加入稀盐酸充分搅拌,当观察到 的现象时,说明滤渣只剩铜。

已知:Fe+2FeCl3═3FeCl2
(1)由步骤①可到断FeCl3与铜反应生成的两种产物是 。
(2)步骤②中发生置换反应的化学方程式为 ,说明金属的活动性:铁 铜。
(3)步骤③加入稀盐酸充分搅拌,当观察到 的现象时,说明滤渣只剩铜。
20.请结合图示实验装置,回答下列问题。
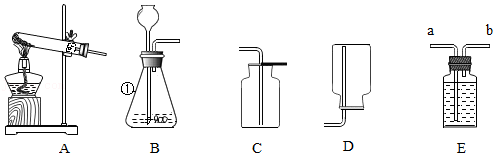
(1)仪器①的名称 。
(2)实验室用A装置制取氧气的化学方程式 。
(3)实验室中既能制取O2又能制取CO2的发生装置为 (填序号),收集CO2气体只能选择C装置,原因是 。
(4)若用E装置收集氧气,气体应该从E装置的 端通入(填“a”或“b”)。

(1)仪器①的名称 。
(2)实验室用A装置制取氧气的化学方程式 。
(3)实验室中既能制取O2又能制取CO2的发生装置为 (填序号),收集CO2气体只能选择C装置,原因是 。
(4)若用E装置收集氧气,气体应该从E装置的 端通入(填“a”或“b”)。
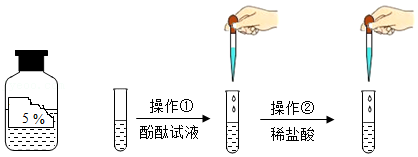
21.某实验小组同学在帮助实验员整理化学式剂时发现了一瓶标签破损的无色溶液,他们猜想瓶内原有的瓶体只能是Na2CO3溶液、NaOH溶液、BaCl2溶液、CuSO4溶液中的一种。为了判断瓶内是何种溶质,并确定试剂瓶的标签,实验小组的同学进行了如下探究活动:
【查阅资料】1.碳酸钠溶液显碱性。
2.氯化钡溶液显中性。
【实验探究1】
(1)大家认为该瓶溶液不可能是 ,原因是 。
(2)甲间学设计了如下方案探究瓶内溶质的成分:
①溶质不是 ;
② 。
【讨论质疑】乙同学认为甲同学的实验方案不严谨,小组同学讨论后一致认为还需要进行下一步探究。
(3)【实验探究2】另取少量瓶内液体于试管中,加入过量的BaCl2溶液(中性),观察到有白色沉淀生成,反应的化学方程式为 ;取上层清液,滴入酚酞试液,溶液呈红色。
(4)【得出结论】该溶液的溶质有 ,该试剂瓶标签上的物质为 。
(5)【反思拓展】造成该溶液出现上述实验现象的原因是 (用化学方程式表示)。

【查阅资料】1.碳酸钠溶液显碱性。
2.氯化钡溶液显中性。
【实验探究1】
(1)大家认为该瓶溶液不可能是 ,原因是 。
(2)甲间学设计了如下方案探究瓶内溶质的成分:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量瓶内液体于试管中,滴加酚酞试液 | 溶液变红色 | ①溶质不是________ |
| 向上述反应后的落液中滴加是足量稀盐酸 | ②________ | 溶质是Na2CO3 |
①溶质不是 ;
② 。
【讨论质疑】乙同学认为甲同学的实验方案不严谨,小组同学讨论后一致认为还需要进行下一步探究。
(3)【实验探究2】另取少量瓶内液体于试管中,加入过量的BaCl2溶液(中性),观察到有白色沉淀生成,反应的化学方程式为 ;取上层清液,滴入酚酞试液,溶液呈红色。
(4)【得出结论】该溶液的溶质有 ,该试剂瓶标签上的物质为 。
(5)【反思拓展】造成该溶液出现上述实验现象的原因是 (用化学方程式表示)。
22.在实验室制取二氧化碳的操作中,将40.0g石灰石加入足量稀盐酸中充分反应,反应过程中生成气体的质量与所加稀盐酸的质量关系如图所示。请回答下列问题(不考虑石灰石中杂质的影响):
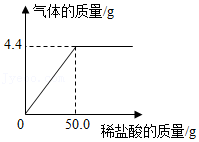
(1)反应生成CO2气体的质量 g。
(2)石灰石中碳酸钙的质量分数。

(1)反应生成CO2气体的质量 g。
(2)石灰石中碳酸钙的质量分数。
查看全部题目