下载高清试卷
【2021年山东省日照市中考化学试卷】-第1页
试卷格式:2021年山东省日照市中考化学试卷.PDF
试卷热词:最新试卷、2021年、山东试卷、日照市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.6月5日是世界环境日,2021年主题是“人与自然和谐共生”,下列做法不符合主题的是( )
- A. 使用脱硫煤,减少酸雨形成
- B. 深埋废旧电池,减少环境污染
- C. 使用可降解塑料,减少白色污染
- D. 倡导“低碳”生活,减少温室气体排放
2.下列图示的实验操作正确的是( )
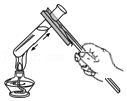 | 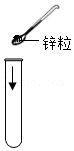 |  | 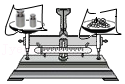 |
| A.加热液体 | B.向试管中加锌粒 | C.鉴别氯化钾和氯化铵 | D.称量食盐 |
- A. A
- B. B
- C. C
- D. D
3.对于人体必需元素,摄入不足或过量均不利于人体健康,下列说法错误的是( )
- A. 缺氟会引起贫血,过量会引起氟斑牙和氟骨病
- B. 缺碘或碘过量都会引起甲状腺肿大
- C. 缺锌会引起食欲不振,生长迟缓,发育不良
- D. 缺硒可能引起表皮角质化和癌症,如摄入量过高,会使人中毒
4.绿茶中含有的茶氨酸(C7H14N2O3)具有消脂减肥、健脑提神等功效。下列说法正确的是( )
- A. 茶氨酸中氮元素的质量分数为28%
- B. 茶氨酸由7个碳原子、14个氢原子、1个氮分子和3个氧原子构成
- C. 茶氨酸分子由碳、氢、氮、氧四种元素组成
- D. 茶氨酸中碳、氢、氮三种元素的质量比为6:1:2
5.某同学用氯酸钾和二氧化锰制取氧气,使用如图所示装置。下列说法或化学方程式正确的是( )
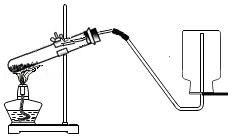

- A. 试管口略向上倾斜,利于管口冷凝水回流
- B. 导管伸入试管较长,便于气体导出
- C. 氧气的密度比空气小,用向下排空气法收集
- D. 2KClO32KCl+3O2↑
MnO2 △
6.下列物质的鉴别方法不能达到相应目的的是( )
| 选项 | 鉴别物质 | 鉴别方法 |
| A | 羊毛线和涤纶线 | 分别点燃,闻气味,观察现象 |
| B | K2SO4溶液和Na2SO4溶液 | 分别滴加Ba(OH)2溶液,观察现象 |
| NaCl溶液和Na2CO3溶液 | 分别滴加澄清石灰水,观察现象 | |
| D | 木炭粉和二氧化锰粉末 | 分别加入H2O2溶液,观察现象 |
- A. A
- B. B
- C. C
- D. D
7.甲醚与液化石油气相似,被誉为“21世纪的新型清洁、高效燃料”,具有优良的环保性能,可用作公交车燃料。甲醚燃烧反应的微观示意图如图所示。
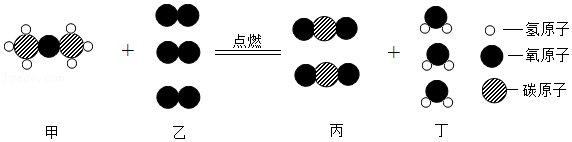
下列说法或化学方程式错误的是( )

下列说法或化学方程式错误的是( )
- A. CH3OCH3+3O22CO2+3H2O
点燃 - B. 丙、丁均为氧化物
- C. 反应前后分子的种类和数目保持不变
- D. 甲醚的化学式与乙醇相同
8.木炭与氧化铜的反应装置如图所示,下列说法错误的是( )
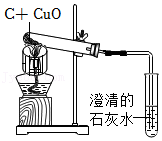

- A. 实验中,木炭体现氧化性
- B. 实验中,氧化铜发生还原反应
- C. 酒精灯上加网罩的目的是使火焰集中并提高温度
- D. 实验结束时,应先撤出导气管后熄灭酒精灯
9.现将等质量且形状相同的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量随反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2)。下列说法正确的是( )
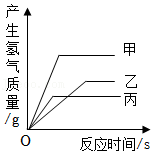

- A. 相对原子质量:丙<乙<甲
- B. 金属活动性:乙<丙<甲
- C. 消耗硫酸的质量:甲<乙<丙
- D. 甲、乙、丙可能分别是锌、铁、镁
10.用稀硫酸与氢氧化钠溶液反应探究中和反应实验时,测得溶液pH的变化如图所示,溶液温度的变化如图所示。下列说法错误的是( )


- A. b点和e点表示酸碱恰好完全反应
- B. 图中温度曲线从室温上升到e点,说明该反应是放热反应
- C. c点和f点所示溶液pH>7,能使无色酚酞溶液变成红色
- D. 该实验是将稀硫酸逐滴滴入一定量的氢氧化钠溶液中
11.试样X由FeO和CuO组成,取质量相等的两份试样按如图所示进行实验:
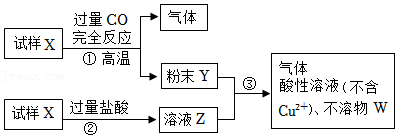
若全部的粉末Y和全部的溶液Z充分反应后生成的不溶物W的质量是6.4g,则每份试样X中CuO的质量为( )

若全部的粉末Y和全部的溶液Z充分反应后生成的不溶物W的质量是6.4g,则每份试样X中CuO的质量为( )
- A. 4g
- B. 8g
- C. 16g
- D. 32g
12.甲醛(HCHO)是一种无色、有刺激性气味的气体。甲醛在空气中充分燃烧生成CO2和H2O。现有HCHO和CO的混合气体20g,将其点燃,充分燃烧后,把生成的气体通入足量的澄清石灰水中,得到白色沉淀70g。下列说法错误的是( )
- A. 混合气体中碳元素的质量为8.4g
- B. 混合气体中氧元素的质量分数是56%
- C. 混合气体中氢元素的质量分数是4%
- D. 混合气体中HCHO和CO的质量比是3:7
13.2019年诺贝尔化学奖授予在锂离子电池研发领域做出卓越贡献的三位科学家。锂是最轻的金属。锂离子电池是可充电的新型高能电池,因质量轻、电容量大,被广泛应用于笔记本电脑、手机、摄像机等请回答下列问题:

(1)锂元素在元素周期表中的信息和锂的原子结构示意图如图所示,下列说法错误的是 (填字母)。
A.锂元素的相对原子质量是6.941g
B.x=2,锂原子核内质子数为3
C.锂元素位于元素周期表中第2周期
D.锂是相对原子质量最小的金属,其单质是密度最小的金属
(2)下图A~D所示粒子共表示 种元素。锂元素的化学性质与下图中 (填字母)的化学性质相似。

(3)某种锂离子电池充电时,钴酸锂(LiCoO2)和碳单质发生的反应可表示为LiCoO2+6C=Li1﹣x CoO2+R
(已配平),其中R的化学式为 。LiCoO2中Co的化合价为 。

(1)锂元素在元素周期表中的信息和锂的原子结构示意图如图所示,下列说法错误的是 (填字母)。
A.锂元素的相对原子质量是6.941g
B.x=2,锂原子核内质子数为3
C.锂元素位于元素周期表中第2周期
D.锂是相对原子质量最小的金属,其单质是密度最小的金属
(2)下图A~D所示粒子共表示 种元素。锂元素的化学性质与下图中 (填字母)的化学性质相似。

(3)某种锂离子电池充电时,钴酸锂(LiCoO2)和碳单质发生的反应可表示为LiCoO2+6C=Li1﹣x CoO2+R
(已配平),其中R的化学式为 。LiCoO2中Co的化合价为 。
14.2021年3月22日是第二十九届“世界水日“,其主题为“珍惜水、爱护水“。自来水厂净水过程示意图如下:
请回答下列问题:
(1)常用絮凝剂的名称是 ,常用吸附剂的名称是 。
(2)二氧化氯(ClO2)是净水过程中常用的消毒剂。工业上制备ClO2的一种方法是:2NaClO3+4HCl=2NaCl+2ClO2+Cl2↑+2H2O,此反应的反应物和生成物中氯元素的化合价共有 种。
(3)自来水进用户前,需进行检测化验。用pH试纸测定自来水的酸碱度,其操作方法是在白瓷板或玻璃片上放一小片pH试纸, ,把试纸显示的颜色与标准比色卡比较,读出自来水的pH。
(4)在实验室里,电解水的实验可证明水的组成,反应的化学方程式为 ,电解时,与电源正极相连的电极附近产生气体的化学式是 。

请回答下列问题:
(1)常用絮凝剂的名称是 ,常用吸附剂的名称是 。
(2)二氧化氯(ClO2)是净水过程中常用的消毒剂。工业上制备ClO2的一种方法是:2NaClO3+4HCl=2NaCl+2ClO2+Cl2↑+2H2O,此反应的反应物和生成物中氯元素的化合价共有 种。
(3)自来水进用户前,需进行检测化验。用pH试纸测定自来水的酸碱度,其操作方法是在白瓷板或玻璃片上放一小片pH试纸, ,把试纸显示的颜色与标准比色卡比较,读出自来水的pH。
(4)在实验室里,电解水的实验可证明水的组成,反应的化学方程式为 ,电解时,与电源正极相连的电极附近产生气体的化学式是 。
15.已知KCl、Na2SO4两种固体的溶解度曲线如图所示。请回答下列问题:

(1)下列说法错误的是 (填字母,下同)。
A.t=27℃(或t=61℃)时,KCl与Na2SO4的溶解度相等
B.t<27℃时,饱和溶液中溶质的质量分数:KCl≤Na2SO4
C.27℃<t≤61℃时,溶解度:KCl≤Na2SO4
D.t=27℃时,将不饱和KCl溶液变成其饱和溶液,可用加溶质的方法
(2)现有40℃时KCl和Na2SO4的饱和溶液(只含两种溶质,且均饱和),若要得到纯净的Na2SO4晶体,下列措施可行的是 。
A.降温到10℃,过滤
B.降温到27℃,过滤
C.升温到61℃,趁热过滤
D.蒸发适量水后,恢复到40℃,过滤
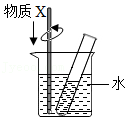
(3)如图所示,试管内是61℃时KCl或Na2SO4的饱和溶液,若向烧杯内的水中加入物质X,会观察到试管内有固体析出,则试管内溶液中的溶质与X的组合可能是下表中的 。
(4)40℃时,将Na2SO4的饱和溶液148g稀释成溶质质量分数为24%的Na2SO4溶液,需加入水的质量为 g。

(1)下列说法错误的是 (填字母,下同)。
A.t=27℃(或t=61℃)时,KCl与Na2SO4的溶解度相等
B.t<27℃时,饱和溶液中溶质的质量分数:KCl≤Na2SO4
C.27℃<t≤61℃时,溶解度:KCl≤Na2SO4
D.t=27℃时,将不饱和KCl溶液变成其饱和溶液,可用加溶质的方法
(2)现有40℃时KCl和Na2SO4的饱和溶液(只含两种溶质,且均饱和),若要得到纯净的Na2SO4晶体,下列措施可行的是 。
A.降温到10℃,过滤
B.降温到27℃,过滤
C.升温到61℃,趁热过滤
D.蒸发适量水后,恢复到40℃,过滤
(3)如图所示,试管内是61℃时KCl或Na2SO4的饱和溶液,若向烧杯内的水中加入物质X,会观察到试管内有固体析出,则试管内溶液中的溶质与X的组合可能是下表中的 。

| 选项 | A | B | C | D |
| 试管内溶液中的溶质 | KCl | KCl | Na2SO4 | Na2SO4 |
| 物质X | NH4NO3 | CaO | NaCl | 浓硫酸 |
(4)40℃时,将Na2SO4的饱和溶液148g稀释成溶质质量分数为24%的Na2SO4溶液,需加入水的质量为 g。
16.硅及其化合物广泛应用于计算机、电子部件制造等领域。芯片是电脑、智能家电的核心部件,它以高纯硅为材料制成。工业上,用焦炭与二氧化硅反应得到含有少量杂质的粗硅,将粗硅提纯后可以得到高纯硅,工艺流程简图如下。请回答下列问题:

(1)硅与地壳中含量(质量分数)最多的元素组成化合物的化学式为 。
(2)反应②的基本反应类型是 。
(3)反应③的化学方程式为 。
(4)实验室里,二氧化硅与镁粉混合加热发生置换反应,也可得到粗硅,反应的化学方程式为 。
(5)SiH4与HCl,每个分子内所有原子的电子数总和均为 (填数字)。

(1)硅与地壳中含量(质量分数)最多的元素组成化合物的化学式为 。
(2)反应②的基本反应类型是 。
(3)反应③的化学方程式为 。
(4)实验室里,二氧化硅与镁粉混合加热发生置换反应,也可得到粗硅,反应的化学方程式为 。
(5)SiH4与HCl,每个分子内所有原子的电子数总和均为 (填数字)。
17.乙二酸俗称草酸,菠菜等植物中含量较多。在浓硫酸存在和加热到157℃条件下,乙二酸能发生反应:
H2C2O4
H2O↑+CO2↑+CO↑。依据下列装置进行实验,可验证乙二酸发生分解反应的产物。
已知白色无水硫酸铜粉末遇水变蓝。请回答下列问题:
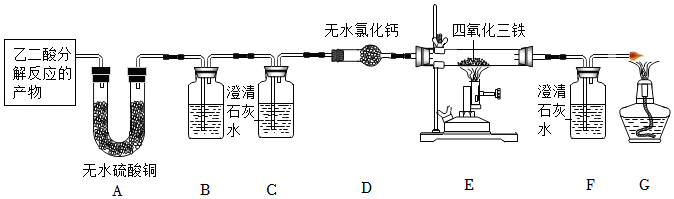
(1)实验中观察到A中现象是 ,A与D中的仪器及药品 (填“能”或“不能”)互换。
(2)B中试剂瓶内盛放足量的物质,其名称是 。
(3)实验时E中发生反应的化学方程式为 。
(4)C中澄清石灰水不变浑浊,F中澄清石灰水变浑浊,证明乙二酸发生分解反应的产物中有 (填化学式)。
(5)G处点燃尾气,发生反应的化学方程式为 。
H2C2O4
| 浓H2SO4 |
已知白色无水硫酸铜粉末遇水变蓝。请回答下列问题:

(1)实验中观察到A中现象是 ,A与D中的仪器及药品 (填“能”或“不能”)互换。
(2)B中试剂瓶内盛放足量的物质,其名称是 。
(3)实验时E中发生反应的化学方程式为 。
(4)C中澄清石灰水不变浑浊,F中澄清石灰水变浑浊,证明乙二酸发生分解反应的产物中有 (填化学式)。
(5)G处点燃尾气,发生反应的化学方程式为 。
18.实验室里有密度为1.84g/cm3的溶质质量分数为98%的浓硫酸,欲用来配制溶质质量分数为9.2%的稀硫酸196g,然后用这种稀硫酸除去铁锈。请回答下列问题:
(1)需要98%浓硫酸的体积为 mL,需要水的体积为 mL。(水的密度可近似看作1g/cm3)
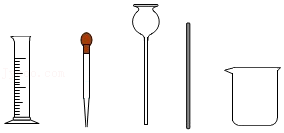
(2)配制过程中,如图仪器不需要的有 (填写仪器名称)。
(3)实验时,如果不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后再涂上3%﹣5%的 溶液。
(4)经测定,配制的稀硫酸中溶质的质量分数小于9.2%,其原因可能是下列中的 (填写字母标号)。
①所用98%的浓碱酸在实验桌上敞口放置一段时间
②稀释前,用蒸馏水润洗配制稀硫酸的烧杯
③量取水的体积时,俯视读数
④把量好的水倒入烧杯时,有少量水溅出烧杯
⑤量取浓硫酸的体职时,仰视读数
A. ①③⑤
B. ③④⑤
C. ①②
D. ②④

(1)需要98%浓硫酸的体积为 mL,需要水的体积为 mL。(水的密度可近似看作1g/cm3)
(2)配制过程中,如图仪器不需要的有 (填写仪器名称)。
(3)实验时,如果不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后再涂上3%﹣5%的 溶液。
(4)经测定,配制的稀硫酸中溶质的质量分数小于9.2%,其原因可能是下列中的 (填写字母标号)。
①所用98%的浓碱酸在实验桌上敞口放置一段时间
②稀释前,用蒸馏水润洗配制稀硫酸的烧杯
③量取水的体积时,俯视读数
④把量好的水倒入烧杯时,有少量水溅出烧杯
⑤量取浓硫酸的体职时,仰视读数
A. ①③⑤
B. ③④⑤
C. ①②
D. ②④
19.某化工产品的成分是氯化钾和氢氧化钾的固体混合物。20℃时,在实验室里,甲、乙、丙三位同学分别取该固体样品放入锥形瓶中,然后再向锥形瓶中加入氯化铜溶液,振荡,充分反应后过滤,称量沉淀的质量。测得实验数据如下表:
请回答下列问题:
(1)表中m的数值为 ; 同学所做的实验中,反应物恰好完全反应。
(2)恰好完全反应时,计算所得溶液中溶质的质量分数。
| 甲 | 乙 | 丙 | |
| 所取固体样品的质量/g | 20 | 20 | 30 |
| 加入氯化铜溶液的质量/g | 100 | 89.8 | 89.8 |
| 反应后生成沉淀的质量/g | 9.8 | m | 9.8 |
请回答下列问题:
(1)表中m的数值为 ; 同学所做的实验中,反应物恰好完全反应。
(2)恰好完全反应时,计算所得溶液中溶质的质量分数。
查看全部题目