下载高清试卷
【2022年湖南省娄底市中考化学一模试卷】-第1页
试卷格式:2022年湖南省娄底市中考化学一模试卷.PDF
试卷热词:最新试卷、2022年、湖南试卷、娄底市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.2022年2月4日20点,万众瞩目的第二十四届冬奥会在北京隆重开幕。在冬奥会开幕盛典中发生的化学变化是( )
- A. LED屏幕发光
- B. 点燃火炬
- C. 雕刻会徽
- D. 升起国旗
2.中国政府承诺“努力争取2060年前实现碳中和”,“碳中和”是使碳排放与碳吸收达到平衡,实现二氧化碳相对“零排放”。为了实现碳中和,从实际出发,以下措施不可行的是( )
- A. 鼓励拼车或乘坐公共交通出行
- B. 推广垃圾分类处理,加强资源回收利用
- C. 禁止使用煤、石油等化石能源
- D. 采用物理或化学方法,捕集或吸收废气中的二氧化碳
3.下列基本实验操作不正确的是( )
- A.
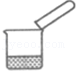 废液倒入指定容器内
废液倒入指定容器内 - B.
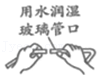 连接仪器
连接仪器 - C.
 取用液体
取用液体 - D.
 加热固体
加热固体
4.对物质进行分类是化学学习的常用方法,下列有关物质分类说法正确的是( )
- A. 金刚石和石墨都是由碳元素组成的纯净物
- B. 冰水混合后属于混合物
- C. 纯净的液态空气是纯净物
- D. 加热高锰酸钾完全分解后,得到的剩余固体是纯净物
5.安全警钟应时刻长鸣。下列做法错误的是( )
- A. 油锅着火,锅盖盖灭
- B. 燃气泄漏,点火检查
- C. 点燃氢气,提前验纯
- D. 面粉厂内,禁止吸烟
6.下列有关水的说法不正确的是( )
- A. 用水灭火的原理是降低可燃物的着火点
- B. 水是一种常见的溶剂
- C. 生活中可以用煮沸的方法降低水的硬度
- D. 电解水实验说明水由氢、氧元素组成
7.下列有关说法中,正确的是( )
- A. 分子可以直接构成物质,原子、离子则不能
- B. CO2和CO的化学性质有差异,是因为构成物质的分子不同
- C. 洗洁精除油污和汽油除油污都是利用乳化作用
- D. 均一、稳定的液体都是溶液
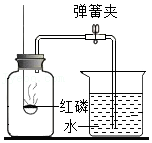
8.如图是用燃磷法测定“空气中氧气含量”的实验,下列说法正确的是( )

- A. 装置中的红磷可以用铁丝来代替
- B. 待红磷熄灭并冷却后,打开弹簧夹,再观察现象
- C. 红磷在空气中燃烧产生大量的白雾
- D. 实验测定氧气的质量约占空气总质量的
1 5
9.用如图所示四个实验探究二氧化碳能否与水反应,实验中所用的纸花均用石蕊染成紫色并干燥。下列说法错误的是( )
 ①喷稀醋酸 ①喷稀醋酸 |  ②喷水 ②喷水 |  ③直接放入CO2中 ③直接放入CO2中 | 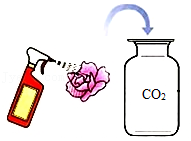 ④喷水后放入CO2中 ④喷水后放入CO2中 |
- A. ①和④的紫色纸花会变红
- B. 对比①,推断④有酸性物质生成
- C. 对比④纸花放入集气瓶前后的现象,省略②也能得出同样的实验结论
- D. 综合①②③④可得出的结论是:二氧化碳能与水反应生成碳酸,且碳酸很稳定
10.吸烟有害健康,香烟的烟气中含有几百种对人体有害的物质,其中尼古丁更是高度成瘾性物质。下列有关尼古丁(化学式为C10H14N2)的说法正确的是( )
- A. 一个尼古丁分子由26个原子构成
- B. 尼古丁中氮元素的质量分数最大
- C. 尼古丁中碳、氢、氮元素的质量比为5:7:1
- D. 尼古丁完全燃烧只生成CO2和H2O
11.下列物质敞口放置在空气中,杯内物质质量变少的是(不考虑水分蒸发)( )
- A. 浓硫酸
- B. 浓盐酸
- C. 澄清石灰水
- D. 氢氧化钠溶液
12.下列有关化学用语表示正确的是( )
- A. 五氧化二磷:P2O5
- B. 银元素:AG
- C. 2个镁离子:2Mg+2
- D. 8个硫原子:S8
13.通过置换反应可判断金属活动性顺序,某同学通过实验来比较铜、铝、银的金属活动性顺序,现有铜、铝、银的三种单质,如果另外只选用一种试剂达到实验目的,最好选用下列试剂中的( )
- A. 硫酸铜溶液
- B. 氯化铝溶液
- C. 硝酸银溶液
- D. 稀硫酸
14.硝酸钾、碳酸钾的溶解度如表。下列说法正确的是( )
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 | |
- A. 碳酸钾的溶解度受温度的影响较大
- B. 20℃时,100 g 的硝酸钾饱和溶液中含有31.6 g溶质
- C. 降低温度时,两种物质的溶液中均有晶体析出
- D. 两种物质的溶解度相等的温度范围是60~80℃
15.催化氧化是制硝酸的主要反应之一。该反应的微观示意图如图。下列说法正确的是( )
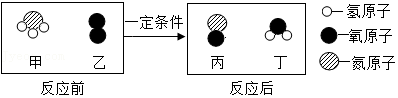

- A. 该反应中共有三种氧化物
- B. 该化学反应是置换反应
- C. 反应前后原子的种类不变
- D. 反应后生成的丙与丁的分子个数比为1:1
16.芯片是电脑、手机等的核心部件,碳基芯片采用石墨烯碳纳米管工艺,性能比硅基芯片更好,我国已突破半导体碳纳米管关键材料的技术瓶颈。请回答:
(1)石墨烯碳纳米管具有良好的 性。
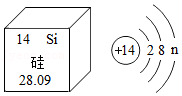
(2)如图是硅元素周期表中的部分信息及原子结构示意图,图中n= ,硅的相对原子质量是 ,硅元素位于元素周期表中的第 周期。
(3)化学反应中元素化合价升高的物质是还原剂,元素化合价降低的物质是氧化剂。在制硅反应SiO2+2C
Si+2CO↑中还原剂是 ,发生还原反应的物质是 。

(1)石墨烯碳纳米管具有良好的 性。
(2)如图是硅元素周期表中的部分信息及原子结构示意图,图中n= ,硅的相对原子质量是 ,硅元素位于元素周期表中的第 周期。
(3)化学反应中元素化合价升高的物质是还原剂,元素化合价降低的物质是氧化剂。在制硅反应SiO2+2C
| 高温 |
17.化学是一门以实验为基础的科学,请回答下列问题。
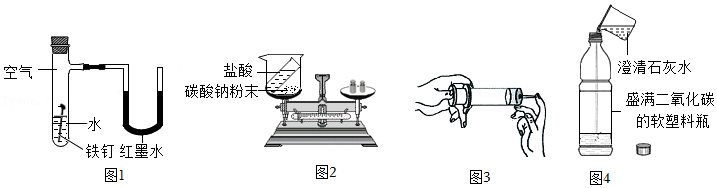
(1)图1中,当铁钉出现明显锈蚀时,U型管内的液面左端 (填“高于”、“低于”或“等于”)右端。
(2)利用图2装置验证质量守恒定律。若反应前天平平衡,反应后天平的指针会向 (填“左”或“右”)偏转。
(3)取气密性良好的两支大小相同的医用注射器,将栓塞向外拉,分别吸入等体积的空气和水,用手指顶住针筒末端的小孔,将栓塞慢慢推入(如图3所示),发现盛空气的注射器较易被压缩,原因是 。
(4)图4所示实验中,经振荡后可观察到的现象有 (填序号)。
①软塑料瓶变瘪
②瓶内溶液变红
③瓶内澄清石灰水变浑浊

(1)图1中,当铁钉出现明显锈蚀时,U型管内的液面左端 (填“高于”、“低于”或“等于”)右端。
(2)利用图2装置验证质量守恒定律。若反应前天平平衡,反应后天平的指针会向 (填“左”或“右”)偏转。
(3)取气密性良好的两支大小相同的医用注射器,将栓塞向外拉,分别吸入等体积的空气和水,用手指顶住针筒末端的小孔,将栓塞慢慢推入(如图3所示),发现盛空气的注射器较易被压缩,原因是 。
(4)图4所示实验中,经振荡后可观察到的现象有 (填序号)。
①软塑料瓶变瘪
②瓶内溶液变红
③瓶内澄清石灰水变浑浊
18.金属材料在生产生活中有广泛的用途。
(1)黄铜是铜锌合金,将纯铜片和黄铜片互相刻画,纯铜片上留下明显划痕,说明合金的硬度比组成它的纯金属的硬度 (填“大“或“小”)。
(2)铝制品具有很好的抗腐蚀性能,其原因是 。
(3)《淮南万毕术》一书中写到“曾青得铁则化为铜”,请用化学方程式表示 。
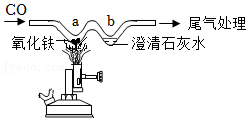
(4)如图,用“W”型玻璃管进行模拟工业炼铁的实验,下列说法正确的是 (填字母)。
A. 要先预热玻璃管,再通一氧化碳
B. a处黑色粉末变为红色
C. a处发生的是置换反应
D. 尾气可用燃着的酒精灯将其点燃或用气球收集起来

(1)黄铜是铜锌合金,将纯铜片和黄铜片互相刻画,纯铜片上留下明显划痕,说明合金的硬度比组成它的纯金属的硬度 (填“大“或“小”)。
(2)铝制品具有很好的抗腐蚀性能,其原因是 。
(3)《淮南万毕术》一书中写到“曾青得铁则化为铜”,请用化学方程式表示 。
(4)如图,用“W”型玻璃管进行模拟工业炼铁的实验,下列说法正确的是 (填字母)。
A. 要先预热玻璃管,再通一氧化碳
B. a处黑色粉末变为红色
C. a处发生的是置换反应
D. 尾气可用燃着的酒精灯将其点燃或用气球收集起来
19.阅读下面科普短文并根据文章内容,回答问题:
食醋中一般含有3%~5%的醋酸,醋酸的化学名称叫乙酸(CH3COOH),是无色有刺激性气味的液体,食醋是一种能增强食品酸味的调味剂,食醋可以除去水壶内的水垢,水垢的主要成分是碳酸钙。醋酸与碳酸钙的反应与稀盐酸与碳酸钙的反应原理相似。除水垢时,可在水壶中加入水,倒入适量醋,浸泡一段时间,不溶于水的碳酸钙会转变成可溶于水的醋酸钙而被除掉。食醋还是一种杀菌剂,冬天在屋子里熬醋可以杀灭细菌,对抗感冒有很大作用。饮酒过量的人可以用食醋来解酒,因为乙酸能跟乙醇发生酯化反应生成乙酸乙酯(有香味)和水,从而达到解酒的目的。醋酸与稀盐酸化学性质相似能与活泼的金属发生置换反应产生氢气。请回答:
(1)乙酸的物理性质 (任写一点)。
(2)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO﹣和 (填离子符号)。
(3)请把醋酸与碳酸钙反应的化学方程式补全。CaCO3+2CH3COOH═(CH3COO)2Ca+ 。
(4)炖鱼时放入适量白酒和白醋味道会更好的原因是 。
(5)家用铁制品不能用来盛放食醋的原因是 。
食醋中一般含有3%~5%的醋酸,醋酸的化学名称叫乙酸(CH3COOH),是无色有刺激性气味的液体,食醋是一种能增强食品酸味的调味剂,食醋可以除去水壶内的水垢,水垢的主要成分是碳酸钙。醋酸与碳酸钙的反应与稀盐酸与碳酸钙的反应原理相似。除水垢时,可在水壶中加入水,倒入适量醋,浸泡一段时间,不溶于水的碳酸钙会转变成可溶于水的醋酸钙而被除掉。食醋还是一种杀菌剂,冬天在屋子里熬醋可以杀灭细菌,对抗感冒有很大作用。饮酒过量的人可以用食醋来解酒,因为乙酸能跟乙醇发生酯化反应生成乙酸乙酯(有香味)和水,从而达到解酒的目的。醋酸与稀盐酸化学性质相似能与活泼的金属发生置换反应产生氢气。请回答:
(1)乙酸的物理性质 (任写一点)。
(2)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO﹣和 (填离子符号)。
(3)请把醋酸与碳酸钙反应的化学方程式补全。CaCO3+2CH3COOH═(CH3COO)2Ca+ 。
(4)炖鱼时放入适量白酒和白醋味道会更好的原因是 。
(5)家用铁制品不能用来盛放食醋的原因是 。
20.实验基本操作考试是娄底市中考必考内容,有以下两个实验:①CO2的制取:②配制50g 10%的NaCl溶液。
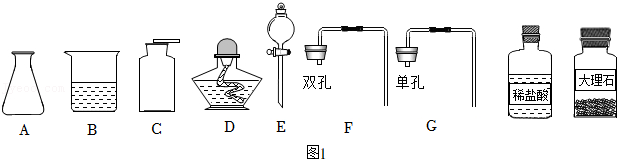
Ⅰ.甲同学抽签后来到实验室,发现本组实验桌上准备了如图1仪器和药品:
(1)图中仪器A的名称 。
(2)甲同学抽到的考签是CO2的制取,该实验的原理为 (用化学方程式表示),可选用的发生装置组合有 (填字母代号),请写出该发生装置的优点 。
Ⅱ.乙同学抽到“配制50g 10%的NaCl溶液”。他的操作步骤如图2所示:
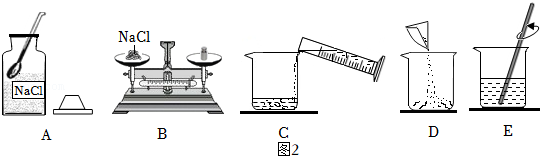
(3)乙同学因操作步骤不合理而扣分,请你予以纠正 。
(4)下列错误操作可能导致溶质质量分数小于10%的是 (填序号)。
①所称取的氯化钠固体不纯
②向烧杯中倒水溶解时部分水洒出
③装瓶时部分溶液洒出
④量取水时仰视读数

Ⅰ.甲同学抽签后来到实验室,发现本组实验桌上准备了如图1仪器和药品:
(1)图中仪器A的名称 。
(2)甲同学抽到的考签是CO2的制取,该实验的原理为 (用化学方程式表示),可选用的发生装置组合有 (填字母代号),请写出该发生装置的优点 。
Ⅱ.乙同学抽到“配制50g 10%的NaCl溶液”。他的操作步骤如图2所示:

(3)乙同学因操作步骤不合理而扣分,请你予以纠正 。
(4)下列错误操作可能导致溶质质量分数小于10%的是 (填序号)。
①所称取的氯化钠固体不纯
②向烧杯中倒水溶解时部分水洒出
③装瓶时部分溶液洒出
④量取水时仰视读数
21.实验课上,老师向滴有无色酚酞试液的NaOH红色溶液中滴加稀HCl,同学们观察到溶液颜色由红色变为无色,说明酸碱发生了中和反应。
【提出问题】HCl和NaOH是否恰好完全反应了?
【查阅资料】Ⅰ.常温下,酚酞在pH≤8.2的溶液中呈无色,在pH>8.2的溶液中呈红色。
Ⅱ.相同温度下,NaOH稀溶液中溶质的质量分数越大,溶液pH越大。
(1)【猜想假设】① ,溶液pH>7;
②恰好完全反应,溶液pH=7;
③HCl过量,溶液pH<7。
【理论论证】分别取少量反应后的无色溶液于3支试管中,按下列方案实验:
(2)假设 错误(填序号);
(3)假设①正确方案3的化学方程式 。
(4)【结论分析】反应后的无色溶液中还有少量NaOH,此时pH的范围 ;加热蒸发一段时间后,恢复至常温,当溶液的pH>8.2时,变为红色。
(5)【反思总结】向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后,溶液的颜色 变为红色。(填“一定”或“不一定”)
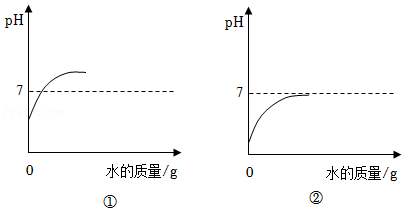
(6)【拓展应用】在探究酸碱性质的实验中,可借助pH传感器监测溶液pH的变化情况。常温下,向盐酸中加水稀释,溶液pH变化与如图吻合的是 。(填序号)
【提出问题】HCl和NaOH是否恰好完全反应了?
【查阅资料】Ⅰ.常温下,酚酞在pH≤8.2的溶液中呈无色,在pH>8.2的溶液中呈红色。
Ⅱ.相同温度下,NaOH稀溶液中溶质的质量分数越大,溶液pH越大。
(1)【猜想假设】① ,溶液pH>7;
②恰好完全反应,溶液pH=7;
③HCl过量,溶液pH<7。
【理论论证】分别取少量反应后的无色溶液于3支试管中,按下列方案实验:
| 实验操作 | 实验现象 | 实验结论 | |
| 方案1 | 滴加几滴碳酸氢钠溶液 | 无气泡产生 | (2)假设________错误(填序号) |
| 方案2 | 加热蒸发 | 蒸发过程中,发现溶液由无色变为红色 | (3)假设①正确方案3的化学方程式________ |
| 方案3 | 滴加几滴硫酸铜溶液 | 有蓝色沉淀生成 |
(2)假设 错误(填序号);
(3)假设①正确方案3的化学方程式 。
(4)【结论分析】反应后的无色溶液中还有少量NaOH,此时pH的范围 ;加热蒸发一段时间后,恢复至常温,当溶液的pH>8.2时,变为红色。
(5)【反思总结】向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后,溶液的颜色 变为红色。(填“一定”或“不一定”)
(6)【拓展应用】在探究酸碱性质的实验中,可借助pH传感器监测溶液pH的变化情况。常温下,向盐酸中加水稀释,溶液pH变化与如图吻合的是 。(填序号)

22.向50.8g溶质质量分数为5%的H2O2液中加入2g MnO2粉末。反应开始后产生氧气的总质量随时间的变化关系如图所示,请回答:
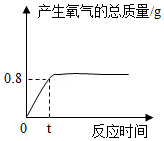
(1)从反应开始到t时,产生氧气的总质量是 g。
(2)试计算:t时,剩余H2O2溶液的溶质质量分数(写出计算过程)。

(1)从反应开始到t时,产生氧气的总质量是 g。
(2)试计算:t时,剩余H2O2溶液的溶质质量分数(写出计算过程)。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解