下载高清试卷
【2022年广东省佛山市顺德区中考化学一模试卷】-第1页
试卷格式:2022年广东省佛山市顺德区中考化学一模试卷.PDF
试卷热词:最新试卷、2022年、广东试卷、佛山市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.下列实验过程中发生了化学变化的是( )
- A. 影子形成
- B. 干冰升华
- C. 蜡烛燃烧
- D. 滚摆上升
2.实验室盛装氢氧化钠的试剂瓶应张贴的安全标志是( )
- A.

- B.

- C.

- D.

3.“以水美城、以水兴城”是顺德的发展战略,下列关于水的叙述合理的是( )
- A. 园林浇灌继续采用大水漫灌
- B. 防治水污染,禁止使用化肥和农药
- C. 生活中常用煮沸将硬水软化
- D. 净水时投药消毒只利用了物理性质
4.中国科学家研究表明:麻黄的有效成分麻黄碱(C10H15NO)可有效降低新冠肺炎死亡风险,下列说法正确的是( )
- A. 麻黄碱由10个碳原子、15个氢原子、1个氮原子和1个氧原子构成
- B. 麻黄碱是由四种元素组成的化合物
- C. 麻黄碱中氢元素的质量分数最大
- D. 麻黄与麻黄碱均属于纯净物
5.下列实验操作错误的是( )
- A.
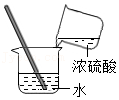 稀释浓硫酸
稀释浓硫酸 - B.
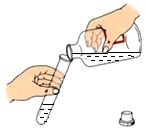 倾倒液体
倾倒液体 - C.
 测量pH
测量pH - D.
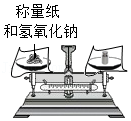 称量氢氧化钠
称量氢氧化钠
6.锂离子蓄电池在“祝融号”火星车的供配电系统中起着重要作用。如图是锂元素的某些信息,下列有关说法错误的是( )
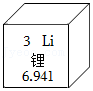

- A. 锂是金属元素
- B. 锂的相对原子质量是6.941g
- C. 锂原子在化学变化中易失去电子
- D. 锂的原子核内有3个质子
7.给淮山去皮时常会接触到含有呈碱性的皂角素黏液,往往会引起皮肤局部瘙痒,涂抹下列物质可缓解瘙痒的是( )
- A. 米醋(pH=3)
- B. 食盐水(pH=7)
- C. 牙膏(pH=9)
- D. 肥皂(pH=10)
8.氮及其化合物的“价类二维图”如图所示,正确的是( )
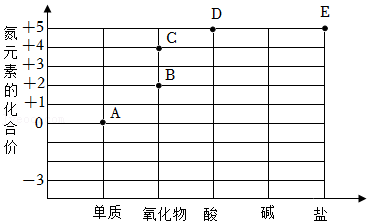

- A. A点对应的物质是氧气
- B. B点对应物质的化学式是N2O
- C. D点对应物质的化学式是N2O5
- D. E点对应物质的化学式可以是KNO3
9.实验室配制50g质量分数为6%的氯化钠溶液。下列说法错误的是( )
- A. 主要步骤包括计算、称量、量取、溶解等
- B. 主要仪器包括天平、量筒、烧杯、玻璃棒等
- C. 溶解时应将玻璃棒抵在烧杯底部进行搅拌
- D. 仰视量筒读数会使所配溶液的溶质质量分数偏小
10.下列实验设计不能达到实验目的是( )
- A.
 探究铁生锈的条件
探究铁生锈的条件 - B.
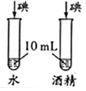 探究相同质量的碘在不同溶剂中的溶解性
探究相同质量的碘在不同溶剂中的溶解性 - C.
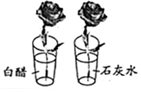 探究月季花的色素能否作酸碱指示剂
探究月季花的色素能否作酸碱指示剂 - D.
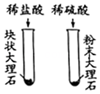 探究影响反应速率的因素
探究影响反应速率的因素
11.化学物质使世界变得更加绚丽多彩,下列物质的用途不合理的是( )
- A. 氢氧化钙用作建筑材料
- B. 氢氧化钠用于改良酸性土壤
- C. 碳酸钠用于制作洗涤剂
- D. 碳酸钙用作补钙剂
12.劳动成就梦想。下列劳动项目与所述化学知识不相符的是( )
| 选项 | 劳动项目 | 化学知识 |
| A | 用扇子扇煤炉火 | 提高煤的着火点 |
| B | 用草木灰(主要成分K2CO3)对蔬菜施肥 | 草木灰能起到抗倒伏作用 |
| C | 用厨余垃圾讴制有机肥 | 厨余垃圾富含N、P等元素 |
| D | 用铅笔芯作简易电池的电极材料 | 铅笔芯具有导电性 |
- A. A
- B. B
- C. C
- D. D
13.硫酸钠是一种重要的化工原料,其溶解度曲线如图所示。下列说法正确的是( )
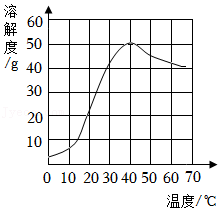

- A. 硫酸钠的溶解度随温度升高而增大
- B. 40℃时硫酸钠的溶解度约为50g
- C. 30℃时硫酸钠饱和溶液的质量分数约为42%
- D. 60℃时硫酸钠饱和溶液降温后一定是饱和溶液
14.我国学者开发促进CO2和H2反应生成甲醇(CH3OH)和水的一种新型催化剂,催化过程微观示意图如图,下列说法不正确的是( )
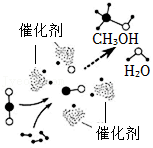

- A. 反应前后原子种类没有发生变化
- B. 两种反应物的分子个数比为1:3
- C. 反应前后催化剂的性质不变
- D. 该反应有利于实现“碳中和”
15.下列物质的鉴别或者物质的除杂方法不可行的是( )
| 鉴别或除杂 | 实验方法 | |
| A | 鉴别白酒和白醋 | 闻气味 |
| B | 鉴别NH4NO3固体和NaOH固体 | 取样于试管中加水,手触摸试管外壁 |
| C | 除去NaOH溶液中少量的Na2CO3 | 滴加适量的氢氧化钡溶液,过滤 |
| D | 除去二氧化碳中混有的少量HCl气体 | 将气体先通过氢氧化钠溶液,再通过浓硫酸 |
- A. A
- B. B
- C. C
- D. D
16.化学与我们的生活、生产、健康、环境等息息相关。回答下列问题:
(1)书写重要档案用碳素墨水,利用单质碳在常温下化学性质 ;明矾可用于净水,是因为明矾溶于水形成胶状物可以 悬浮于水中的杂质,使之从水中沉降出来。
(2)农业生产中常用CO(NH2)2、KCl、K2HPO4按一定比例来配制无土栽培的营养液,属于复合肥的是 ,尿素CO(NH2)2中氧元素和氢元素的质量比为 。
(3)服用含氢氧化铝【Al(OH)3】药物可以治疗胃酸(主要成分盐酸)过多症,药物反应原理是通过酸与碱发生 反应生成盐和水。
(4) 被认为是理想的清洁、高能燃料;温室效应增强是人类当前面临的最大环境问题,能产生温室效应的气体除 外、还有臭氧、甲烷、氟氯代烷等。
(1)书写重要档案用碳素墨水,利用单质碳在常温下化学性质 ;明矾可用于净水,是因为明矾溶于水形成胶状物可以 悬浮于水中的杂质,使之从水中沉降出来。
(2)农业生产中常用CO(NH2)2、KCl、K2HPO4按一定比例来配制无土栽培的营养液,属于复合肥的是 ,尿素CO(NH2)2中氧元素和氢元素的质量比为 。
(3)服用含氢氧化铝【Al(OH)3】药物可以治疗胃酸(主要成分盐酸)过多症,药物反应原理是通过酸与碱发生 反应生成盐和水。
(4) 被认为是理想的清洁、高能燃料;温室效应增强是人类当前面临的最大环境问题,能产生温室效应的气体除 外、还有臭氧、甲烷、氟氯代烷等。
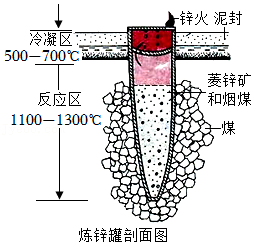
17.《天工开物•五金》中记载金属锌的冶炼方法:“每炉甘石(ZnCO3)十斤,装载入一泥罐内,封裹泥固,以渐砑干,勿使火拆裂。然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定,毁罐取出,每十耗去其二,即倭铅(金属锌)也,如图。
(已知:锌的熔点为419℃,沸点为907℃)
(1)将“炉甘石和煤炭”磨成粉末,目的是 ,“其底铺薪,发火煅红”是利用煤燃烧 热量。
(2)反应区中ZnCO3分解生成ZnO和另一种氧化物,反应的化学方程式为 。罐内煤炭的作用是 。
(3)冷凝区中,锌由气态转化为液态,理论上该区应控制的温度范围是 ℃;“冷定”后方能“毁罐”取锌,从化学变化角度看,可防止 。
(4)“锌火”主要是罐内产生的CO燃烧,避免其直排到空气中的的原因是 。

(已知:锌的熔点为419℃,沸点为907℃)
(1)将“炉甘石和煤炭”磨成粉末,目的是 ,“其底铺薪,发火煅红”是利用煤燃烧 热量。
(2)反应区中ZnCO3分解生成ZnO和另一种氧化物,反应的化学方程式为 。罐内煤炭的作用是 。
(3)冷凝区中,锌由气态转化为液态,理论上该区应控制的温度范围是 ℃;“冷定”后方能“毁罐”取锌,从化学变化角度看,可防止 。
(4)“锌火”主要是罐内产生的CO燃烧,避免其直排到空气中的的原因是 。
18.根据如图中的实验装置,回答下列问题:
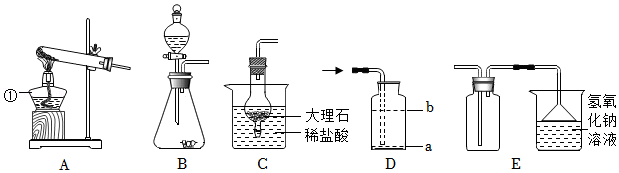
(1)仪器①的名称 ,用装置A制取O2,试管中反应的化学方程式为 。
(2)检查装置B气密性的方法:关闭活塞, ,则气密性良好。用锌粒和稀硫酸在该装置中制取H2,装置内反应的化学方程式为 。
(3)C装置的优点是可随时控制反应的发生与停止,如果打开弹簧夹,稀盐酸从干燥管下端小口进入,固体与液体 ,反应便能发生。若用装置D收集CO2,集气瓶中导管应处的位置是 (填“a”或“b”)。
(4)若用亚硫酸钠粉末和浓硫酸来制取SO2,所选用的发生装置是 (填字母),收集二氧化硫常用的是E装置,其中烧杯中的氢氧化钠溶液的作用 。

(1)仪器①的名称 ,用装置A制取O2,试管中反应的化学方程式为 。
(2)检查装置B气密性的方法:关闭活塞, ,则气密性良好。用锌粒和稀硫酸在该装置中制取H2,装置内反应的化学方程式为 。
(3)C装置的优点是可随时控制反应的发生与停止,如果打开弹簧夹,稀盐酸从干燥管下端小口进入,固体与液体 ,反应便能发生。若用装置D收集CO2,集气瓶中导管应处的位置是 (填“a”或“b”)。
(4)若用亚硫酸钠粉末和浓硫酸来制取SO2,所选用的发生装置是 (填字母),收集二氧化硫常用的是E装置,其中烧杯中的氢氧化钠溶液的作用 。
19.化学实践活动课上,老师拿来一包久置空气中的碱石灰干燥剂(氧化钙和氢氧化钠的混合物),让同学们设计实验进行探究。
(1)碱石灰极易与空气中的水蒸气、二氧化碳反应而变质,其中氧化钙与水的基本反应类型是 ,氢氧化钠在空气中变质的原因,用化学方程式解释为 ,因此碱石灰要 保存。
(2)同学们决定对这包碱石灰成分进行探究。
【猜想假设】
猜想Ⅰ:未变质,只含有氧化钙和氢氧化钠。
猜想Ⅱ:部分变质,有氢氧化钙、碳酸钙和碳酸钠等。
猜想Ⅲ:完全变质,只含有碳酸钙和碳酸钠。
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性。
(2)【设计实验】设计如下流程进行实验:
(3)【讨论分析】实验3是否可以先滴加过量氯化钙溶液,再滴入酚酞溶液,为什么? 。
(1)碱石灰极易与空气中的水蒸气、二氧化碳反应而变质,其中氧化钙与水的基本反应类型是 ,氢氧化钠在空气中变质的原因,用化学方程式解释为 ,因此碱石灰要 保存。
(2)同学们决定对这包碱石灰成分进行探究。
【猜想假设】
猜想Ⅰ:未变质,只含有氧化钙和氢氧化钠。
猜想Ⅱ:部分变质,有氢氧化钙、碳酸钙和碳酸钠等。
猜想Ⅲ:完全变质,只含有碳酸钙和碳酸钠。
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性。
(2)【设计实验】设计如下流程进行实验:
| 实验 | 实验步骤 | 现象 | 结论 |
| 实验1 | 取少量碱石灰样品于烧杯中,加入足量的水,触摸烧杯外壁,充分搅拌后过滤,得到滤渣和滤液。 | 温度________(填“升高”、“降低”或“没有变化”) | 猜想Ⅲ正确 |
| 实验2 | 取少量上述滤渣于试管中,滴加过量________,并将产生的气体通入澄清石灰水中。 | 产生气泡,澄清石灰水________ | |
| 实验3 | 取少量上述滤液于另一支试管中,先滴加酚酞溶液,再滴加过量氯化钙溶液。 | 溶液先变成红色,________ |
(3)【讨论分析】实验3是否可以先滴加过量氯化钙溶液,再滴入酚酞溶液,为什么? 。
20.碳酸亚铁(FeCO3)可作补血剂,某硫酸厂产生的炉渣中除了有Fe2O3、FeO,还有一定量的SiO2,兴趣小组利用炉渣尝试制备FeCO3,其流程如图所示:
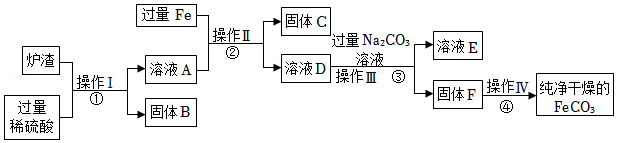
已知:SiO2不溶于水,也不与稀硫酸反应;碳酸亚铁隔绝空气加热至282℃开始分解为CO2和FeO。
(1)固体B的名称是 ,步骤①中Fe2O3发生反应的化学方程式 。
(2)反应②的化学方程式Fe+Fe2(SO4)3= ;
; 中的化学式 。操作Ⅱ的名称是 ,该操作所用到的玻璃仪器包括烧杯、漏斗和 。
中的化学式 。操作Ⅱ的名称是 ,该操作所用到的玻璃仪器包括烧杯、漏斗和 。
(3)步骤③反应发生的化学方程式 。溶液E中溶质的化学式 。
(4)操作Ⅳ包括洗涤、烘干等,其中烘干的温度不能超过282℃的原因 。

已知:SiO2不溶于水,也不与稀硫酸反应;碳酸亚铁隔绝空气加热至282℃开始分解为CO2和FeO。
(1)固体B的名称是 ,步骤①中Fe2O3发生反应的化学方程式 。
(2)反应②的化学方程式Fe+Fe2(SO4)3=
 ;
; 中的化学式 。操作Ⅱ的名称是 ,该操作所用到的玻璃仪器包括烧杯、漏斗和 。
中的化学式 。操作Ⅱ的名称是 ,该操作所用到的玻璃仪器包括烧杯、漏斗和 。(3)步骤③反应发生的化学方程式 。溶液E中溶质的化学式 。
(4)操作Ⅳ包括洗涤、烘干等,其中烘干的温度不能超过282℃的原因 。
21.某研究学习小组为探究木炭还原氧化铜的实验。
(1)氧化铜中铜元素的质量分数为 ;
(2)要使80g氧化铜完全被还原,需要碳的质量至少是多少?
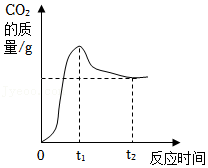
(3)小组同学将80g氧化铜和8.4g的炭粉在隔绝空气的容器中持续加强热,通过CO2传感器测得容器内CO2的质量变化曲线如图所示。
①t1时CO2的质量≤ 。
②分析t1﹣t2密闭容器中CO2的质量减少的原因是 。
③t2时容器内气体的碳、氧元素质量比为 。
(1)氧化铜中铜元素的质量分数为 ;
(2)要使80g氧化铜完全被还原,需要碳的质量至少是多少?
(3)小组同学将80g氧化铜和8.4g的炭粉在隔绝空气的容器中持续加强热,通过CO2传感器测得容器内CO2的质量变化曲线如图所示。
①t1时CO2的质量≤ 。
②分析t1﹣t2密闭容器中CO2的质量减少的原因是 。
③t2时容器内气体的碳、氧元素质量比为 。

查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解