下载高清试卷
【2021-2022学年江苏省南通市如东市九年级(上)期末化学试卷】-第1页
试卷格式:2021-2022学年江苏省南通市如东市九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2022年、江苏试卷、南通市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷

扫码查看解析
试卷题目
1.创建全国文明城市打造自然生态宜居宜业新南通。下列做法中,不合理的是( )
- A. 秸秆粉碎还田,禁止随意焚烧
- B. 垃圾分类回收,节约资源能源
- C. 骑行共享单车,倡导绿色出行
- D. 污水未经处理,直接排入大海
2.水是一种最常用的溶剂。下列做法或说法正确的是( )
- A. 用絮凝剂明矾可降低水的硬度
- B. 硝酸铵溶于水制成的冰袋可给高烧病人降温
- C. 天然水经过自然沉降、过滤、吸附,即得纯水
- D. 用150mL酒精和50mL蒸馏水混合配制200mL的医用酒精
3.下列物质的性质与用途不具有对应关系的是( )
- A. 干冰能与水反应,可用作制冷剂
- B. 石墨呈灰黑色、质软而滑腻,可用作铅笔芯
- C. 氮气化学性质不活泼,可用作金属焊接的保护气
- D. 生石灰与水反应放热,可用作自热食品的发热源
4.含碳物质与含铁物质有如图所示的转化关系,下列说法正确的是( )
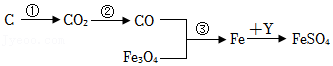

- A. 反应①只能是化合反应
- B. 反应②中CO2被还原
- C. 反应③为置换反应
- D. 物质Y可以为硫酸锌
5.金属材料包括铁、铝、铜等纯金属以及它们的合金。下列有关说法不正确的是( )
- A. 铝在空气中具有很好的抗腐蚀性能
- B. 生铁和钢都是铁的合金,属于混合物
- C. 黄铜片(铜锌合金)的硬度小于铜片的硬度
- D. 室温下钛与稀盐酸不能反应,可判断钛的金属活动性比镁弱
6.下列有关化学学科观念的说法中不正确的是( )
- A. 微粒观:水分子是由氢原子和氧原子构成的
- B. 守恒观:铁丝在氧气中燃烧,反应前后固体的质量相等
- C. 转化观:氧气和二氧化碳在定条件下可以相互转化
- D. 结构观:金刚石和石墨物理性质有明显差异,因为它们碳原子的排列方式不同
7.下列实验方案,不能达到相应实验目的的是( )
- A.
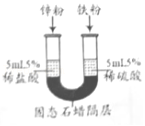 探究Zn、Fe金属活动性强弱
探究Zn、Fe金属活动性强弱 - B.
 探究铜在生成铜绿时是否需要CO2
探究铜在生成铜绿时是否需要CO2 - C.
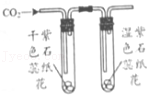 验证二氧化碳能与水发生反应
验证二氧化碳能与水发生反应 - D.
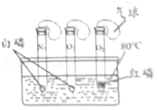 验证可燃物燃烧需要两个条件
验证可燃物燃烧需要两个条件
8.盐场晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,它们的溶液度曲线如图所示。下列说法正确的是( )


- A. KCl的溶解度大于MgSO4的溶解度
- B. t1℃时,100g MgCl2饱和溶液中含有60g MgCl2
- C. t1℃时,KCl和MgSO4饱和溶液所含的溶质质量相等
- D. 将t2℃时MgSO4的饱和溶液降温到t1℃,溶液依然饱和
9.下列有关实验室制取二氧化碳气体的说法正确的是( )(注:浓硫酸具有强吸水性)
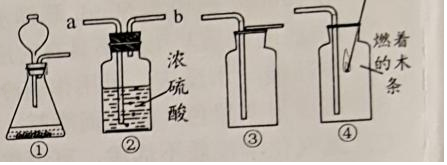

- A. 用装置①可以制取CO2
- B. 用装置②可干燥CO2,气体从b管进
- C. 用装置③可收集CO2
- D. 用装置④对CO2气体进行验满
10.实验室现有一瓶水垢样品,其成分为氢氧化镁和碳酸钙。已知:氢氧化镁受热易分解,反应的化学方程式为:Mg(OH)2
MgO+H2O;碳酸钙高温下才分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如图所示。关于加热一段时间后剩余固体的判断,下列说法不正确的是( )

| △ |

- A. 图中ab间任一点(不包括a、b两点)的剩余固体成分为CaCO3、MgO和Mg(OH)2
- B. 图中x=7.6
- C. 若向c点的剩余固体中加入足量稀盐酸,充分反应生成CO2的质量为4.4g
- D. 某时刻测得剩余固体中钙元素的质量分数为36.0%,则此时剩余固体的成分为CaCO3和MgO
11.宏观和微观相结合是认识物质结构与性质的重要方法,结合图示完成问题:
(1)图1是元素周期表中的一部分及硒原子的结构示意图。
①硒元素位于元素周期表中的第 周期。
②图1中n的值为 ,硒化钠的化学式为 。
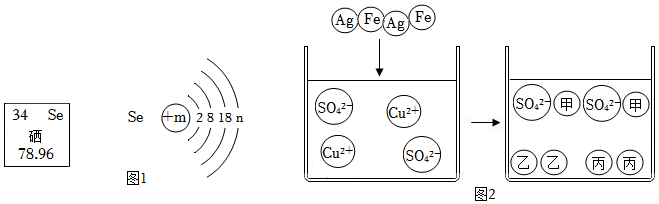
(2)向硫酸铜溶液中加入Fe、Ag两种金属,微观变化情况如图2。溶液中新生成的离子甲是 (填离子符号)。
(3)中国化学家研究的一种新型复合光催化利碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物可以利用太阳光实现高效分解水,原理如图所示。

①这个过程是将 能转化为化学能。
②写出反应Ⅰ的化学方程式: 。
(1)图1是元素周期表中的一部分及硒原子的结构示意图。
①硒元素位于元素周期表中的第 周期。
②图1中n的值为 ,硒化钠的化学式为 。

(2)向硫酸铜溶液中加入Fe、Ag两种金属,微观变化情况如图2。溶液中新生成的离子甲是 (填离子符号)。
(3)中国化学家研究的一种新型复合光催化利碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物可以利用太阳光实现高效分解水,原理如图所示。

①这个过程是将 能转化为化学能。
②写出反应Ⅰ的化学方程式: 。
12.以FeSO4•7H2O为原料制备铁红(Fe2O3)的一种方法如图:
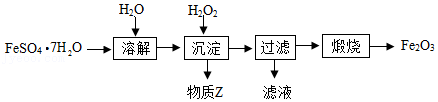
(1)“溶解”时能加快溶解的方法有 (写一种即可)。
(2)“沉淀”时的主要反应为:2FeSO4+H2O2+2H2O═2FeO(OH)↓+2 ,FeO(OH)中铁元素的化合价为 。“沉淀”时反应温度不宜过高,其原因是 。
(3)“过滤”后需对固体进行洗涤与干燥。实验室进行过滤时需要的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
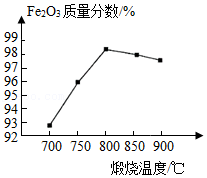
(4)“煅烧”时反应的化学方程式为 。在其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响如图。最适宜的煅烧温度为 ℃。

(1)“溶解”时能加快溶解的方法有 (写一种即可)。
(2)“沉淀”时的主要反应为:2FeSO4+H2O2+2H2O═2FeO(OH)↓+2 ,FeO(OH)中铁元素的化合价为 。“沉淀”时反应温度不宜过高,其原因是 。
(3)“过滤”后需对固体进行洗涤与干燥。实验室进行过滤时需要的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(4)“煅烧”时反应的化学方程式为 。在其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响如图。最适宜的煅烧温度为 ℃。

13.能源利用和环境保护已成为人类日益关注的问题。
(1)化石燃料主要包括煤、石油和 。煤燃烧时排放出二氧化氮、 (填化学式)等污染物会形成酸雨。化石燃料的使用,产生的CO2气体如果过度排放会造成 的加剧。
(2)为了充分发挥能源的作用,工业上常将煤进行如图的综合利用:

①将煤隔绝空气加强热的过程属于 变化(填“物理”或“化学”)。
②工业上用一氧化碳和赤铁矿(主要成分Fe2O3)高温下炼铁的化学方程式为 。
③工业上常将生铁(含C2%~4.3%)炼成钢(含C0.03%~2%),生铁炼钢时通入过量氧气的目的是 。
(3)氢燃料汽车投入使用的关键是解决氢气的储存和运输问题。氢化钙(CaH2)固体是一种储氢材料。氢化钙通常用氢气和钙加热制得,制备氢化钙固体的实验装置如图所示。
请阅读下列资料后回答问题:

资料:a、碱石灰是氧化钙和氢氧化钠的混合物:
b、钙、氢化钙遇水立即发生反应Ca+2H2O═Ca(OH)2+H2↑;CaH2+2H2O═Ca(OH)2+2H2↑。
①为了实验安全,点燃C装置酒精灯前应 ;
②装置A中生成氢气的化学方程式为: 。
③装置B的作用是 。
(1)化石燃料主要包括煤、石油和 。煤燃烧时排放出二氧化氮、 (填化学式)等污染物会形成酸雨。化石燃料的使用,产生的CO2气体如果过度排放会造成 的加剧。
(2)为了充分发挥能源的作用,工业上常将煤进行如图的综合利用:

①将煤隔绝空气加强热的过程属于 变化(填“物理”或“化学”)。
②工业上用一氧化碳和赤铁矿(主要成分Fe2O3)高温下炼铁的化学方程式为 。
③工业上常将生铁(含C2%~4.3%)炼成钢(含C0.03%~2%),生铁炼钢时通入过量氧气的目的是 。
(3)氢燃料汽车投入使用的关键是解决氢气的储存和运输问题。氢化钙(CaH2)固体是一种储氢材料。氢化钙通常用氢气和钙加热制得,制备氢化钙固体的实验装置如图所示。
请阅读下列资料后回答问题:

资料:a、碱石灰是氧化钙和氢氧化钠的混合物:
b、钙、氢化钙遇水立即发生反应Ca+2H2O═Ca(OH)2+H2↑;CaH2+2H2O═Ca(OH)2+2H2↑。
①为了实验安全,点燃C装置酒精灯前应 ;
②装置A中生成氢气的化学方程式为: 。
③装置B的作用是 。
14.某实验小组用石墨作电极进行电解水实验,为增加导电性,改用20℃时Ca(OH)2饱和溶液进行电解,实验时除两个电极均有气泡冒出外,在正极石墨电极的附近溶液中还出现了白色浑浊现象,该小组对白色浑浊出现的原因进行了探究。
[猜想与假设]
①电解过程中溶液温度升高,导致Ca(OH)2析出而出现白色浑浊。
②电解过程中因水量的减少,导致Ca(OH)2析出而出现白色浑浊。
③与电极材料石墨(主要成分是碳)有关。
[查阅资料]
Ⅰ.氢氧化钙的溶解度曲线如图所示。
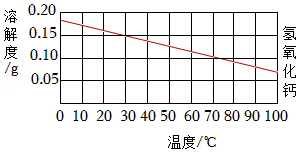
Ⅱ.氢氧化钙饱和溶液通电后温度约上升5℃。
[进行实验]
(1)实验1.甲同学通过实验排除了猜想①的可能性。简述甲同学的实验方案 。
实验2.乙同学进行了如下实验:
(2)猜想 (填序号)不合理。
实验3.丙同学进行了如下实验:
[解释与结论]
(3)给Ca(OH)2饱和溶液加热,温度上升5℃后得到的溶液为Ca(OH)2 (填“饱和”或“不饱和”)溶液。
(4)实验3中更换石墨电极为惰性铂电极,通电2分钟后a、b两电极气体的体积比约为 。
(5)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是 ,溶液中产生白色浑浊的化学方程式为 。
[猜想与假设]
①电解过程中溶液温度升高,导致Ca(OH)2析出而出现白色浑浊。
②电解过程中因水量的减少,导致Ca(OH)2析出而出现白色浑浊。
③与电极材料石墨(主要成分是碳)有关。
[查阅资料]
Ⅰ.氢氧化钙的溶解度曲线如图所示。

Ⅱ.氢氧化钙饱和溶液通电后温度约上升5℃。
[进行实验]
(1)实验1.甲同学通过实验排除了猜想①的可能性。简述甲同学的实验方案 。
实验2.乙同学进行了如下实验:
| 实验装置 | 主要实验操作 | 实验现象 | 实验结论 |
 | 用石墨做电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生:a试管中溶液未出现白色浑浊;b试管中溶液明显出现白色浑浊 | (2)猜想________(填序号)不合理。 |
| 取少量b试管中白色浑浊液,加10mL水,振荡 | 白色浑浊不溶解 |
(2)猜想 (填序号)不合理。
实验3.丙同学进行了如下实验:
| 主要实验操作 | 实验现象 |
| 更换石墨电极为惰性铂电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生:a、b试管中溶液均未出现白色浑浊 |
[解释与结论]
(3)给Ca(OH)2饱和溶液加热,温度上升5℃后得到的溶液为Ca(OH)2 (填“饱和”或“不饱和”)溶液。
(4)实验3中更换石墨电极为惰性铂电极,通电2分钟后a、b两电极气体的体积比约为 。
(5)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是 ,溶液中产生白色浑浊的化学方程式为 。
15.在抗击“新冠肺炎“疫情期间,常用一定浓度的过氧乙酸(CH3COOOH)溶液对公共场所进行消毒。过氧乙酸是无色透明液体,易挥发,化学性质不稳定,遇热易分解。
(1)市售过氧乙酸溶液的质量分数一般为20%。保存该溶液的方法是 ;若以其为原料配制200kg质量分数为0.5%的稀溶液,所需水的质量为 kg。
(2)工业上常以冰醋酸(纯净物)、过氧化氢为原料制备过氧乙酸,其反应原理为:CH3COOH+H2O2═CH3COOOH+H2O。某同学利用该原理制备过氧乙酸溶液,步骤如下:
步骤Ⅰ:取质量分数为5%过氧化氢溶液136g于烧杯中。
步骤Ⅱ:向烧杯中加入冰醋酸至过氧化氢恰好完全反应(借助于某种指示剂指示反应终点)。
计算所得过氧乙酸溶液的质量 。(请将计算过程写在答题卡上)
(1)市售过氧乙酸溶液的质量分数一般为20%。保存该溶液的方法是 ;若以其为原料配制200kg质量分数为0.5%的稀溶液,所需水的质量为 kg。
(2)工业上常以冰醋酸(纯净物)、过氧化氢为原料制备过氧乙酸,其反应原理为:CH3COOH+H2O2═CH3COOOH+H2O。某同学利用该原理制备过氧乙酸溶液,步骤如下:
步骤Ⅰ:取质量分数为5%过氧化氢溶液136g于烧杯中。
步骤Ⅱ:向烧杯中加入冰醋酸至过氧化氢恰好完全反应(借助于某种指示剂指示反应终点)。
计算所得过氧乙酸溶液的质量 。(请将计算过程写在答题卡上)
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解