下载高清试卷
【2021-2022学年江苏省南京市浦口区九年级(上)期末化学试卷】-第1页
试卷格式:2021-2022学年江苏省南京市浦口区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2022年、江苏试卷、南京市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷

扫码查看解析
试卷题目
1.下列金属中导电性能最好的是( )
- A. 铜
- B. 铝
- C. 铁
- D. 银
2.下列有关“美丽中国”生态文明建设的措施,理解不正确的是( )
- A. 开发新能源,以如期实现“碳达峰、碳中和”
- B. 坚持“绿色化学”理念,努力实现零排放
- C. “垃圾分类”可充分利用资源,保护生态环境
- D. “雨污分流”以防止酸雨对水源造成污染
3.下列物质由分子构成的是( )
- A. 铝
- B. 氢氧化钠
- C. 金刚石
- D. C60
4.下列化学用语书写不正确的是( )
- A. 2个氢原子:2H
- B. 氢气中氢元素的化合价:2
+1 H - C. 2个氢分子:2H2
- D. 2个氢离子:2H+
5.下列有关做法,不符合安全要求的是( )
- A. 油锅着火,可倒入蔬菜,降温灭火
- B. 加油站不应建有围墙
- C. 煤矿井下应保持通风良好,严禁烟火
- D. 夜间闻到“燃气”气味,应开灯及时查明漏点
6.分类是解决复杂问题的一种思维方法,下列相关分类不正确的是( )
- A. 根据物质反应的能量变化,可将化学反应分为放热反应和吸热反应
- B. 根据物质组成元素是否异同,可将物质分为单质和氧化物
- C. 根据水中含有可溶性钙、镁化合物的多少,可将地表水分为硬水和软水
- D. 根据物质溶解能力的大小,可将物质的溶解性分为易溶、可溶、微溶和难溶
7.关于如图所示微粒结构示意图的说法,正确的是( )
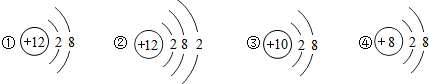

- A. ①③属于金属元素
- B. ①②属于同种元素
- C. ③④是阴离子
- D. ②④是稳定结构
8.下列相关排列顺序,正确的是( )
- A. Fe元素的质量分数由大到小:Fe、FeO、Fe3O4、Fe2O3
- B. 金属活动性由强到弱:Fe、Mg、Al、Cu
- C. 人类使用金属材料由早到晚:Fe2O3、Cu、Al、Fe
- D. 地壳中元素含量(质量分数)由多到少:O、Si、Fe、Al
9.把少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是( )
- A. 面粉
- B. 硫酸铜
- C. 氯化钠
- D. 植物油
10.下列有关物质的性质表述,正确的是( )
- A. O2、H2、CO、CO2、CH4都是无色,难溶于水的气体
- B. 木炭、铁粉、二氧化锰、氧化铁、氧化铜均为黑色固体
- C. 合金与纯金属相比,其熔点更高,硬度更大
- D. 物质的性质很大程度决定用途,但不是决定用途的唯一因素
11.N(NO2)3是科学家2011年发现的一种新型火箭推进剂的原料,下列有关说法正确的是( )
- A. N(NO2)3由三种元素组成
- B. N(NO2)3由4个氮原子和6个氧原子构成的
- C. N(NO2)3的相对分子质量152
- D. N(NO2)3中氮元素的质量分数为18.4%
12.下列实验设计不能达到目的的是( )
| A | B | C | D | |
| 实验 |  | 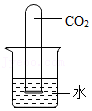 | 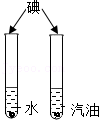 | 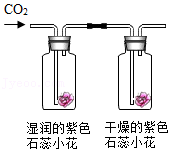 |
| 目的 | 验证铁钉锈蚀与氧气有关 | 验证CO2可溶于水 | 探究溶剂种类对溶解的影响 | 探究二氧化碳与水的反应 |
- A. A
- B. B
- C. C
- D. D
13.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是( )
- A. N2(O2)——通过灼热的氧化铜
- B. FeSO4溶液(CuSO4)——加入过量的铁粉,过滤
- C. Zn(Cu)——加入足量的稀盐酸,过滤、洗涤、干燥
- D. NaCl(泥沙)——过滤,蒸发、结晶
14.甲、乙、丙、丁为初中化学常见的物质,转化关系如图(反应条件已略去),下列说法不正确的是( )


- A. 甲一定是单质
- B. 乙一定是化合物
- C. 丙可能是水
- D. 丁可能是铜
15.用等质量相同表面积的镁条、等体积不同浓度的稀盐酸在一定条件下反应,实验结果如图所示。下列结论正确的是( )
①镁与盐酸的反应是放热反应
②b曲线对应的盐酸浓度较大
③盐酸浓度越大,反应速率越快
④单位时间内放出热量越多,反应速率越快
⑤装置内氢气的质量先增大,后减小
⑥两种情况最终产生氢气的质量可能相同

①镁与盐酸的反应是放热反应
②b曲线对应的盐酸浓度较大
③盐酸浓度越大,反应速率越快
④单位时间内放出热量越多,反应速率越快
⑤装置内氢气的质量先增大,后减小
⑥两种情况最终产生氢气的质量可能相同

- A. ①②③④
- B. ①③④⑤
- C. ①③④⑥
- D. ③④⑤⑥
16.资源是大自然赐予人类的礼物,是赖以生存和发展的物质基础。
(1)煤、石油、 等化石燃料是不可再生能源。乙醇汽油的开发与利用可适当地节省石油资源,请写出乙醇燃烧的化学方程式 。
(2)理解燃烧的本质,使化石燃料充分燃烧也是节约能源的一种方式。使燃料充分燃烧通常考虑两点:一是 ,二是燃料与空气要有足够大的接触面积。
(3)如图所示某同学将一燃着的蜡烛伸入盛有氢气的集气瓶内,当伸入其中时,蜡烛熄灭,慢慢取出后又燃烧。请分析蜡烛熄灭和重新燃烧的原因。
蜡烛熄灭的原因: 。重新燃烧的原因: 。
(4)下列措施有利于保护金属资源的是 。
A.防止金属资源腐蚀
B.金属回收再利用
C.有计划地合理开采
D.寻找金属代用品
(5)用2000t含Fe2O3 80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?(写出计算过程,计算结果保留1位小数)

(1)煤、石油、 等化石燃料是不可再生能源。乙醇汽油的开发与利用可适当地节省石油资源,请写出乙醇燃烧的化学方程式 。
(2)理解燃烧的本质,使化石燃料充分燃烧也是节约能源的一种方式。使燃料充分燃烧通常考虑两点:一是 ,二是燃料与空气要有足够大的接触面积。
(3)如图所示某同学将一燃着的蜡烛伸入盛有氢气的集气瓶内,当伸入其中时,蜡烛熄灭,慢慢取出后又燃烧。请分析蜡烛熄灭和重新燃烧的原因。
蜡烛熄灭的原因: 。重新燃烧的原因: 。
(4)下列措施有利于保护金属资源的是 。
A.防止金属资源腐蚀
B.金属回收再利用
C.有计划地合理开采
D.寻找金属代用品
(5)用2000t含Fe2O3 80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?(写出计算过程,计算结果保留1位小数)

17.某实验室的废水中含有大量AgNO3、Zn(NO3)2和Fe(NO3)2,化学兴趣小组欲从该废液中回收银,并得到副产品硫酸亚铁晶体。实验方案如图:

(1)固体甲中含有的物质是(填化学式) ;溶液乙中含有的物质是(填化学式) 。
(2)写出步骤①中反应的化学方程式: 。
(3)写出判断步骤①中加入A已过量的实验方案。

(1)固体甲中含有的物质是(填化学式) ;溶液乙中含有的物质是(填化学式) 。
(2)写出步骤①中反应的化学方程式: 。
(3)写出判断步骤①中加入A已过量的实验方案。
| 操作 | 现象和结论 |
18.根据下列实验装置回答问题。
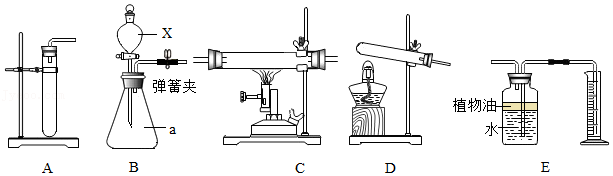
(1)写出装置图中标号仪器的名称:a 。
(2)A装置可用于常温下固体与液体间反应,写出在A装置内可发生反应的化学方程式: 。
(3)检查B装置气密性的操作是 ;若用B装置制取气体,则B与A相比的优点是 。
(4)C装置可用于固体与气体间的反应,如碳与二氧化碳反应,其化学方程式为 ,此处实验现象是 。
(5)用D、E装置组合可制取氨气(NH3),并收集、测量氨气的体积。氨气是一种无色、有刺激性气味的气体,极易溶于水。实验用加热氯化铵和氢氧化钙两种固体的混合物来制取氨气,同时生成氯化钙和水。则制取氨气的化学方程式为 ;影响此实验中氨气体积测量准确性的因素有 。
①装置气密性
②温度
③生成的水蒸气
④装置内原有空气
⑤排水的导管长短、高低

(1)写出装置图中标号仪器的名称:a 。
(2)A装置可用于常温下固体与液体间反应,写出在A装置内可发生反应的化学方程式: 。
(3)检查B装置气密性的操作是 ;若用B装置制取气体,则B与A相比的优点是 。
(4)C装置可用于固体与气体间的反应,如碳与二氧化碳反应,其化学方程式为 ,此处实验现象是 。
(5)用D、E装置组合可制取氨气(NH3),并收集、测量氨气的体积。氨气是一种无色、有刺激性气味的气体,极易溶于水。实验用加热氯化铵和氢氧化钙两种固体的混合物来制取氨气,同时生成氯化钙和水。则制取氨气的化学方程式为 ;影响此实验中氨气体积测量准确性的因素有 。
①装置气密性
②温度
③生成的水蒸气
④装置内原有空气
⑤排水的导管长短、高低
19.某无色气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的一种或几种,现将该气体依次通过如图所示装置。观察到:①A装置内未见浑浊现象;②D装置内无水硫酸铜变蓝(无水硫酸铜遇水变蓝);③最终收集到一种不能燃烧的干燥气体(假设每步反应都是完全的)。请回答下列问题:
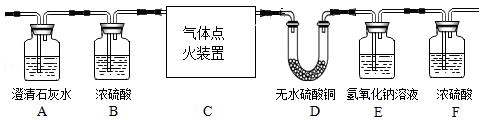
(1)由①可知原混合气体中肯定不含 ;
(2)由②可知原混合气体中一定含有 ;
(3)E装置的作用是 ;
(4)实验过程中记录的实验数据如下,并依据数据可推知原气体组成。
则该气体的成分为 。

(1)由①可知原混合气体中肯定不含 ;
(2)由②可知原混合气体中一定含有 ;
(3)E装置的作用是 ;
(4)实验过程中记录的实验数据如下,并依据数据可推知原气体组成。
| D装置总质量 | E装置总质量 | |
| 反应前 | 156.6g | 356.8g |
| 反应后 | 158.4g | 361.2g |
则该气体的成分为 。
20.如图是初中化学部分物质间相互转化关系图,“→”表示物质间存在转化关系,部分反应物、生成物或反应条件已略去,请结合关系图回答下列问题。
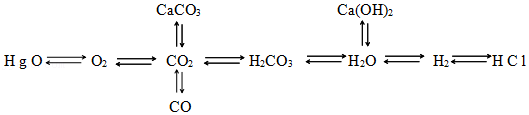
(1)由此关系图可推知水有 化学性质。
(2)在CO2→CO的反应中表现出CO2的 性。
(3)H2、CO都有可燃性和还原性,都可通过 反应(填基本反应类型)生成对应的氧化物。
(4)请写出下列物质间转化的化学方程式。
CaCO3→CO2: ;
Ca(OH)2→H2O: 。

(1)由此关系图可推知水有 化学性质。
(2)在CO2→CO的反应中表现出CO2的 性。
(3)H2、CO都有可燃性和还原性,都可通过 反应(填基本反应类型)生成对应的氧化物。
(4)请写出下列物质间转化的化学方程式。
CaCO3→CO2: ;
Ca(OH)2→H2O: 。
21.溶解度与速度、密度一样,都是控制某变量,度量另一变量,以表达事物固有属性。
(1)20℃时NaCl的溶解度为36g,其含义是 。
(2)影响固体溶解度大小的因素有 (填字母,下同)。
A.温度
B.压强
C.溶质、溶剂的种类
D.搅拌
F.颗粒大小
E.溶质、溶剂的质量
(3)影响固体物质溶解速度快慢的因素有 。
A.温度
B.搅拌
C.颗粒大小
D.振荡
(4)不同温度下,O2的溶解度随压强的变化如图1所示,图中t1对应的温度为40℃,则t2对应的温度 。
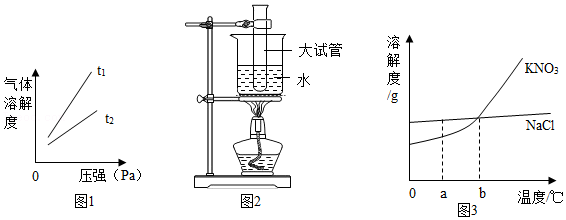
A.大于40℃
B.小于40%
C.无法确
某学生在教师的指导下完成KNO3溶解度的测定实验。
(5)步骤1:分别准确称取3.5g、1.5g、2.0g KNO3。加入药品后发现托盘天平指针偏向右边,则接下来的操作是 。
A.添加KNO3直至天平平衡
B.取出KNO3直至天平平衡
C.改变砝码、游码,直至天平平衡
D.重新调节平衡螺母至天平平衡
(6)步骤2:将3.5g KNO3放入大试管中,并用量筒量取10.0mL蒸馏水于试管内。注意量筒必须放平稳,视线要与液体 保持水平。
(7)步骤3:振荡大试管,发现有固体未溶解,于是用如图2所示方法进行水浴加热,使固体全部溶解,则此加热方法的优点是 。
步骤4:取出大试管,插入温度计,用玻璃棒轻轻搅拌并摩擦试管壁,同时观察温度计的读数。当刚有晶体析出时,立即记下此时的温度T1。
(8)步骤5:此时在大试管中再加入1.5g KNO3,重复步骤3、4,记录温度为T2;同样方法,再加入2.0g KNO3实验,记录温度为T3。则T3时KNO3的溶解度为 g。
实验交流与反思:
(9)交流1:判断溶液的饱和状态是溶解度测量的关键点。欲使接近饱和的KNO3溶液变为饱和溶液的三种方法是 。
(10)交流2:依据学生实验后绘制的图3溶解度曲线,下列说法正确的是 。
A.NaCl的溶解度小于KNO3的溶解度
B.分别将b℃时,两种物质的饱和溶液降温至a℃,KNO3溶液析出的晶体多
C.在a℃时若配制等质量的两物质的饱和溶液,KNO3所需的水量多
D.从含有少量NaCl的KNO3中提纯KNO3,可采用降温结晶的方法
(1)20℃时NaCl的溶解度为36g,其含义是 。
(2)影响固体溶解度大小的因素有 (填字母,下同)。
A.温度
B.压强
C.溶质、溶剂的种类
D.搅拌
F.颗粒大小
E.溶质、溶剂的质量
(3)影响固体物质溶解速度快慢的因素有 。
A.温度
B.搅拌
C.颗粒大小
D.振荡
(4)不同温度下,O2的溶解度随压强的变化如图1所示,图中t1对应的温度为40℃,则t2对应的温度 。

A.大于40℃
B.小于40%
C.无法确
某学生在教师的指导下完成KNO3溶解度的测定实验。
(5)步骤1:分别准确称取3.5g、1.5g、2.0g KNO3。加入药品后发现托盘天平指针偏向右边,则接下来的操作是 。
A.添加KNO3直至天平平衡
B.取出KNO3直至天平平衡
C.改变砝码、游码,直至天平平衡
D.重新调节平衡螺母至天平平衡
(6)步骤2:将3.5g KNO3放入大试管中,并用量筒量取10.0mL蒸馏水于试管内。注意量筒必须放平稳,视线要与液体 保持水平。
(7)步骤3:振荡大试管,发现有固体未溶解,于是用如图2所示方法进行水浴加热,使固体全部溶解,则此加热方法的优点是 。
步骤4:取出大试管,插入温度计,用玻璃棒轻轻搅拌并摩擦试管壁,同时观察温度计的读数。当刚有晶体析出时,立即记下此时的温度T1。
(8)步骤5:此时在大试管中再加入1.5g KNO3,重复步骤3、4,记录温度为T2;同样方法,再加入2.0g KNO3实验,记录温度为T3。则T3时KNO3的溶解度为 g。
实验交流与反思:
(9)交流1:判断溶液的饱和状态是溶解度测量的关键点。欲使接近饱和的KNO3溶液变为饱和溶液的三种方法是 。
(10)交流2:依据学生实验后绘制的图3溶解度曲线,下列说法正确的是 。
A.NaCl的溶解度小于KNO3的溶解度
B.分别将b℃时,两种物质的饱和溶液降温至a℃,KNO3溶液析出的晶体多
C.在a℃时若配制等质量的两物质的饱和溶液,KNO3所需的水量多
D.从含有少量NaCl的KNO3中提纯KNO3,可采用降温结晶的方法
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解