下载高清试卷
【2020-2021学年四川省成都市青羊区九年级(上)期末化学试卷】-第1页
试卷格式:2020-2021学年四川省成都市青羊区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2021年、四川试卷、成都市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷
扫码查看解析
试卷题目
1.下列物质中,属于溶液的是( )
- A. 糖水
- B. 牛奶
- C. 米粥
- D. 豆浆
2.某原子的原子核内有1个质子和2个中子,则该原子的核外电子数为( )
- A. 3
- B. 2
- C. 1
- D.
3.垃圾分类从你我他开始。易拉罐属于( )
- A.
 可回收物
可回收物 - B.
 有害垃圾
有害垃圾 - C.
 厨余垃圾
厨余垃圾 - D.
 其他垃圾
其他垃圾
4.乙醇俗称酒精,其完全燃烧的化学方程式为:C2H5OH+3O2
2CO2+3H2O,根据该化学方程式无法获取的信息是( )
| 点燃 |
- A. 反应物和生成物
- B. 反应所需条件
- C. 反应物的颜色和状态
- D. 生成物的分子个数比
5.下列化学符号正确的是( )
- A. 1个一氧化碳分子:Co
- B. 2个碳酸根离子:2CO32﹣
- C. 3个亚铁离子:3Fe3+
- D. 4个氢原子:2H2
6.化学与生活息息相关,下列说法不正确的是( )
- A. 家用电器着火,立即用水浇灭
- B. 炒菜时油锅着火,应立即盖上锅盖
- C. “钻木取火”的原理是通过摩擦生热使温度达到木材着火点
- D. 燃气灶火焰出现黄色,锅底出现黑色时,可增大灶具进风口
7.不同温度时,NaCl固体的溶解度如表所示。20℃时,将50g NaCl固体加入到盛有100g水的烧杯中,充分溶解得到溶液。下列说法正确的是( )
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
- A. 烧杯中溶液的质量为150g
- B. 烧杯中剩余固体的质量为14g
- C. 加入50g水,搅拌后烧杯中仍有剩余固体
- D. 升高温度能将烧杯中的饱和溶液变为不饱和溶液
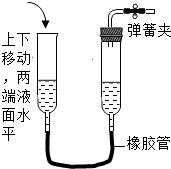
8.下列各图所示装置的气密性检查中,漏气的是( )
- A.
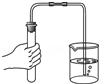
- B.
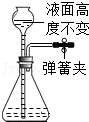
- C.
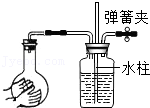
- D.
9.下表是元素周期表的一部分,则下列回答正确的是( )


- A. 12号元素的离子符号是Mg+2
- B. 氯原子的原子结构示意图是
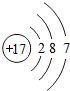
- C. 表中左边是非金属元素、右边是金属元素
- D. 硫元素的相对原子质量为16g
10.下列实验不能达到实验目的的是( )
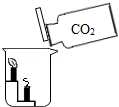 | 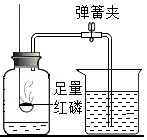 | 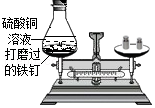 | 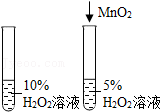 |
| A.验证二氧化碳的密度比空气大 | B.探究空气中氧气含量 | C.验证质量守恒定律 | D.探究反应物浓度对反应速率的影响 |
- A. A
- B. B
- C. C
- D. D
11.中国科学家成功将二氧化碳转化为乙烯(C2H4),其反应前后分子种类的微观示意图如图所示。下列说法不正确的是( )
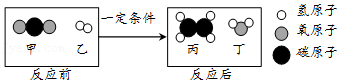

- A. 反应中原子种类没有改变
- B. 反应前后分子种类发生了改变
- C. 丙和丁中的氢元素全部来自于乙中
- D. 参加反应的甲与生成的丙质量比为11:7
12.如图所示装置可用于实验室制取某些气体,并能随开随用.下表中所选用的药品及制取的气体完全正确的是一组是( )
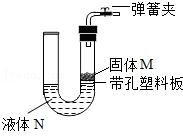
| 选项 | 选用药品 | 制取的气体 | |
| 固体M | 液体N | ||
| ① | 锌粒 | 稀硫酸 | 氢气 |
| ② | 碳酸钠 | 浓盐酸 | 二氧化碳 |
| ③ | 大理石 | 稀盐酸 | 二氧化碳 |
| ④ | 二氧化锰 | 过氧化氢 | 氧气 |

- A. ①
- B. ②
- C. ③
- D. ④
13.如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )
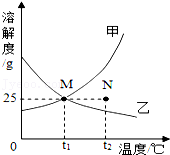

- A. 甲物质的溶解度随温度的升高而增大
- B. 在t1℃时,甲、乙两物质的溶解度相等
- C. 在 t2℃时,N点表示甲物质的不饱和溶液
- D. 在t1℃时,100g乙物质的饱和溶液中溶质的质量是25g
14.某密闭容器内有四种物质,在一定条件下充分反应。测得反应前后各物质质量如表。下列有关说法中不正确的是( )
A.a的值等于18
B.X是反应物
C.该反应属于分解反应
D.若Y和Z的相对分子质量之比为20:11,则Y和Z的化学计量系数(即化学方程式中化学式前的系数)之比为2:1
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 224 | 10 | 0 | 2 |
| 反应后质量/g | 2 | 170 | 44 | a |
A.a的值等于18
B.X是反应物
C.该反应属于分解反应
D.若Y和Z的相对分子质量之比为20:11,则Y和Z的化学计量系数(即化学方程式中化学式前的系数)之比为2:1
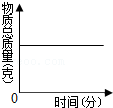
15.一定质量的木炭与过量氧气在密闭容器内加热使其充分反应。下图中能正确反映容器内有关的量随时间变化关系的图象是( )
- A.
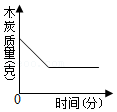
- B.
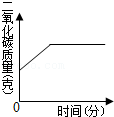
- C.
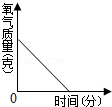
- D.
16.科技改变生活。
(1)氮气充入食品包装袋防腐,是因为 。
(2)宇航员太空行走时,需要“人造空气”供给呼吸。这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、还有二氧化碳。“人造空气”中供给呼吸的物质是 ,“人造空气”中氮气和空气中的氮气化学性质 (填“相同”或“不同”)。
(3)修建高铁过程中常用黑火药(含KNO3、S、C)进行工程爆破,黑火药爆炸时产生浓烟,推测该浓烟中含有K2S,从元素守恒角度说明理由 。
(4)最新研究表明,在光照条件下,利用Pt/TiO2为催化剂分解水可以得到过氧化氢和氢气,该反应的化学方程式为 。
(1)氮气充入食品包装袋防腐,是因为 。
(2)宇航员太空行走时,需要“人造空气”供给呼吸。这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、还有二氧化碳。“人造空气”中供给呼吸的物质是 ,“人造空气”中氮气和空气中的氮气化学性质 (填“相同”或“不同”)。
(3)修建高铁过程中常用黑火药(含KNO3、S、C)进行工程爆破,黑火药爆炸时产生浓烟,推测该浓烟中含有K2S,从元素守恒角度说明理由 。
(4)最新研究表明,在光照条件下,利用Pt/TiO2为催化剂分解水可以得到过氧化氢和氢气,该反应的化学方程式为 。
17.人类的生产生活离不开燃料。
(1)化石燃料包括天然气、煤和 ,天然气的主要成分是 。
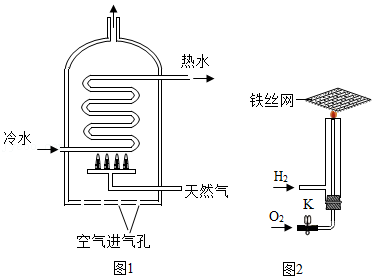
(2)家用燃气热水器的工作原理如图1所示,若“空气进气孔”被部分堵塞,导致天然气燃烧不充分,会产生的有毒气体是 。
(3)氢气属于清洁燃料,是因为 。工业上利用氢氧焰(氢气在氧气中燃烧所产生的高温火焰)切割金属。进行图2所示实验:关闭K,点燃氢气(已验纯),铁丝发红,不熔断;打开K,一段时间后,点燃氢气(已验纯),铁丝熔断。出现上述不同现象的原因是 。
(4)开发和利用新能源是解决能源问题的重要途径。图3利用了新能源的是 (填序号)。

(1)化石燃料包括天然气、煤和 ,天然气的主要成分是 。
(2)家用燃气热水器的工作原理如图1所示,若“空气进气孔”被部分堵塞,导致天然气燃烧不充分,会产生的有毒气体是 。
(3)氢气属于清洁燃料,是因为 。工业上利用氢氧焰(氢气在氧气中燃烧所产生的高温火焰)切割金属。进行图2所示实验:关闭K,点燃氢气(已验纯),铁丝发红,不熔断;打开K,一段时间后,点燃氢气(已验纯),铁丝熔断。出现上述不同现象的原因是 。
(4)开发和利用新能源是解决能源问题的重要途径。图3利用了新能源的是 (填序号)。


18.(1)果糖(C6H12O6)主要存在于蜂蜜、水果中,具有口感好、甜度高等优点。请回答:
①果糖分子中碳、氢、氧原子的个数比为 。
②果糖中氧元素质量分数的计算式为 。
(2)某潜水艇上有100人,如果每人每天消耗氧气为1.44kg,所需要的氧气全部由Na2O2与CO2反应来提供。根据化学方程式计算,每天总共需要Na2O2的质量是多少?
已知:2Na2O2+2CO2═2Na2CO3+O2。
①果糖分子中碳、氢、氧原子的个数比为 。
②果糖中氧元素质量分数的计算式为 。
(2)某潜水艇上有100人,如果每人每天消耗氧气为1.44kg,所需要的氧气全部由Na2O2与CO2反应来提供。根据化学方程式计算,每天总共需要Na2O2的质量是多少?
已知:2Na2O2+2CO2═2Na2CO3+O2。
19.高纯硅可用于制备硅半导体材料,其主要生产流程如图所示:
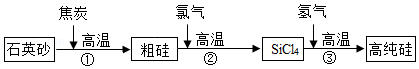
(1)①发生反应的化学方程式为SiO2+2C
Si+2CO↑,该反应中碳元素的化合价变化为零价→+2价,硅元素的化合价变化为 。
(2)②反应的基本反应类型为 (填“化合反应”或“分解反应”)。
(3)SiO2属于 (填序号)。
A. 纯净物
B. 化合物
C. 氧化物

(1)①发生反应的化学方程式为SiO2+2C
| 高温 |
(2)②反应的基本反应类型为 (填“化合反应”或“分解反应”)。
(3)SiO2属于 (填序号)。
A. 纯净物
B. 化合物
C. 氧化物
20.尿素[CO(NH2)2]是一种常用氮肥,如图是利用甲烷制尿素的主要流程: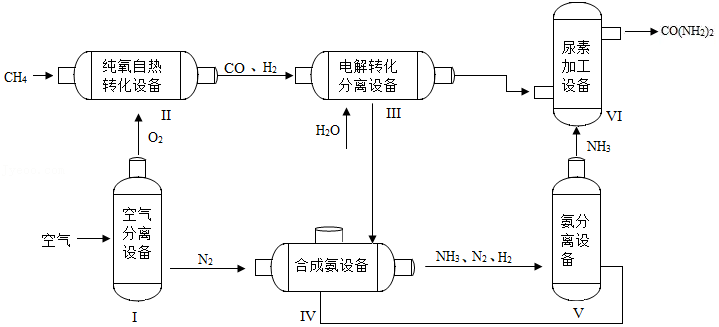
(1)设备Ⅲ中的反应在一定条件下进行,产生CO2和H2,该反应的化学方程式为 ,其中化合价升高的元素是 。
(2)设备Ⅵ中,参加反应的物质是 。
(3)设备Ⅴ中,可以循环利用的气体是 。

(1)设备Ⅲ中的反应在一定条件下进行,产生CO2和H2,该反应的化学方程式为 ,其中化合价升高的元素是 。
(2)设备Ⅵ中,参加反应的物质是 。
(3)设备Ⅴ中,可以循环利用的气体是 。
21.根据如图所示的实验回答问题。
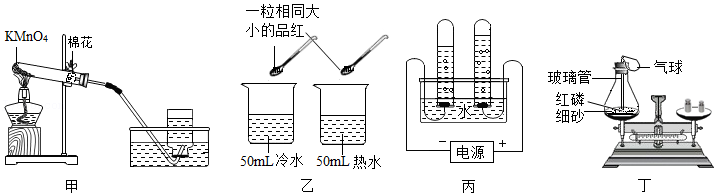
(1)甲中棉花的作用是 。
(2)乙的目的是研究品红分子在水中的运动速率与 的关系。
(3)丙是电解水实验,反应的化学方程式为 ;与电源正极相连的试管中产生的气体是 。
(4)丁是验证质量守恒定律。其中红磷燃烧的现象是 ;充分反应并冷却后,天平仍保持平衡,从微观的角度解释其原因 。

(1)甲中棉花的作用是 。
(2)乙的目的是研究品红分子在水中的运动速率与 的关系。
(3)丙是电解水实验,反应的化学方程式为 ;与电源正极相连的试管中产生的气体是 。
(4)丁是验证质量守恒定律。其中红磷燃烧的现象是 ;充分反应并冷却后,天平仍保持平衡,从微观的角度解释其原因 。
22.利用如图所示装置进行实验。
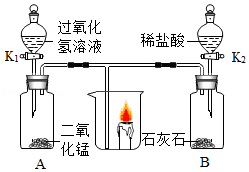
(1)打开K1,放入适量的过氧化氢溶液,关闭K1,观察到蜡烛 ;A中发生反应的化学方程式为 。
(2)为证明CO2在通常条件下不燃烧、也不支持燃烧,继续的操作是 。

(1)打开K1,放入适量的过氧化氢溶液,关闭K1,观察到蜡烛 ;A中发生反应的化学方程式为 。
(2)为证明CO2在通常条件下不燃烧、也不支持燃烧,继续的操作是 。
23.在利用红磷燃烧测定空气中氧气含量的实验中,用传感器记录集气瓶内氧气浓度随时间变化的情况,如图2所示。
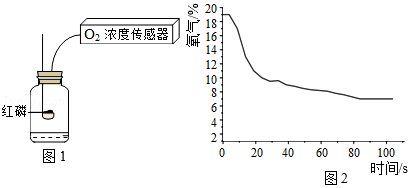
【进行实验】
活动1:证明红磷熄灭后,氧气还有剩余
【解释与结论】
(1)红磷燃烧的化学方程式为 。
(2)步骤Ⅰ中白磷始终不燃烧的原因是 。
(3)步骤Ⅱ中的现象①是 。
(4)实验中气球的作用是 。
活动2:探究影响剩余氧气浓度的因素
用图1装置进行实验,得到数据如表。
(5)通过对比右表中红磷和白磷的相关数据,可以得出影响剩余氧气浓度的因素可能是 。
(6)结合以上探究及实验数据,在“测定空气中氧气含量”的实验中,通常使用红磷而不用木炭的原因可能有 。

【进行实验】
活动1:证明红磷熄灭后,氧气还有剩余
| 实验装置 | 实验步骤 | 现象 | 结论 |
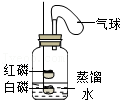 | Ⅰ.用高能激光笔照射燃烧匙中足量的红磷 | 红磷燃烧,放出大量热,一段时间后熄灭,白磷始终不燃烧 | 红磷熄灭后,氧气还有剩余 |
| Ⅱ.冷却后,将装有白磷的燃烧匙提出水面,用高能激光笔照射 | 白磷现象①________ |
【解释与结论】
(1)红磷燃烧的化学方程式为 。
(2)步骤Ⅰ中白磷始终不燃烧的原因是 。
(3)步骤Ⅱ中的现象①是 。
(4)实验中气球的作用是 。
活动2:探究影响剩余氧气浓度的因素
用图1装置进行实验,得到数据如表。
| 可燃物 | 白磷 | 红磷 | 木炭 |
| 着火点/℃ | 40 | 240 | 370 |
| 生成物状态 | 固态 | 固态 | 气态 |
| 剩余氧气浓度 | 3.1% | 7.0% | 14.0% |
(5)通过对比右表中红磷和白磷的相关数据,可以得出影响剩余氧气浓度的因素可能是 。
(6)结合以上探究及实验数据,在“测定空气中氧气含量”的实验中,通常使用红磷而不用木炭的原因可能有 。
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解