下载高清试卷
【2021-2022学年湖北省孝感市八校联谊九年级(上)月考化学试卷】-第1页
试卷格式:2021-2022学年湖北省孝感市八校联谊九年级(上)月考化学试卷.PDF
试卷热词:最新试卷、2022年、湖北试卷、孝感市试卷、化学试卷、九年级试卷、月考试卷、初中试卷
扫码查看解析
试卷题目
1.嫦娥五号执行的下列探月任务一定涉及化学变化的是( )
- A. 漫步月面
- B. 采集月壤
- C. 展示国旗
- D. 点火返航
2.下列实验基本操作,错误的是( )
- A.
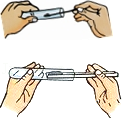 取
取 - B.
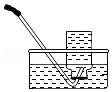 收
收 - C.
 称
称 - D.
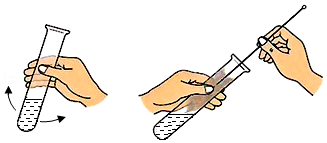 洗
洗
3.下列有关说法:( )
①CO2在空气中含量增多会加剧温室效应,属于空气污染物;
②为减少“水华”现象发生,提倡使用无磷洗衣粉;
③工厂加高烟囱有利于防治空气污染;
④使用含碳量低的物质生活就是“低碳”生活;
⑤过滤只能除去水中的不溶性杂质,无法除去可溶性杂质;
⑥为了节约用水,可以用工业废水直接浇灌农田;
⑦洁净的空气、自来水均属于混合物。正确的组合是
①CO2在空气中含量增多会加剧温室效应,属于空气污染物;
②为减少“水华”现象发生,提倡使用无磷洗衣粉;
③工厂加高烟囱有利于防治空气污染;
④使用含碳量低的物质生活就是“低碳”生活;
⑤过滤只能除去水中的不溶性杂质,无法除去可溶性杂质;
⑥为了节约用水,可以用工业废水直接浇灌农田;
⑦洁净的空气、自来水均属于混合物。正确的组合是
- A. ②⑤⑦
- B. ①③④
- C. ③④⑦
- D. ②④⑥
4.下列关于化学用语的说法,错误的一项是( )
- A. FeCl2读作氯化亚铁;SO2读作二氧化硫
- B. 3H只有微观意义;C60表示60个碳原子
- C. NH4NO3中,氮元素的化合价不相同
- D. 2Mg+O22MgO,可读作每48份质量的镁与32份质量的氧气完全反应,生成80份质量的氧化镁
点燃
5.将氯化氢转化为氯气的技术是当今研究的热点,一定条件下,甲与乙反应生成丙和丁,相关物质的分子模型如表所示(其中: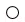 表示氢原子,
表示氢原子, 表示氧原子,
表示氧原子, 表示氯原子),下列说法正确的是( )
表示氯原子),下列说法正确的是( )
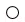 表示氢原子,
表示氢原子, 表示氧原子,
表示氧原子, 表示氯原子),下列说法正确的是( )
表示氯原子),下列说法正确的是( )| 物质 | 甲 | 乙 | 丙 | 丁 |
| 分子模型 |  |  |  |  |
- A. 该反应体现了甲的氧化性
- B. 表中涉及两种含氧化合物
- C. 该反应的甲、乙的质量比为73:36
- D. 该反应中所有元素的化合价均发生了改变
6.分析和推理是化学学习常用的方法,以下推理正确的是( )
- A. 点燃氢气前要检验氢气的纯度,所以点燃任何可燃性气体前一定要检验气体的纯度
- B. 燃烧都伴随有发光、放热现象,有发光、放热现象的变化也一定是燃烧
- C. 化合物是由两种或两种以上元素组成的纯净物,则两种或两种以上元素组成的物质一定是化合物
- D. 稀有气体元素原子最外层电子数为8,最外层电子数为8的粒子一定是稀有气体元素的原子
7.已知H2S是一种生命体系信号分子,它在O2中燃烧的化学方程式是2H2S+3O2
2X+2H2O。下列说法正确的是( )
| 点燃 |
- A. 该反应过程中放出热量
- B. H2S中硫元素的化合价是﹣1
- C. 该反应体现O2的可燃性
- D. 大量X进入空气不会引起酸雨
8.下列实验方案合理的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去CuO中少量的C粉 | 将混合物隔绝空气高温加热 |
| B | 鉴别H2O和H2O2溶液 | 取样,分别加入少量MnO2观察现象 |
| C | 将硬水软化 | 加肥皂水 |
| D | 检验二氧化碳是否收集满 | 将燃着的木条伸入集气瓶中 |
- A. A
- B. B
- C. C
- D. D
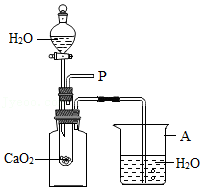
9.小张发现养鱼师傅向鱼塘中撒一种微黄色的过氧化钙(CaO2)固体,鱼塘中立即产生大量气泡,为探究过氧化钙与水反应产生了何种气体,做了如下实验,步骤如下:
Ⅰ.检查装置气密性,装置气密性良好
Ⅱ.向试管中加入一定量的过氧化钙,向烧杯和分液漏斗中加足量水,连接好装置
Ⅲ.打开分液漏斗活塞,把带火星的木条放在P处,观察现象
下列有关说法正确的个数为( )
①若观察到P处带火星木条复燃,则证明过氧化钙与水反应有氧气生成
②若P处带火星木条复燃,则可以证明氧气具有可燃性
③若观察到A中导管口有气泡冒出,则证明过氧化钙与水反应放热,使瓶内压强增大,瓶内气体受热膨胀而从A中导管口逸出
④若实验室用过氧化钙与水反应制取氧气,其发生装置与过氧化氢溶液制氧气相同
Ⅰ.检查装置气密性,装置气密性良好
Ⅱ.向试管中加入一定量的过氧化钙,向烧杯和分液漏斗中加足量水,连接好装置
Ⅲ.打开分液漏斗活塞,把带火星的木条放在P处,观察现象
下列有关说法正确的个数为( )
①若观察到P处带火星木条复燃,则证明过氧化钙与水反应有氧气生成
②若P处带火星木条复燃,则可以证明氧气具有可燃性
③若观察到A中导管口有气泡冒出,则证明过氧化钙与水反应放热,使瓶内压强增大,瓶内气体受热膨胀而从A中导管口逸出
④若实验室用过氧化钙与水反应制取氧气,其发生装置与过氧化氢溶液制氧气相同

- A. 1个
- B. 2个
- C. 3个
- D. 4个
10.某过氧化氢溶液中氧元素的质量分数为90%,加入二氧化锰充分反应后,过滤得135g液体,则生成氧气的质量为( )
- A. 60.75g
- B. 10g
- C. 15g
- D. 121.5g
11.化学基础与常识
(1)地壳中含量最多的金属元素是 (用元素符号表示)。
(2)硫原子和氮原子属于不同种元素的本质原因是 。
(3)利用活性炭的 可以有效地除去冰箱异味。
(4)乙醇(化学式为C2H5OH)分子中碳、氢、氧的原子个数比为 。
(5)“长征五号”运载火箭采用液氢作为燃料,我国科研团队研制的低温合成催化剂STSO颗粒,大大降低了太阳能分解水的成本。对该制氢反应描述正确的是 (填字母序号)。
A.太阳能转化为化学能
B.产生的氢气被压缩成液态后分子体积减小
C.反应过程中分子种类改变,原子种类不变
D.产生的氢气与氧气体积之比为1:2
(6)“天和”号核心舱的太阳能电池翼由砷化镓材料制成。如图是镓、砷原子的结构示意图,x= ,请写出砷化镓的化学式 。

(1)地壳中含量最多的金属元素是 (用元素符号表示)。
(2)硫原子和氮原子属于不同种元素的本质原因是 。
(3)利用活性炭的 可以有效地除去冰箱异味。
(4)乙醇(化学式为C2H5OH)分子中碳、氢、氧的原子个数比为 。
(5)“长征五号”运载火箭采用液氢作为燃料,我国科研团队研制的低温合成催化剂STSO颗粒,大大降低了太阳能分解水的成本。对该制氢反应描述正确的是 (填字母序号)。
A.太阳能转化为化学能
B.产生的氢气被压缩成液态后分子体积减小
C.反应过程中分子种类改变,原子种类不变
D.产生的氢气与氧气体积之比为1:2
(6)“天和”号核心舱的太阳能电池翼由砷化镓材料制成。如图是镓、砷原子的结构示意图,x= ,请写出砷化镓的化学式 。

12.“垃圾是放错的资源”。碘循环工艺不仅能吸收SO2,减少环境污染,而且还可以得到仅含一种元素的化工原料X,流程如图所示:
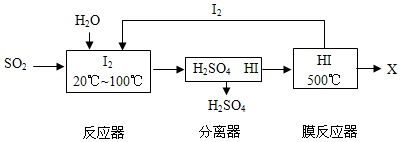
(1)流程中可循环利用的物质是 。
(2)膜反应器中发生的是分解反应,X的化学式是 。
(3)反应器中发生反应的化学方程式为 。

(1)流程中可循环利用的物质是 。
(2)膜反应器中发生的是分解反应,X的化学式是 。
(3)反应器中发生反应的化学方程式为 。
13.依据表中的元素回答下列问题
(1)写出一种常见的酸的化学式 。
(2)A、B、C、D、E都是由以上元素组成的初中化学常见物质,其中B、C的分子都由相同两种原子构成,且常温下均为液体;自然界中,绿色植物可实现D→E的转化。它们之间的转化关系如图所示(部分反应物生成物反应条件已略去,“→”表示物质间的转化关系)
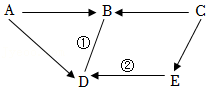
①C、D化学式分别为:C ,D 。
②若A为石灰石的主要成分,写出由A→D的反应方程式 。
③图中反应②一定属于 反应。(填“化合“、”氧化“或”分解“)
| 元素名称 | 碳 | 氢 | 氧 | 氯 | 钙 |
| 元素符号 | C | H | O | Cl | Ca |
(1)写出一种常见的酸的化学式 。
(2)A、B、C、D、E都是由以上元素组成的初中化学常见物质,其中B、C的分子都由相同两种原子构成,且常温下均为液体;自然界中,绿色植物可实现D→E的转化。它们之间的转化关系如图所示(部分反应物生成物反应条件已略去,“→”表示物质间的转化关系)

①C、D化学式分别为:C ,D 。
②若A为石灰石的主要成分,写出由A→D的反应方程式 。
③图中反应②一定属于 反应。(填“化合“、”氧化“或”分解“)
14.氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中制备KClO3的化学方程式为3Cl2+6KOH
5KCl+KClO3+3H2O。若21.3克Cl2完全参加反应,可制得多少克的KClO3?
| △ |
15.如图是实验室制取气体常用的部分实验装置,请回答下列问题:
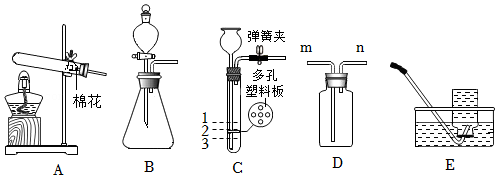
(1)用装置A制备O2,则A中发生反应的化学方程式为 。
(2)实验室制取CO2,若用装置C作发生装置,关闭弹簧夹,反应停止后,液面应位于 (填“1”、“2”或“3”)处,若用装置D收集二氧化碳,气体应从 (填“m”或“n”)端进入。
(3)实验室可选用B和E组合制取氢气,据此推断下列说法正确的是 。
A. 制取氢气的药品都是液体
B. 氢气密度比空气大
C. 氢气不与水反应
D. 制取氢气在常温下进行

(1)用装置A制备O2,则A中发生反应的化学方程式为 。
(2)实验室制取CO2,若用装置C作发生装置,关闭弹簧夹,反应停止后,液面应位于 (填“1”、“2”或“3”)处,若用装置D收集二氧化碳,气体应从 (填“m”或“n”)端进入。
(3)实验室可选用B和E组合制取氢气,据此推断下列说法正确的是 。
A. 制取氢气的药品都是液体
B. 氢气密度比空气大
C. 氢气不与水反应
D. 制取氢气在常温下进行
16.“控制变量”是科学探究实验中一种常见的实验手段,黑色固体碳(C)和黑色固体氧化铜(CuO)在温度较高时能反应生成红色的铜和二氧化碳气体,化学小组想要节约药品且尽快完成实验,于是对反应条件进行探究,实验数据如表:
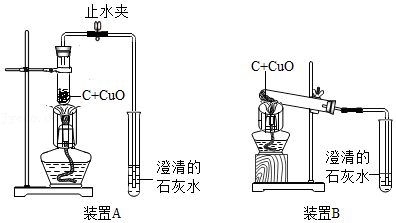
(1)实验过程中可以观察到澄清石灰水会 (填实验现象)。
(2)根据表格中信息:对比实验1和2,说明装置 (填“A”或“B”)更适合该实验。对比实验1和 ,说明粉末状药品反应更快,其原因可能是 (填序号)。分析表格,碳和氧化铜最适当的质量比为 (填最简整数比)。
A.碳粉质量比越大反应越快
B.物质接触越充分反应越快
C.温度越高反应越快
(3)实验刚开始时,装置左侧试管内还未出现红色固体,右侧试管中澄清石灰水却变化明显,请你写出左侧试管内可能发生的化学方程式 。
| 序号 | 装置 | 药品 | 反应完成耗时 |
| 1 | A | 碳(粉末)0.1g+氧化铜1.2g | 120s |
| 2 | B | 碳(粉末)0.1g+氧化铜1.2g | 560s |
| 3 | A | 碳(粉末)0.1g+氧化铜1.2g | 480s |
| 4 | A | 碳(粉末)0.12g+氧化铜1.2g | 110s |
| 5 | A | 碳(粉末)0.15g+氧化铜1.2g | 110s |

(1)实验过程中可以观察到澄清石灰水会 (填实验现象)。
(2)根据表格中信息:对比实验1和2,说明装置 (填“A”或“B”)更适合该实验。对比实验1和 ,说明粉末状药品反应更快,其原因可能是 (填序号)。分析表格,碳和氧化铜最适当的质量比为 (填最简整数比)。
A.碳粉质量比越大反应越快
B.物质接触越充分反应越快
C.温度越高反应越快
(3)实验刚开始时,装置左侧试管内还未出现红色固体,右侧试管中澄清石灰水却变化明显,请你写出左侧试管内可能发生的化学方程式 。
查看全部题目