下载高清试卷
【2022年贵州省黔东南州八校联盟中考化学一模试卷】-第1页
试卷格式:2022年贵州省黔东南州八校联盟中考化学一模试卷.PDF
试卷热词:最新试卷、2022年、贵州试卷、黔东南苗族侗族自治州试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.下列过程中发生物理变化的是( )
- A. 可燃冰燃烧
- B. 铁钉生锈
- C. 矿石粉碎
- D. 光合作用
2.图中的实验方法或操作正确的是( )
- A.
 倾倒液体
倾倒液体 - B.
 振荡试管
振荡试管 - C.
 尾气处理
尾气处理 - D.
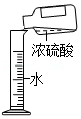 稀释浓硫酸
稀释浓硫酸
3.生活中处处有化学,下列说法中不合理的是( )
- A. 用食醋可以除去水壶中的水垢
- B. 用肥皂水涂抹蚊子叮咬处,可以减轻痛痒
- C. 用洗洁精清洗餐具,可以除去油污
- D. 油锅着火时,可以用水浇灭
4.分类是学习和研究化学的一种常见方法,下列分类正确的是( )
- A. 混合物:空气、溶液、冰水混合物
- B. 氧化物:氧化钙、过氧化钠、五氧化二磷
- C. 复合肥:硝酸钾、硫酸氢钾、氯化铵
- D. 碱类:火碱、纯碱、氢氧化钙
5.交警常用装备重铬酸钾(K2Cr2O7)的仪器监测司机是否酒后开车,因为酒中的乙醇分子可以使橙红色的重铬酸钾变成绿色的硫酸铬[Cr2(SO4)3],重铬酸钾和硫酸铬中的铬元素的化合价依次为( )
- A. +3,+5
- B. +5,+3
- C. +3,+6
- D. +6,+3
6.在一个密闭容器内有甲、乙、丙、丁四种物质,一定条件下进行反应,反应前后物质的质量如表
下列说法正确的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/克 | 40 | 50 | 10 | 30 |
| 反应后的质量/克 | 待测 | 90 | 10 | 0 |
下列说法正确的是( )
- A. 反应后甲的质量为零
- B. 该反应一定是化合反应
- C. 丙一定是该反应的催化剂
- D. 化学反应中甲:乙:丁的质量比为10:90:30
7.在Cu(NO3)2、Mg(NO3)2和AgNO3混合溶液中,加入一定量的铁粉充分反应后过滤。下列说法正确的是( )
- A. 滤渣中一定含有Cu、Ag
- B. 滤渣中一定含有Ag
- C. 滤液中一定不含AgNO3
- D. 滤液中可能含有Mg(NO3)2、Fe(NO3)2
8.下列除去杂质的方法中,合理的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | HCl | 通入氢氧化钠溶液中 |
| B | NaCl | CaCl2 | 加入过量的碳酸钠溶液并过滤,向滤液中再加入适量的稀盐酸 |
| C | 铁粉 | 铜粉 | 加入适量的稀硫酸,过滤 |
| D | CaCO3 | Na2CO3 | 加入适量的稀盐酸 |
- A. A
- B. B
- C. C
- D. D
9.请用H、O、Cl、Na、Fe五种元素中的一种或几种,按要求完成下列各题:
(1)写出符合下列要求的化学符号;
①两个氢原子 ;②五个铁离子 。
(2)写出符合下列要求物质的化学式:
①能使带火星木条复燃的气体 ;②可用于除去铁锈的酸 。
(3)请用上述元素中一种或几种组成的物质,写出符合下列要求的一根化学方程式:
①只有单质生成的分解反应 ;
②有沉淀生成的复分解反应 。
(1)写出符合下列要求的化学符号;
①两个氢原子 ;②五个铁离子 。
(2)写出符合下列要求物质的化学式:
①能使带火星木条复燃的气体 ;②可用于除去铁锈的酸 。
(3)请用上述元素中一种或几种组成的物质,写出符合下列要求的一根化学方程式:
①只有单质生成的分解反应 ;
②有沉淀生成的复分解反应 。
10.化学与人类生活、生产活动息息相关。根据所学化学知识回答下列问题:
(1)生活中常用 来区分硬水和软水。
(2)人的胃液里含有适量的 (填名称),可以帮助消化。
(3)食用“加铁酱油”可预防贫血,其中的“铁”是指 (填“元素”或“原子”)。
(4)厨房油锅着火,盖上锅盖可以立即灭火,其原理是 。
(1)生活中常用 来区分硬水和软水。
(2)人的胃液里含有适量的 (填名称),可以帮助消化。
(3)食用“加铁酱油”可预防贫血,其中的“铁”是指 (填“元素”或“原子”)。
(4)厨房油锅着火,盖上锅盖可以立即灭火,其原理是 。
11.如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
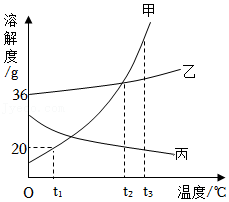
(1)t1℃时将3克的甲物质放入到10克的水中,所得溶液的溶质质量分数为 。(精确到0.1%)
(2)把t1℃丙的饱和溶液升温至t3℃,丙溶液的溶质质量分数 (填“变大”“不变”或“变小”)。
(3)若把t3℃时甲、乙、丙物质的饱和溶液分别降温到t1℃时,则三种溶液的溶质质量分数由小到大的顺序是 。
(4)当温度t的取值范围在 ℃时,甲的溶解度大于乙的溶解度。

(1)t1℃时将3克的甲物质放入到10克的水中,所得溶液的溶质质量分数为 。(精确到0.1%)
(2)把t1℃丙的饱和溶液升温至t3℃,丙溶液的溶质质量分数 (填“变大”“不变”或“变小”)。
(3)若把t3℃时甲、乙、丙物质的饱和溶液分别降温到t1℃时,则三种溶液的溶质质量分数由小到大的顺序是 。
(4)当温度t的取值范围在 ℃时,甲的溶解度大于乙的溶解度。
12.下列A~H都是初中常见的物质。已知A为实验室常用的燃料酒精,F是常用于改良酸性土壤的一种碱,它们之间的转化关系如图所示:
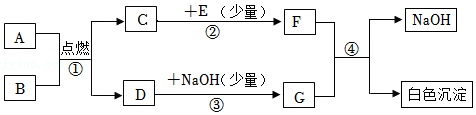
(1)固体D俗称 ,可用于人工降雨、制造舞台云雾。
(2)写出反应②的化学方程式 ,其基本反应类型为 反应。
(3)写出F+G反应的化学方程式: 。

(1)固体D俗称 ,可用于人工降雨、制造舞台云雾。
(2)写出反应②的化学方程式 ,其基本反应类型为 反应。
(3)写出F+G反应的化学方程式: 。
13.通过对化学的学习,你已掌握了实验室制取气体的有关知识,请结合图回答有关问题:

(1)写出图中标号仪器的名称:② ;
(2)用加热高锰酸钾的方法制取氧气,反应的化学方程式是 ,反应的发生装置和收集装置是 (填字母编号);
(3)用B装置制取二氧化碳气体,反应的化学方程式是 ,应选用的收集装置是 (填字母编号),选择的理由是 ;
(4)实验室常用锌粒和稀硫酸反应制取氢气。若用C装置制取氢气,该装置的优点是 。

(1)写出图中标号仪器的名称:② ;
(2)用加热高锰酸钾的方法制取氧气,反应的化学方程式是 ,反应的发生装置和收集装置是 (填字母编号);
(3)用B装置制取二氧化碳气体,反应的化学方程式是 ,应选用的收集装置是 (填字母编号),选择的理由是 ;
(4)实验室常用锌粒和稀硫酸反应制取氢气。若用C装置制取氢气,该装置的优点是 。
14.氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知:氢化钙(CaH2)遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的CaH2 加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液
【提出问题】滤液中溶质的成分是什么?
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
(1)经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因 。
【实验验证】
(2)猜想 不成立;
(3) 。
【反思与拓展】
(4)写出氢化钙(CaH2)与水反应的化学方程式 。
(5)若向NH4Cl的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和 。
(6)登山运动员携带CaH2作为能源提供剂与携带氢气相比,其优点是 (写一条即可)。
【提出问题】滤液中溶质的成分是什么?
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
(1)经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因 。
【实验验证】
| 实验 | 现象 | 结论 |
| (2)取少量滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想________不成立 |
| (3)另取少量滤液,向其中加入足量稀盐酸 | ________ | 猜想三成立 |
(2)猜想 不成立;
(3) 。
【反思与拓展】
(4)写出氢化钙(CaH2)与水反应的化学方程式 。
(5)若向NH4Cl的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和 。
(6)登山运动员携带CaH2作为能源提供剂与携带氢气相比,其优点是 (写一条即可)。
15.某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示。求:

(1)铜锌合金中,Zn的质量分数是 。
(2)所用稀硫酸溶液中溶质的质量分数是多少?

(1)铜锌合金中,Zn的质量分数是 。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解