下载高清试卷
【2022年江苏省泰州市高港区中考化学一模试卷】-第1页
试卷格式:2022年江苏省泰州市高港区中考化学一模试卷.PDF
试卷热词:最新试卷、2022年、江苏试卷、泰州市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.化学帮助我们正确认识物质,下列说法正确的是( )
- A. 高层住房着火时,打开所有门窗大声呼救
- B. 厨房燃气泄漏,立即打开油烟机排气
- C. 为延长食品保质期,可添加适量小苏打
- D. 自然条件下难以降解的塑料,会造成白色污染
2.下列物质由离子直接构成的是( )
- A. 氢氧化钠
- B. 金刚石
- C. 铁丝
- D. 蔗糖
3.下列变化中,属于物理变化的是( )
- A. 工业制二氧化碳
- B. 煤的干馏
- C. 洗洁精去油污
- D. 钢铁生锈
4.下列有关“粗盐的初步提纯”的实验操作不符合规范要求的是( )
- A.
 称量
称量 - B.
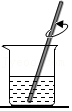 溶解
溶解 - C.
 过滤
过滤 - D.
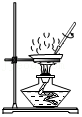 蒸发
蒸发
5.下列化学用语正确的是( )
- A. 氦气:He2
- B. 2个锰酸根离子:2MnO4﹣
- C. 水银:Ag
- D. 氢氧化铝:AI(OH)3
6.下列实验现象的描述正确的是( )
- A. 向少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝
- B. 将SO2气体通入稀高锰酸钾溶液中,溶液由浅紫红色逐渐变成无色
- C. 细铁丝在氧气中燃烧,火星四射,生成四氧化三铁
- D. 向葡萄糖溶液中加入新制氢氧化铜,加热至沸,产生黑色沉淀
7.如图为硒元素在周期表中的信息及原子结构示意图,下列说法错误的是( )


- A. x=34
- B. 硒元素属于非金属元素
- C. 硒原子在化学变化中易得到电子形成Se2+
- D. 硒元素的相对原子质量为78.96
8.从深海鱼油中提取出来的一种不饱和脂肪酸被称为“脑黄金”,它的化学式为C26H40O2,下列关于“脑黄金”说法正确的是( )
- A. 脑黄金是一种有机化合物
- B. 脑黄金分子是由碳、氢、氧三种元素组成
- C. 脑黄金中碳、氢、氧元素质量比为:13:20:1
- D. 脑黄金中氢元素质量分数最小
9.下列关于水的叙述错误的是( )
- A. 水是常用的溶剂
- B. 净水时用活性炭杀菌消毒
- C. 用肥皂水区分硬水和软水
- D. 电解水正极产生的气体具有助燃性
10.科学家设计了“人造树叶”模拟光合作用,如图是其反应的装置和微观示意图,下列说法错误的是( )
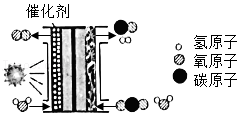

- A. 该过程实现了太阳能向化学能转化
- B. 反应前后催化剂的化学性质和质量不变
- C. 反应前后分子和原子数目均不改变
- D. 该反应的化学方程式为CO2+H2OCO+H2+O2
催化剂 光照
11.下列有关物质的检验、鉴别、除杂或分离等实验方案不合理的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别羊毛和棉花 | 灼烧,闻气味 |
| B | 检验废水中是否含有SO42﹣ | 滴加BaCl2溶液 |
| C | 除去NaCl溶液中混有的CuSO4 | 加入适量Ba(OH)2溶液,过滤 |
| D | 分离KCl和MnO2固体 | 溶解,过滤,洗涤干燥,蒸发结晶 |
- A. A
- B. B
- C. C
- D. D
12.逻辑推理是化学学习常用的思维方法,下列推理正确的是( )
- A. 碱性溶液能使酚酞试液变红,能使酚酞试液变红的溶液一定显碱性
- B. 酸雨的pH小于7,因此pH小于7的雨水一定是酸雨
- C. 化合物中有多种元素,所以含多种元素的物质是化合物
- D. 同种元素原子的质子数相同,所以质子数相同的原子一定属于同种元素
13.如图是A、B、C三种固体物质的溶解度曲线。以下说法正确的是( )
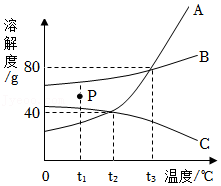

- A. t2℃时,将20gA物质加入到50g水中充分搅拌、溶解后,所得溶液质量是70g
- B. 图中P点所表示的B物质的溶液为饱和溶液
- C. A物质中混有少量的B物质,可采用蒸发结晶的方法提纯A物质
- D. 将t3℃时A、B、C三种物质的饱和溶液分别降温到t2℃(忽略水的蒸发)三种溶液的溶质质量分数由大到小的顺序是B>A=C
14.小明将未经砂纸打磨的铝条放入盛有足量稀盐酸的密闭容器中,用压强传感器测得容器内压强和反应时间的变化曲线如图所示,下列分析正确的是( )
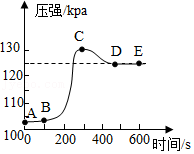

- A. AB段表示铝与稀盐酸反应
- B. 铝与稀盐酸反应是放热反应
- C. CD段压强减小只和温度变化有关
- D. 盐酸的浓度:C点>D点=E点
15.将20g铜与碳的混合物在氧气中充分灼烧后,冷却,称重,发现反应后的固体质量仍为20g,则原混合物中碳的质量分数为( )
- A. 10%
- B. 16%
- C. 20%
- D. 24%
16.化学与社会发展、生产生活密切相关。
(1)“沉睡三千年,一醒惊天下!”三星堆青铜器出土后立刻惊动了世界。青铜属于 (填“复合”“有机高分子”或“金属”)材料。
(2)《汉代古火井碑序》记载:“诸葛丞相躬莅视察,改进技法,刳斑竹以导气(气指天然气),引井火以煮盐”,请用化学方程式表示天然气燃烧的原理 。
(3)食醋(含醋酸)、精盐(NaCl)、碱面(Na2CO3)、蔗糖(C12H22O11)都是厨房常备物品。用碱性溶液浸泡蔬菜可降低蔬菜残留农药的毒性,因此,在厨房中浸泡新鲜蔬菜时,可加入适量的 。食用过量的醋会引起钙流失,青少年缺乏钙元素会导致 病。
(4)对于二氧化碳的排放,我国提出力争于2030年前达到峰值,于2060年前实现碳中和。“碳捕捉与封存”是我国的一项先进技术,二氧化碳气体能被压缩是因为 。被封存的二氧化碳有许多用途,请写出一条: 。
(1)“沉睡三千年,一醒惊天下!”三星堆青铜器出土后立刻惊动了世界。青铜属于 (填“复合”“有机高分子”或“金属”)材料。
(2)《汉代古火井碑序》记载:“诸葛丞相躬莅视察,改进技法,刳斑竹以导气(气指天然气),引井火以煮盐”,请用化学方程式表示天然气燃烧的原理 。
(3)食醋(含醋酸)、精盐(NaCl)、碱面(Na2CO3)、蔗糖(C12H22O11)都是厨房常备物品。用碱性溶液浸泡蔬菜可降低蔬菜残留农药的毒性,因此,在厨房中浸泡新鲜蔬菜时,可加入适量的 。食用过量的醋会引起钙流失,青少年缺乏钙元素会导致 病。
(4)对于二氧化碳的排放,我国提出力争于2030年前达到峰值,于2060年前实现碳中和。“碳捕捉与封存”是我国的一项先进技术,二氧化碳气体能被压缩是因为 。被封存的二氧化碳有许多用途,请写出一条: 。
17.A~I是初中化学常见的物质,互相直接能发生下列反应(反应条件均未标注)
①A+B→C+D ②B+E→F+G ③A+H→E+I ④C+E→F
其中A是一种红棕色粉末,B是胃酸的主要成分,E是应用最广泛的金属,F和C的元素组成相同,H和I元素组成相同,反应③是高炉炼铁的主要反应。请回答下列问题:
(1)写出B的化学式 ;写出反应②的基本反应类型 。
(2)写出反应①的现象 。
(3)写出下列反应的化学方程式:
反应③ ;反应④ 。
①A+B→C+D ②B+E→F+G ③A+H→E+I ④C+E→F
其中A是一种红棕色粉末,B是胃酸的主要成分,E是应用最广泛的金属,F和C的元素组成相同,H和I元素组成相同,反应③是高炉炼铁的主要反应。请回答下列问题:
(1)写出B的化学式 ;写出反应②的基本反应类型 。
(2)写出反应①的现象 。
(3)写出下列反应的化学方程式:
反应③ ;反应④ 。
18.如图1是实验室常用的部分实验装置,请回答下列问题:
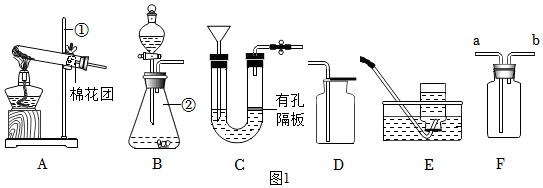
(1)仪器名称:① ,② 。
(2)用高锰酸钾制氧气,可选用的发生装置是 。(选填序号),反应化学方程式为 。若用E来收集氧气,收集完毕的操作顺序是 (填写序号顺序)。
①盖上玻璃片 ②正放在实验台上 ③取出集气瓶
(3)实验室制CO2的反应化学方程式为 ,为方便控制反应的发生和停止,应选择的发生装置是 (选填序号);如果用F装置收集CO2,验满的操作是 。
(4)FeS2和O2在加热条件下可反应生成SO2,图2是实验室利用FeS2制取SO2的装置。

①装置H中浓硫酸的作用是 。
②装置J用于收集SO2,说明SO2气体的密度 (选“小于”或“大于”)空气。
③用化学方程式表示实验中NaOH溶液的作用 。

(1)仪器名称:① ,② 。
(2)用高锰酸钾制氧气,可选用的发生装置是 。(选填序号),反应化学方程式为 。若用E来收集氧气,收集完毕的操作顺序是 (填写序号顺序)。
①盖上玻璃片 ②正放在实验台上 ③取出集气瓶
(3)实验室制CO2的反应化学方程式为 ,为方便控制反应的发生和停止,应选择的发生装置是 (选填序号);如果用F装置收集CO2,验满的操作是 。
(4)FeS2和O2在加热条件下可反应生成SO2,图2是实验室利用FeS2制取SO2的装置。

①装置H中浓硫酸的作用是 。
②装置J用于收集SO2,说明SO2气体的密度 (选“小于”或“大于”)空气。
③用化学方程式表示实验中NaOH溶液的作用 。
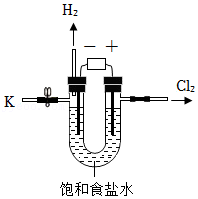
19.某兴趣小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣。在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验。
(一)电解饱和食盐水可以制得氢氧化钠、氯气(C12)和氢气,进而生产具有消毒、漂白作用的“84”消毒液。
(1)实验过程中与负极相连的导管口周围严禁明火,其原因是 。
(2)写出电解饱和食盐水的化学方程式 。
制取“84”消毒液(有效成分为NaClO)的原理:Cl2+2NaOH=NaCl+NaClO+H2O;
(3)小吴向2mL“84”消毒液中滴加2﹣3滴无色酚酞试液,发现溶液先变红后褪色,说明“84”消毒液显 性,并有漂白性。
(二)该兴趣小组的同学想了解久置的“84”消毒液是否变质,设计了下列探究实验。
【查阅资料】
①品红溶液是一种红色色素。
②“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应(2NaClO+CO2+H2O═2HClO+Na2CO3),NaClO溶液、HClO都具有漂白、杀菌、消毒功效,能使品红溶液褪色氯化钠和碳酸钠不能使品红溶液褪色。
③HClO不稳定,受热或光照会分解,分解后丧失漂白作用。
④Ca(ClO)2易溶于水
【提出问题】放置一段时间的“84”消毒液是否变质?如果变质,变质程度如何?
【提出猜想】猜想1:未变质,溶液中主要成分为NaCl、NaClO
(4)猜想2:部分变质,溶液中主要成分为 。
猜想3:全部变质,溶液中主要成分为NaCl、Na2CO3
(5)【实验探究】
猜想 不成立;
。
(6)写出实验操作①中产生白色沉淀的化学方程式 。
(7)【交流反思】实验最终确定猜想3成立。有人提出直接将这样的“84”消毒液倒掉会污染环境,为了将碳酸钠除去,我们应该向其中加入稀盐酸,直到 为止。
(8)【拓展应用】“84”消毒液存放时应注意的事项是 。
(一)电解饱和食盐水可以制得氢氧化钠、氯气(C12)和氢气,进而生产具有消毒、漂白作用的“84”消毒液。
(1)实验过程中与负极相连的导管口周围严禁明火,其原因是 。
(2)写出电解饱和食盐水的化学方程式 。
制取“84”消毒液(有效成分为NaClO)的原理:Cl2+2NaOH=NaCl+NaClO+H2O;
(3)小吴向2mL“84”消毒液中滴加2﹣3滴无色酚酞试液,发现溶液先变红后褪色,说明“84”消毒液显 性,并有漂白性。
(二)该兴趣小组的同学想了解久置的“84”消毒液是否变质,设计了下列探究实验。
【查阅资料】
①品红溶液是一种红色色素。
②“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应(2NaClO+CO2+H2O═2HClO+Na2CO3),NaClO溶液、HClO都具有漂白、杀菌、消毒功效,能使品红溶液褪色氯化钠和碳酸钠不能使品红溶液褪色。
③HClO不稳定,受热或光照会分解,分解后丧失漂白作用。
④Ca(ClO)2易溶于水
【提出问题】放置一段时间的“84”消毒液是否变质?如果变质,变质程度如何?
【提出猜想】猜想1:未变质,溶液中主要成分为NaCl、NaClO
(4)猜想2:部分变质,溶液中主要成分为 。
猜想3:全部变质,溶液中主要成分为NaCl、Na2CO3
(5)【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取适量该溶液于烧杯中,滴入适量氯化钙溶液 | 产生白色沉淀 | 猜想________不成立 |
| ②另取适量该溶液于试管中,滴入几滴品红溶液 | ________ | 猜想3成立 |
猜想 不成立;
。
(6)写出实验操作①中产生白色沉淀的化学方程式 。
(7)【交流反思】实验最终确定猜想3成立。有人提出直接将这样的“84”消毒液倒掉会污染环境,为了将碳酸钠除去,我们应该向其中加入稀盐酸,直到 为止。
(8)【拓展应用】“84”消毒液存放时应注意的事项是 。

20.氢氧化镁是一种重要的化工原料。某矿石由MgO、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
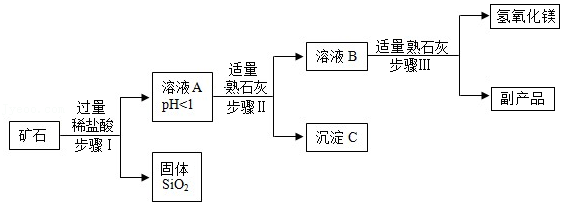
部分金属阳离子以氢氧化物形成沉淀时溶液的pH见右表:
(1)步骤I分离溶液A和固体SiO2的实验操作名称是 。
(2)溶液A中的阳离子有 (填离子符号)。
(3)为了使Cu(OH)2完全沉淀,步骤Ⅱ需控制的pH范围是 。
(4)步骤Ⅲ反应的化学方程式为 。
(5)所得产品表面可能残留少量滤液,需用蒸馏水多次洗涤,如何检验产品是否洗涤干净 。
(6)现有200kg含氧化镁40%的矿石,假设各步均充分反应,镁元素无损耗,最终能制得多少千克的氢氧化镁?(写出计算过程)

部分金属阳离子以氢氧化物形成沉淀时溶液的pH见右表:
| 沉淀物 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀 | 4.2 | 9.1 |
| 完全沉淀 | 6.7 | 11.1 |
(1)步骤I分离溶液A和固体SiO2的实验操作名称是 。
(2)溶液A中的阳离子有 (填离子符号)。
(3)为了使Cu(OH)2完全沉淀,步骤Ⅱ需控制的pH范围是 。
(4)步骤Ⅲ反应的化学方程式为 。
(5)所得产品表面可能残留少量滤液,需用蒸馏水多次洗涤,如何检验产品是否洗涤干净 。
(6)现有200kg含氧化镁40%的矿石,假设各步均充分反应,镁元素无损耗,最终能制得多少千克的氢氧化镁?(写出计算过程)
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解