下载高清试卷
【2021年山东省威海市经济技术开发区中考化学一模试卷】-第1页
试卷格式:2021年山东省威海市经济技术开发区中考化学一模试卷.PDF
试卷热词:最新试卷、2021年、山东试卷、威海市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.物质是不断运动变化的。下列变化属于化学变化的是( )
①苹果榨汁②动物呼吸③铁水铸成锅④植物光合作用⑤燃放焰火⑥风力发电⑦纺纱织布⑧食物霉变
①苹果榨汁②动物呼吸③铁水铸成锅④植物光合作用⑤燃放焰火⑥风力发电⑦纺纱织布⑧食物霉变
- A. ②④⑤⑧
- B. ①②④⑤
- C. ④⑤⑦
- D. ③⑦⑧
2.下列关于物质分类的说法正确的是( )
①食醋②氧化钙③干冰④镁条⑤氢气⑥酒精⑦氯化钾
①食醋②氧化钙③干冰④镁条⑤氢气⑥酒精⑦氯化钾
- A. 混合物有①⑦
- B. 有机物有④⑥
- C. 氧化物有②③
- D. 单质有⑤⑥
3.江苏无锡李阿姨怀疑人民币上可能沾染新冠病毒,放进微波炉中加热消毒。不到一分钟,微波炉中就飘出了焦糊味。李阿姨慌忙去取现金,但为时已晚,纸币大部分已经炭化至黑色。下列说法错误的是( )
- A. 能闻到焦糊味说明分子在不断地运动
- B. 纸币炭化发生了物理变化
- C. 纸币是一种可燃物
- D. 微波炉加热提供了纸张炭化的条件
4.人类研究化学变化的目的之一是获得新物质。下列对获取物质的认识正确的是( )
- A. 二氧化碳、氧气都可以用向下排空气法收集,因为密度比空气大
- B. 熟石灰加水可以制得生石灰
- C. 海水制碱,通入氨气的目的是促进二氧化碳的溶解
- D. 海水淡化过程发生了化学变化,反应前后元素的种类不变
5.下列对化肥和农药的说法正确的是( )
- A. 使用化肥越多,农作物产量越高
- B. 铵态氮肥与熟石灰混合施用可以提高肥效
- C. 大量使用农药会导致土壤和食品污染,因此要杜绝使用农药
- D. 适当增大蔬菜大棚内二氧化碳的浓度,可以提高产量
6.工业炼锰的化学方程式为:8Al+3Mn3O4
9Mn+4Al2O3。下列对该反应的认识正确的是( )
| 高温 |
- A. 该反应属于复分解反应
- B. 反应前后,锰元素的化合价升高
- C. 铝发生了还原反应
- D. 该反应可用于工业生产,说明锰的市场价格高于铝
7.规范的操作是化学实验成果的保障.下列实验操作正确的是( )
- A.
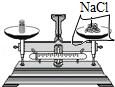 称量NaCl固体
称量NaCl固体 - B.
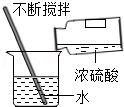 稀释浓硫酸
稀释浓硫酸 - C.
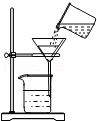 过滤
过滤 - D.
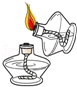 点燃酒精灯
点燃酒精灯
8.图表是化学学习的重要工具。下列对图表的使用不正确的是( )
- A. 根据元素周期表,查找元素原子核内中子数
- B. 根据金属活动性顺序,判断金属能否与稀盐酸反应产生氢气
- C. 根据“酸、碱和盐溶解性表”,判断物质的溶解性
- D. 根据物质的溶解度曲线,查找物质在某一温度时的溶解度
9.下列关于燃烧和灭火的说法,正确的是( )
- A. 发生火灾时,要迅速打开所有门窗,通风降温
- B. 灭火一定要同时破坏燃烧的三个条件
- C. 将木柴架空燃烧,目的是降低可燃物的着火点
- D. 钻木取火通过摩擦生热,温度达到了可燃物的着火点
10.下列实验方案设计中,不能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去CuCl2溶液中的少量稀盐酸 | 加适量CuO,充分反应 |
| B | 除去氧气中的少量氢气 | 把气体通过灼热的铜网 |
| C | 检验暴露在空气中的氢氧化钠样品是否变质 | 加入适量稀盐酸,观察 |
| D | 鉴别NaOH、NaCl、NH4NO3、CuSO4四种固体 | 分别加入适量水,观察 |
- A. A
- B. B
- C. C
- D. D
11.探秘原子结构。
(1)人类探索原子结构的奥秘,经历了漫长的过程。如图是几位有代表性的科学家及他们提出的原子结构模型,模型建立的先后顺序是 (填字母序号)。
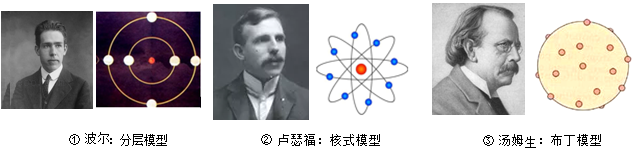
A.①②③
B.③②①
C.①③②
D.③①②
(2)1911年,物理学家卢瑟福用一束带正电的、质量比电子大得多的高速α粒子轰击金箔,发现:多数α粒子穿过金箔后仍保持原来的运动方向,少数α粒子发生了较大角度的偏转,极少数α粒子被反弹。
①实验中的金箔可以压制成厚度仅为0.12微米的薄片,约是头发丝直径的
,厚度里没有太多原子,这是因为金具有良好的 性。
②当α粒子轰击金箔时,图中四条运动轨迹不可能出现的是 (填序号)。
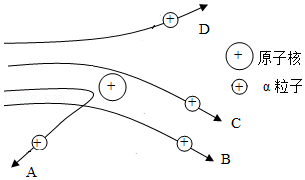
卢瑟福根据实验现象推测:原子中心有一个很小的结构(原子核),原子核具有如下特点: 。
(3)用高能粒子轰击原子核是研究微观粒子的一种常用方法。
1934年,意大利科学家费米用中子轰击铀235原子(质子数为92,相对原子质量是235,元素符号为U),得到了一种质量增加的原子。他公开宣布发现了93号元素(质子数为93的元素),被科学界认可并获得了诺贝尔物理学奖。1938年,德国科学家哈恩重复费米的实验后,发现实验中得到的是56号钡元素,并用如图模型定义这一变化。费米知道后,立即重复了实验,坦率地检讨并纠正了错误。
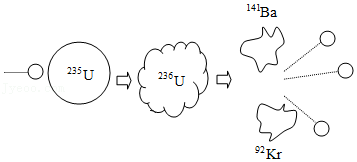
①235U原子中,中子数是 。
②上述变化是不是化学变化 ,理由是 。
(4)分析原子结构及原子的发现历程,以下观点正确的是 。
A.科学模型的建立是一个不断完善、修正的过程
B.模型是一种重要的方法,人类借助模型构建,对原子的认识逐渐接近本质
C.科学结论的得出要依据客观事实,面对前人的观点要敢于质疑
D.科学理论的发展过程是发现并改正前人错误认识的过程
(1)人类探索原子结构的奥秘,经历了漫长的过程。如图是几位有代表性的科学家及他们提出的原子结构模型,模型建立的先后顺序是 (填字母序号)。

A.①②③
B.③②①
C.①③②
D.③①②
(2)1911年,物理学家卢瑟福用一束带正电的、质量比电子大得多的高速α粒子轰击金箔,发现:多数α粒子穿过金箔后仍保持原来的运动方向,少数α粒子发生了较大角度的偏转,极少数α粒子被反弹。
①实验中的金箔可以压制成厚度仅为0.12微米的薄片,约是头发丝直径的
| 1 |
| 150 |
②当α粒子轰击金箔时,图中四条运动轨迹不可能出现的是 (填序号)。

卢瑟福根据实验现象推测:原子中心有一个很小的结构(原子核),原子核具有如下特点: 。
(3)用高能粒子轰击原子核是研究微观粒子的一种常用方法。
1934年,意大利科学家费米用中子轰击铀235原子(质子数为92,相对原子质量是235,元素符号为U),得到了一种质量增加的原子。他公开宣布发现了93号元素(质子数为93的元素),被科学界认可并获得了诺贝尔物理学奖。1938年,德国科学家哈恩重复费米的实验后,发现实验中得到的是56号钡元素,并用如图模型定义这一变化。费米知道后,立即重复了实验,坦率地检讨并纠正了错误。

①235U原子中,中子数是 。
②上述变化是不是化学变化 ,理由是 。
(4)分析原子结构及原子的发现历程,以下观点正确的是 。
A.科学模型的建立是一个不断完善、修正的过程
B.模型是一种重要的方法,人类借助模型构建,对原子的认识逐渐接近本质
C.科学结论的得出要依据客观事实,面对前人的观点要敢于质疑
D.科学理论的发展过程是发现并改正前人错误认识的过程
12.物质的溶解。
t1℃时,将M、N两种固体物质(均不含结晶水)各25g,分别加入盛有100g水的烧杯中,充分搅拌后现象如图甲所示;升温到t2℃时,忽略水分蒸发,现象如图乙所示。图丙是M、N两种固体物质在水中的溶解度曲线。
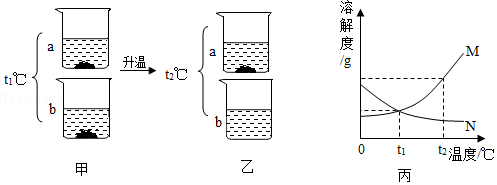
(1)a烧杯中溶解的物质是 。
(2)图甲中,两烧杯溶液中溶质的质量分数大小关系是(填大于、小于或等于)a b。
(3)图乙中,烧杯b中溶质的质量分数为 ,所得溶液是否饱和 。
(4)若M中混有少量N,提纯M可以采取 法。
t1℃时,将M、N两种固体物质(均不含结晶水)各25g,分别加入盛有100g水的烧杯中,充分搅拌后现象如图甲所示;升温到t2℃时,忽略水分蒸发,现象如图乙所示。图丙是M、N两种固体物质在水中的溶解度曲线。

(1)a烧杯中溶解的物质是 。
(2)图甲中,两烧杯溶液中溶质的质量分数大小关系是(填大于、小于或等于)a b。
(3)图乙中,烧杯b中溶质的质量分数为 ,所得溶液是否饱和 。
(4)若M中混有少量N,提纯M可以采取 法。
13.化学与疫情防控。
新型冠状病毒具有传染性,做好日常消毒,是疫情防控的重要措施之一。消毒液可选择75%酒精、过氧乙酸、次氯酸钠等。过氧乙酸(化学式CH3COOOH)是一种有机酸,为无色液体,具有强烈刺激性气味,易挥发,易溶于水,水溶液呈酸性,具有强烈的氧化性,对纸、木塞、橡胶和皮肤等有腐蚀作用,易分解生成乙酸和氧气。浓度大于45%就有爆炸性,遇高热、还原剂就可能引起爆炸。
(1)图1是过氧乙酸分子和乙酸分子的结构式,从元素组成的角度看二者的共同点是 。二者化学性质不同,主要是图2的哪种结构导致的 (填序号)。

(2)写出过氧乙酸分解的化学方程式 。过氧乙酸溶液与乙酸溶液都呈酸性的原因是 。
(3)使用过氧乙酸时要十分小心,不慎沾在皮肤上,应当 。将100g溶质质量分数为10%的过氧乙酸溶液稀释成0.2%的溶液用于环境消毒,需要加水 g,配制过程中可以使用下列哪些器具 (填序号)。
A.铝桶
B.塑料桶
C.橡胶桶
D.木棒
E.铁棒
F.玻璃棒
(4)根据过氧乙酸的物理性质,写出一条保存中的注意事项 。
新型冠状病毒具有传染性,做好日常消毒,是疫情防控的重要措施之一。消毒液可选择75%酒精、过氧乙酸、次氯酸钠等。过氧乙酸(化学式CH3COOOH)是一种有机酸,为无色液体,具有强烈刺激性气味,易挥发,易溶于水,水溶液呈酸性,具有强烈的氧化性,对纸、木塞、橡胶和皮肤等有腐蚀作用,易分解生成乙酸和氧气。浓度大于45%就有爆炸性,遇高热、还原剂就可能引起爆炸。
(1)图1是过氧乙酸分子和乙酸分子的结构式,从元素组成的角度看二者的共同点是 。二者化学性质不同,主要是图2的哪种结构导致的 (填序号)。

(2)写出过氧乙酸分解的化学方程式 。过氧乙酸溶液与乙酸溶液都呈酸性的原因是 。
(3)使用过氧乙酸时要十分小心,不慎沾在皮肤上,应当 。将100g溶质质量分数为10%的过氧乙酸溶液稀释成0.2%的溶液用于环境消毒,需要加水 g,配制过程中可以使用下列哪些器具 (填序号)。
A.铝桶
B.塑料桶
C.橡胶桶
D.木棒
E.铁棒
F.玻璃棒
(4)根据过氧乙酸的物理性质,写出一条保存中的注意事项 。
14.化学与航天事业。
人类的生命活动离不开清新的空气。在航天飞行器座舱内,空气更新过程如图所示。请分析回答下列问题: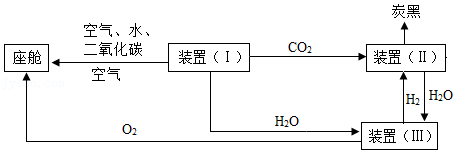
(1)在如图空气更新的过程中,C、H、O三种元素中的 (填符号)元素没有参与再利用。
(2)装置(Ⅱ)中,在高温和催化剂的条件下,CO2和H2发生反应的化学方程式为 ,该反应属于基本反应类型中的 。根据学过的知识,装置(Ⅲ)中发生反应的化学方程式是 。
(3)研究发现,在太空舱中NiFe2O4能将呼出的二氧化碳转化为氧气,而本身的质量和化学性质在反应前后都没有发生改变。NiFe2O4在这一反应中的作用是 。已知NiFe2O4中Ni元素的化合价为+2价,则Fe元素的化合价为 。
人类的生命活动离不开清新的空气。在航天飞行器座舱内,空气更新过程如图所示。请分析回答下列问题:

(1)在如图空气更新的过程中,C、H、O三种元素中的 (填符号)元素没有参与再利用。
(2)装置(Ⅱ)中,在高温和催化剂的条件下,CO2和H2发生反应的化学方程式为 ,该反应属于基本反应类型中的 。根据学过的知识,装置(Ⅲ)中发生反应的化学方程式是 。
(3)研究发现,在太空舱中NiFe2O4能将呼出的二氧化碳转化为氧气,而本身的质量和化学性质在反应前后都没有发生改变。NiFe2O4在这一反应中的作用是 。已知NiFe2O4中Ni元素的化合价为+2价,则Fe元素的化合价为 。
15.酿造中的化学。
我国是最早酿酒的国家,早在2000年前就发明了酿酒技术。酿造白酒时,先将富含淀粉的植物种子(如大米等)蒸熟、冷却至40℃左右,将适量酒曲(含有糖化酶、酒化酶)用少量冷开水调成悬浊液,与蒸熟的原料混合均匀,放在30℃~40℃环境下,淀粉【(C6H10O5)n】在糖化酶和水的作用下,转化为葡萄糖;生成的葡萄糖在酒化酶作用下,转化为酒精,同时释放出能使澄清石灰水变浑浊的气体。
在酿酒过程中,如果保存不当,白酒中的酒精就会与空气中的氧气发生缓慢氧化,转化成醋酸和水而变酸。
(1)新酿出的酒往往比较浑浊,为了获得比较清澈的酒,可以进行 操作。在这一过程中,酒精在溶液中的质量分数 (填“有”或“没有”)发生改变。
(2)写出酿酒过程发生反应的化学方程式 。
(3)通过粮食直接酿出的白酒中酒精的体积分数为15%左右(即酒精度为15°左右),为了增大酒精度,还需要蒸馏。在标准大气压下,水的沸点是100℃,酒精的沸点是78.3℃,蒸馏时应当控制温度的范围在 。
(4)酒精是一种常用的燃料,酒精完全燃烧的化学方程式是 ,反应中能量的主要转化形式是 ;酿酒过程中,因保存不当导致酒精缓慢氧化变酸的化学方程式是 。酒精缓慢氧化与酒精燃烧产物不同,是因为 。反应物相同,但生成物不同的化学变化很多,请再举一例 。
(5)许多外界因素会影响化学反应的进程或速率,控制这些因素就可以让化学反应朝着我们期望的方向进行。例如酿酒时我们需要控制温度在30℃~40℃之间,以促进发酵。请你再列举一个影响化学反应速率的因素,并以锌和稀硫酸反应为例,通过实验说明该因素对化学反应的影响:
我国是最早酿酒的国家,早在2000年前就发明了酿酒技术。酿造白酒时,先将富含淀粉的植物种子(如大米等)蒸熟、冷却至40℃左右,将适量酒曲(含有糖化酶、酒化酶)用少量冷开水调成悬浊液,与蒸熟的原料混合均匀,放在30℃~40℃环境下,淀粉【(C6H10O5)n】在糖化酶和水的作用下,转化为葡萄糖;生成的葡萄糖在酒化酶作用下,转化为酒精,同时释放出能使澄清石灰水变浑浊的气体。
在酿酒过程中,如果保存不当,白酒中的酒精就会与空气中的氧气发生缓慢氧化,转化成醋酸和水而变酸。
(1)新酿出的酒往往比较浑浊,为了获得比较清澈的酒,可以进行 操作。在这一过程中,酒精在溶液中的质量分数 (填“有”或“没有”)发生改变。
(2)写出酿酒过程发生反应的化学方程式 。
(3)通过粮食直接酿出的白酒中酒精的体积分数为15%左右(即酒精度为15°左右),为了增大酒精度,还需要蒸馏。在标准大气压下,水的沸点是100℃,酒精的沸点是78.3℃,蒸馏时应当控制温度的范围在 。
(4)酒精是一种常用的燃料,酒精完全燃烧的化学方程式是 ,反应中能量的主要转化形式是 ;酿酒过程中,因保存不当导致酒精缓慢氧化变酸的化学方程式是 。酒精缓慢氧化与酒精燃烧产物不同,是因为 。反应物相同,但生成物不同的化学变化很多,请再举一例 。
(5)许多外界因素会影响化学反应的进程或速率,控制这些因素就可以让化学反应朝着我们期望的方向进行。例如酿酒时我们需要控制温度在30℃~40℃之间,以促进发酵。请你再列举一个影响化学反应速率的因素,并以锌和稀硫酸反应为例,通过实验说明该因素对化学反应的影响:
| 影响因素 | 实验方案 | 预期现象及结论 |
16.实验技能考试后,同学们对制取二氧化碳反应后的废液进行了如下探究:取大理石与盐酸反应后的废液10g于烧杯中,滴加溶质质量分数为5%的氢氧化钠溶液10g,溶液pH变化如图所示,计算废液中盐酸的溶质质量分数。


查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解