下载高清试卷
【2022年江苏省泰州市中考化学模拟试卷】-第1页
试卷格式:2022年江苏省泰州市中考化学模拟试卷.PDF
试卷热词:最新试卷、2022年、江苏试卷、泰州市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.生活中处处都有物质变化。下列属于化学变化的是( )
- A. 西瓜榨汁
- B. 食物腐败
- C. 瓷碗破碎
- D. 湿衣晾干
2.下列物质的用途主要与其物理性质有关的是( )
- A. 铁粉作食品保鲜剂
- B. 氮气作灯泡填充气
- C. 干冰制造舞台云雾
- D. 镁粉用于制造烟花
3.中国是世界上第一个生产激光晶体[氟代硼铍酸钾(KBe2BO3F2)]这种战略性材料的国家,氟代硼铍酸钾(KBe2BO3F2)属于( )
- A. 氧化物
- B. 酸
- C. 碱
- D. 盐
4.如图所示的实验操作中,正确的是( )
- A.

- B.
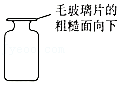
- C.
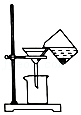
- D.

5.下列关于实验现象的描述中正确的是( )
- A. 红磷在空气中燃烧,产生大量五氧化二磷
- B. 硝酸铵溶于水,溶液温度升高
- C. 向肥皂水中滴加石蕊试液,溶液变红
- D. 向面包片上滴加碘酒呈蓝色
6.实验室以大理石为原料制备CO2并获得无水CaCl2。下列装置能达到相应实验目的的是( )
- A.
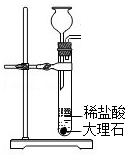 生成CO2
生成CO2 - B.
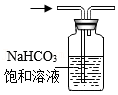 除去CO2中的HCl
除去CO2中的HCl - C.
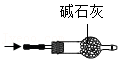 干燥CO2
干燥CO2 - D.
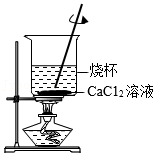 制得无水CaCl2
制得无水CaCl2
7.下列排序正确的是( )
- A. 空气中气体含量:由多到少
O2、N2、CO2 - B. 常见溶液的pH:由大到小
柠檬汁、蒸馏水、肥皂水 - C. 氯元素的化合价:由高到低
NaClO、Cl2、NaCl - D. 氮元素的质量分数:由大到小
NO、N2O5、NO2
8.在元素周期表中锂元素的某些信息如图所示,下列有关锂的说法不正确的是( )


- A. 原子序数为3
- B. 元素符号为Li
- C. 属于金属元素
- D. 相对原子质量为6.941g
9.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
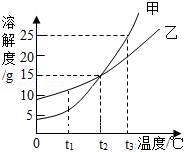

- A. 乙中含有少量甲,可用冷却热饱和溶液的方法提纯乙
- B. t3℃时,甲的溶液溶质质量分数一定大于乙的溶液溶质质量分数
- C. t3℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t2℃,析出晶体的质量甲一定大于乙
- D. t1℃时,乙的不饱和溶液只有通过蒸发溶剂的方法才能转变成饱和溶液
10.营养素对人类的生命活动具有重要意义。下列说法中,正确的是( )
- A. 钙、铁、锌是人体必需的微量元素
- B. 霉变的大米洗净后可食用
- C. 大量食用高脂肪、高热量的食物不会使人肥胖
- D. 处于生长发育期的青少年对蛋白质的需求比成年人多
11.下列实验方案不能达到实验目的的是( )
- A. 鉴别真假黄金,看颜色
- B. 鉴别硬水和软水,加肥皂水搅拌后观察
- C. 鉴别合成纤维和羊毛纤维,点燃后闻气味
- D. 将Zn和Ag分别放入CuSO4溶液中可比较Zn、Cu、Ag的金属活动性
12.下列物质的转化在给定条件下均能实现的是( )
- A. SSO2点燃
O2 H2SO4H2O - B. Fe3O4Fe高温
CO FeCl2稀盐酸 - C. C6H12O6CO2酶
O2 CaCO3CaCl2溶液 - D. KNO3K2CO3Na2CO3溶液KCl稀HCl
13.除去下列各物质中少量杂质,选用的方案不合理的是( )
| 选项 | 物质 | 所含杂质 | 方案 |
| A | H2 | H2O(气) | 混合气体通过浓硫酸 |
| B | KCl | MnO2 | 加水溶解、过滤、蒸发 |
| C | CuO | C | 在氧气流中加热 |
| D | NaOH溶液 | Ca(OH)2 | 加入过量Na2CO3溶液,过滤 |
- A. A
- B. B
- C. C
- D. D
14.下列各组物质的溶液,不另加试剂就能鉴别出来的一组是( )
- A. Na2CO3、HCl、H2SO4
- B. KCl、NaCl、Na2SO4
- C. FeCl3、NaOH、KNO3
- D. HCl、NaOH、Ca(OH)2
15.已知电导率传感器用于测量溶液的导电性强弱。一定条件下,电导率的大小能反映离子浓度的大小。常温下将一定质量的氯化钠固体加入盛有 100mL 蒸馏水烧杯中,测得的电导率数据如图所示。以下分析不正确的是( )


- A. 由图可知,a 点对应的操作是向水中加入氯化钠固体
- B. c点的电导率不再变化,说明此时溶液一定达到饱和状态
- C. 测定氯化钠溶液中不同位置的电导率,数值相同,说明氯化钠溶液是均一的
- D. 由图可知,可通过测量液体电导率来区分蒸馏水和稀氯化钠溶液
16.发挥化学力量,抵御新冠疫情!回答下列问题:
(1)有效防控,测量体温。家庭体温计中的银白色液体的化学式为 。
(2)杀菌消毒,净化校园。
①84消毒液的有效成分为次氯酸钠(NaClO),其中氯元素的化合价为 。
②现用50g质量分数为4%的过氧乙酸溶液配制0.5%的消毒液,需水 mL,主要实验步骤为:计算、 、稀释。
(3)安全出行,佩戴口罩。口罩中活性炭起 作用,某品牌口罩所用材料如图所示,其中属于有机合成材料的是 。
(4)合理膳食,增强免疫。如表是豆浆中部分营养成分的平均质量分数,请回答:
豆浆中的 在消化道内会被分解成可被人体吸收的多种氨基酸,豆浆中含有的人体必需的微量元素,可以预防 。
(5)科学洗手,天天健康。洗洁精清洗油污,利用其 作用。

(1)有效防控,测量体温。家庭体温计中的银白色液体的化学式为 。
(2)杀菌消毒,净化校园。
①84消毒液的有效成分为次氯酸钠(NaClO),其中氯元素的化合价为 。
②现用50g质量分数为4%的过氧乙酸溶液配制0.5%的消毒液,需水 mL,主要实验步骤为:计算、 、稀释。
(3)安全出行,佩戴口罩。口罩中活性炭起 作用,某品牌口罩所用材料如图所示,其中属于有机合成材料的是 。
(4)合理膳食,增强免疫。如表是豆浆中部分营养成分的平均质量分数,请回答:
| 成分 | 蛋白质 | 油脂 | 糖类 | 钙 | 铁 | 维生素 |
| 质量分数(%) | 1.8 | 0.7 | 1.1 | 0.01 | 0.0005 | 0.015 |
豆浆中的 在消化道内会被分解成可被人体吸收的多种氨基酸,豆浆中含有的人体必需的微量元素,可以预防 。
(5)科学洗手,天天健康。洗洁精清洗油污,利用其 作用。

17.水乡兴化,鱼肥蟹美。“鱼浮灵”是化学增氧剂,含过氧碳酸钠(2Na2CO3•3H2O2),溶于水增加水体溶氧量,提高活鱼成活率。琦琦同学对“鱼浮灵”的成分、增氧原理及制备进行如下探究:
【查阅资料】①过氧碳酸钠具有碳酸钠和过氧化氢的双重性质,过氧化氢可用于消毒、漂白;
②碳酸钠溶液显碱性,含有OH﹣、CO
;Na+不影响过氧化氢的分解;
③相同温度下,pH相同的溶液,OH﹣的浓度也相同;
④异丙醇为有机溶剂,水与异丙醇可以互溶,过氧碳酸钠在异丙醇中溶解度较小。
【探究一】“鱼浮灵”的成分测定。琦琦设计如下方案,请补充完成实验报告中的相关内容。
(1)
(2)过氧碳酸钠的用途不合理的是 (填字母)。
A.鱼池增氧 B.消毒剂 C.干燥剂 D.漂白剂
【探究二】“鱼浮灵”增氧原理。
【提出问题】过氧碳酸钠溶液中的哪种微粒对过氧化氢分解有促进作用?
(3)【猜想假设】猜想一: ;猜想二:OH﹣;猜想三:CO
和OH﹣
【实验过程】相同温度下,进行H2O2溶液以及H2O2溶液中分别加Na2CO3、NaOH的实验,测定相同时间内溶液的pH、溶解氧含量(mg/L),数据如下:
(4)【实验结论】对比实验数据,证明猜想 正确。
【探究三】“鱼浮灵”的工业制备。
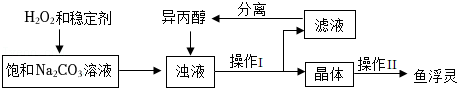
(5)稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子裹住,化学方程式为 。
(6)浊液中加入异丙醇的作用是 。
(7)操作Ⅱ中洗涤晶体的试剂最好选用 (填字母)。
A.饱和NaCl溶液 B.水 C.异丙醇 D.稀盐酸
(8)根据如表数据,你认为上述制备反应的最佳温度范围是 ℃。
【查阅资料】①过氧碳酸钠具有碳酸钠和过氧化氢的双重性质,过氧化氢可用于消毒、漂白;
②碳酸钠溶液显碱性,含有OH﹣、CO
| 2- |
| 3 |
③相同温度下,pH相同的溶液,OH﹣的浓度也相同;
④异丙醇为有机溶剂,水与异丙醇可以互溶,过氧碳酸钠在异丙醇中溶解度较小。
【探究一】“鱼浮灵”的成分测定。琦琦设计如下方案,请补充完成实验报告中的相关内容。
(1)
| 实验序号 | 实验步骤 | 实验现象 | 解释或结论 |
| ① | 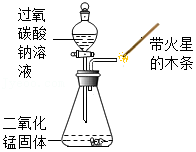 | 锥形瓶中有大量气泡产生, | 分液漏斗的作用是: ,溶液中含有过氧化氢。 |
| ② | 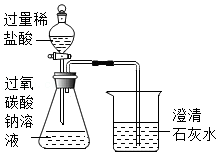 | 锥形瓶中有大量气泡产生, | 溶液中含有Na2CO3 |
(2)过氧碳酸钠的用途不合理的是 (填字母)。
A.鱼池增氧 B.消毒剂 C.干燥剂 D.漂白剂
【探究二】“鱼浮灵”增氧原理。
【提出问题】过氧碳酸钠溶液中的哪种微粒对过氧化氢分解有促进作用?
(3)【猜想假设】猜想一: ;猜想二:OH﹣;猜想三:CO
| 2- |
| 3 |
【实验过程】相同温度下,进行H2O2溶液以及H2O2溶液中分别加Na2CO3、NaOH的实验,测定相同时间内溶液的pH、溶解氧含量(mg/L),数据如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 试剂 | 4%H2O2溶液 | 4%H2O2溶液+Na2CO3 | 4%H2O2溶液+NaOH | 4%H2O2溶液+NaOH |
| pH | 6.01 | 8.14 | 8.15 | 9.26 |
| 溶解氧 | 6.44 | 9.11 | 9.12 | 10.97 |
(4)【实验结论】对比实验数据,证明猜想 正确。
【探究三】“鱼浮灵”的工业制备。

(5)稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子裹住,化学方程式为 。
(6)浊液中加入异丙醇的作用是 。
(7)操作Ⅱ中洗涤晶体的试剂最好选用 (填字母)。
A.饱和NaCl溶液 B.水 C.异丙醇 D.稀盐酸
(8)根据如表数据,你认为上述制备反应的最佳温度范围是 ℃。
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率% | 85.49 | 85.78 | 88.38 | 83.01 |
18.如图表示某些物质间转化关系(反应条件和部分产物已省略)。其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属。
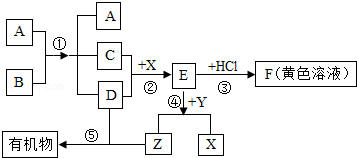
请回答下列问题:
(1)反应①中A物质的作用是 ;
(2)反应③、④的化学方程式:③ ;④ ;
(3)在日常生活中为防止反应②的发生,可采取的措施是 (写一点即可);
(4)在自然界中普遍存在反应⑤,其名称为 。

请回答下列问题:
(1)反应①中A物质的作用是 ;
(2)反应③、④的化学方程式:③ ;④ ;
(3)在日常生活中为防止反应②的发生,可采取的措施是 (写一点即可);
(4)在自然界中普遍存在反应⑤,其名称为 。
19.A、B、C、D、E、F是初中化学常见的物质,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其反应情况如图所示:(短线“﹣”相连的物质间能反应,箭头“→”表示能生成)
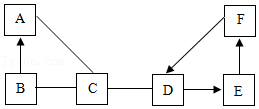
(1)A的化学式为 ;F→D的反应属于 (填基本反应类型)反应,该反应属于 (填“放热”或“吸热”)反应。
(2)写出下列反应或转化的化学方程式。
B与C反应: ;D转化为E: ,该反应在实验室中可用来 (填一种用途)。
(3)写出F的一种用途: 。

(1)A的化学式为 ;F→D的反应属于 (填基本反应类型)反应,该反应属于 (填“放热”或“吸热”)反应。
(2)写出下列反应或转化的化学方程式。
B与C反应: ;D转化为E: ,该反应在实验室中可用来 (填一种用途)。
(3)写出F的一种用途: 。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解