下载高清试卷
【2021年广东省茂名市茂南区中考化学模拟试卷】-第1页
试卷格式:2021年广东省茂名市茂南区中考化学模拟试卷.PDF
试卷热词:最新试卷、2021年、广东试卷、茂名市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.2020年3月9日19时55分,我国在西昌卫星发射中心用长征三号乙运载火箭成功发射北斗系统第五十四颗导航卫星,卫星发射步骤包括:Ⅰ加注燃料、Ⅱ点火起飞、Ⅲ星箭分离、Ⅳ卫星入轨,其中涉及化学变化的步骤是( )
- A. Ⅰ
- B. Ⅱ
- C. Ⅲ
- D. Ⅳ
2.分类和归纳是行之有效、简单易行的科学方法。下列说法错误的是( )
- A. 锂、汞都属于金属元素
- B. 锌、碘都属于人体必需微量元素
- C. 尿素[CO(NH2)2]、硝酸钾都属于复合肥料
- D. 金刚石、氦气都属于单质
3.以下几种实验操作,正确的是( )
- A.
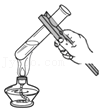 给试管中液体加热
给试管中液体加热 - B.
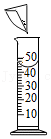 将NaCl倒入量筒中配制溶液
将NaCl倒入量筒中配制溶液 - C.
 将锌粒放入试管中
将锌粒放入试管中 - D.
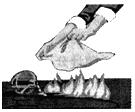 酒精灯失火用湿抹布扑盖
酒精灯失火用湿抹布扑盖
4.火箭使用的一种燃料是偏二甲肼(C2H8N2),发生如下反应:C2H8N2+2X
2CO2+4H2O+3N2,下列说法不正确的是( )
| 点燃 |
- A. 工业上可用分离液态空气法得到N2
- B. C2H8N2属于有机物
- C. X的化学式是NO2
- D. CO2是光合作用的原料之一
5.逻辑推理是化学学习中常用的思维方法,下列推理正确的是( )
- A. 非金属氧化物与碱反应生成盐和水,故可以用氢氧化钠吸收CO
- B. 同种元素的粒子具有相同的质子数,所以质子数相同的粒子属于同种元素
- C. 碱一定含有氢元素
- D. 活泼金属和酸反应有气体产生,则与酸反应产生气体的物质一定是活泼金属
6.中考复习阶段,某同学梳理了以下知识:
①纯碱属于碱;
②干冰不是冰;
③合金属于合成材料;
④pH<7的溶液一定显酸性;
⑤100g质量分数为10%的稀盐酸蒸发掉50g的水后可以得到20%的盐酸溶液;
⑥浓硫酸能使纸张、木材变黑,是因为浓硫酸有吸水性。
上面说法正确的是( )
①纯碱属于碱;
②干冰不是冰;
③合金属于合成材料;
④pH<7的溶液一定显酸性;
⑤100g质量分数为10%的稀盐酸蒸发掉50g的水后可以得到20%的盐酸溶液;
⑥浓硫酸能使纸张、木材变黑,是因为浓硫酸有吸水性。
上面说法正确的是( )
- A. ①②④
- B. ③⑥
- C. ④⑥
- D. ②④
7.利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )


- A. 实验时应先点燃酒精灯后通CO
- B. b处可用澄清石灰水检验生成的CO2
- C. 充分加热,a处固体由黑色变为红色
- D. 可用NaOH溶液吸收尾气中的CO
8.已知:Na2O+H2O═2NaOH。向一定量的稀氢氧化钠溶液中加入少量Na2O固体至消失,恢复到原来温度(不考虑水的蒸发)。下列关于所得溶液的说法中,正确的是( )
- A. 溶质质量增多,溶液的质量减少
- B. 溶质质量增多,溶液的质量不变
- C. 溶剂的质量减少,溶质质量分数不变
- D. 溶剂的质量减少,溶质质量分数增大
9.下列物质的性质与用途均正确并相对应的是( )
| 性质 | 用途 | |
| A | 铝在空气中与氧气反应生成致密氧化膜 | 铝合金用于制作卫生间的置物架 |
| B | 钨的导电性好 | 钨用于制作灯泡里的灯丝 |
| C | CO2水溶液显酸性 | CO2用作大棚蔬菜的气体肥料 |
| D | 氢氧化钠能够与酸反应 | 氢氧化钠用于改良酸性土壤 |
- A. A
- B. B
- C. C
- D. D
10.科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为CH2O),该反应过程的微观示意图如图。下列说法正确的是( )


- A. 物质甲为甲醛,其分子由碳原子和水分子构成
- B. 物质乙中氧元素的化合价为﹣2价
- C. 该反应前后原子种类和数目均发生改变
- D. 该反应消耗物质甲和生成物质丁的质量比为5:3
11.下列实验操作中不能达到实验目的的是( )
| 选项 | 物质 | 目的 | 主要实验操作 |
| A | H2O和H2O2 | 鉴别 | 取样,分别加入少量二氧化锰,观察现象 |
| B | 稀盐酸中是否含有稀H2SO4 | 检验 | 取样,分别加入适量BaCl2,观察现象 |
| C | CaCl2和CaCO3的混合物 | 分离 | 溶解、过滤、洗涤固体并烘干,蒸发滤液 |
| D | BaCl2溶液混有Ba(NO3)2杂质 | 除杂 | 先加入过量Na2SO4溶液,过滤、洗涤;再向所得固体中加入适量稀盐酸 |
- A. A
- B. B
- C. C
- D. D
12.向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
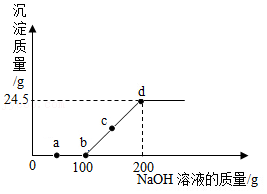

- A. a点溶液中含有两种溶质
- B. bc段发生反应的类型为置换反应
- C. 根据图中数据可以计算出氢氧化钠溶液的浓度
- D. d点溶液中主要存在的离子为Na+、Cu2+、OH﹣、SO42﹣
13.甲、乙两种固体(不含结晶水)的溶解度曲线如图所示,有关分析正确的是( )
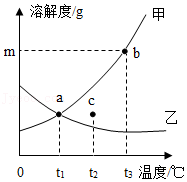

- A. a对应的甲、乙两种溶液,溶质的质量相等
- B. t3℃时,甲、乙两种饱和溶液中,溶质的质量甲>乙
- C. t2℃时,c点所对应两种溶液的溶质质量分数甲>乙
- D. 将t3℃时,甲、乙两种不饱和溶液、降温到t1℃后,都能变为饱和溶液
14.下列各组物质通常情况下不能实现如图所示的转变的是( )
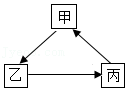
| 选项 | 甲 | 乙 | 丙 |
| A | O2 | CO2 | H2O |
| B | Cu | CuO | CuSO4 |
| C | CaCO3 | CaO | Ca(OH)2 |
| D | C | CO2 | CO |

- A. A
- B. B
- C. C
- D. D
15.下列四个图像能正确反映对应变化关系的是( )
- A.
 在密闭容器中点燃红磷
在密闭容器中点燃红磷 - B.
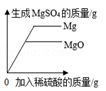 向等质量的Mg和MgO中分别加入足量等浓度的稀硫酸
向等质量的Mg和MgO中分别加入足量等浓度的稀硫酸 - C.
 向一定量的AgNO3和Cu(NO3)2的混合溶液中加入锌粉至过量
向一定量的AgNO3和Cu(NO3)2的混合溶液中加入锌粉至过量 - D.
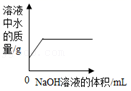 常温下向一定量的稀硫酸中滴加NaOH溶液
常温下向一定量的稀硫酸中滴加NaOH溶液
16.类价二维图反映的是元素的化合价与物质类别之间的关系,构建类价二维图是化学学习的重要方法。图1是某同学绘制的关于碳元素的类价二维图。
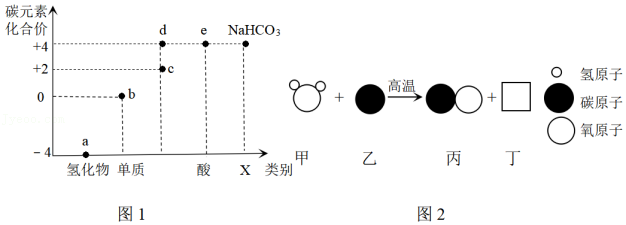
(1)写化学式:a ;e 。
(2)X处对应物质的类别是 。
(3)煤的主要成分是单质碳。图2是用煤合成水煤气的反应微观示意图。该反应中方框丁中微粒的图示为 ,乙对应的物质表现出了 性(填“还原”或“氧化”)。
(4)类价二维图中的物质在一定条件下可以相互转化。请从含碳物质中选择合适物质完成下列表格:

(1)写化学式:a ;e 。
(2)X处对应物质的类别是 。
(3)煤的主要成分是单质碳。图2是用煤合成水煤气的反应微观示意图。该反应中方框丁中微粒的图示为 ,乙对应的物质表现出了 性(填“还原”或“氧化”)。
(4)类价二维图中的物质在一定条件下可以相互转化。请从含碳物质中选择合适物质完成下列表格:
| 转化类型 | 转化的化学方程式 | 反应用途 |
| 碳元素化合价升高 | 工业炼铁 | |
| 炼铜的置换反应 | ||
| 碳元素化合价不变 | NaHCO3+HCl═NaCl+CO2↑+H2O |
17.日常生活、社会发展与化学密切相关。
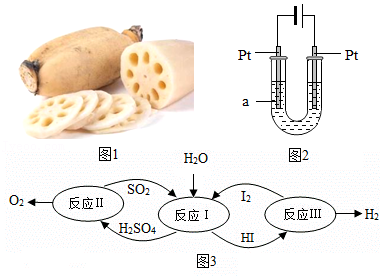
(1)每100g莲藕中含有16.2g糖类、0.9g蛋白质、0.1g脂肪,以及丰富的维生素A、维生素C和铁、钙等元素。
①糖类的组成元素有 。
②人误食重金属盐中毒后,为减轻毒性,最好服用 。(填序号)
a.蛋清
b.乙酸铅溶液
c.水
(2)材料是人类赖以生存的物质基础,是人类社会进步的关键。地铁的轨道建设需用大量钢材。钢材属于 (填字母)。
a.金属材料
b.无机非金属材料
c.有机高分子材料
(3)图2是电解水的示意图,电极a上产生的气体是 。农业生产常用10%~20%的NaCl溶液选种。将300g 25%的NaCl溶液稀释为15%的NaCl溶液,需加水 g。
(4)图3是科学家研究出来的一种以太阳能为热源的碘硫循环分解水制氢的反应流程图。请结合图回答:
①“反应Ⅰ”的化学方程式为 ;
②理论上,每分解ag水能得到氢气 g。

(1)每100g莲藕中含有16.2g糖类、0.9g蛋白质、0.1g脂肪,以及丰富的维生素A、维生素C和铁、钙等元素。
①糖类的组成元素有 。
②人误食重金属盐中毒后,为减轻毒性,最好服用 。(填序号)
a.蛋清
b.乙酸铅溶液
c.水
(2)材料是人类赖以生存的物质基础,是人类社会进步的关键。地铁的轨道建设需用大量钢材。钢材属于 (填字母)。
a.金属材料
b.无机非金属材料
c.有机高分子材料
(3)图2是电解水的示意图,电极a上产生的气体是 。农业生产常用10%~20%的NaCl溶液选种。将300g 25%的NaCl溶液稀释为15%的NaCl溶液,需加水 g。
(4)图3是科学家研究出来的一种以太阳能为热源的碘硫循环分解水制氢的反应流程图。请结合图回答:
①“反应Ⅰ”的化学方程式为 ;
②理论上,每分解ag水能得到氢气 g。
18.实验室制取Cl2:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,已知:盐酸(HCl)是一种无色液体,具有挥发性;Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。
(1)如果实验室用装置A来制取氧气,则反应的化学方程式为 2KClO3
2KCl+3O2↑ ,用E装置收集氧气,则气体从 d 端通入;如果用D装置收集CO2,则气体从 a 端通入。
(2)将红热的细铁丝插入盛有氧气的集气瓶中时可以看到的现象是 剧烈燃烧,火星四射,有黑色固体生成 ,该反应的化学方程式为 3Fe+2O2
Fe3O4 。
(3)图中A、B、C三种发生装置和D、E两种收集装置,请回答下列问题:
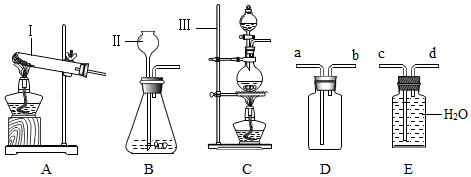
①实验室制取Cl2时,应选择的发生装置是 C (填序号)。
②用A装置制取氧气后,从剩余固体中分离出MnO2的实验步骤有溶解、过滤和洗涤。过滤时玻璃棒的作用是 引流 。
③下列对实验室制取O2、CO2和Cl2的分析中正确的是 D (填序号)。
| △ |
(1)如果实验室用装置A来制取氧气,则反应的化学方程式为 2KClO3
| MnO2 |
| △ |
(2)将红热的细铁丝插入盛有氧气的集气瓶中时可以看到的现象是 剧烈燃烧,火星四射,有黑色固体生成 ,该反应的化学方程式为 3Fe+2O2
| 点燃 |
(3)图中A、B、C三种发生装置和D、E两种收集装置,请回答下列问题:

①实验室制取Cl2时,应选择的发生装置是 C (填序号)。
②用A装置制取氧气后,从剩余固体中分离出MnO2的实验步骤有溶解、过滤和洗涤。过滤时玻璃棒的作用是 引流 。
③下列对实验室制取O2、CO2和Cl2的分析中正确的是 D (填序号)。
- A. 制取CO2和Cl2的发生装置相同
- B. O2、CO2和Cl2都能用排水法收集
- C. 制取Cl2的反应中MnO2是催化剂
- D. 用E装置收集O2时,O2应从d管导入
19.某化学兴趣小组用稀盐酸除去铁钉表面的铁锈(主要成分是Fe2O3),发现反应开始时铁锈消失,有气泡产生,溶液颜色为黄色,一段时间后变为浅绿色。
(提出问题)一段时间后溶液颜色为什么由黄色变为浅绿色?
(查阅资料)(1)Fe2O3+6HCl═2FeCl3+3H2O
(2)FeCl3的溶液呈黄色
(提出猜想)
Ⅰ.溶液变浅绿色与盐酸有关;
Ⅱ. ;
Ⅲ.溶液变浅绿色与水有关。
(设计方案)为验证猜想,设计如下方案:
(实验结论)盐酸除去铁钉表面的铁锈后,Fe与FeCl3反应使溶液由黄色变为浅绿色。
(交流讨论)查阅资料知,FeCl2溶液为绿色,Fe与FeCl3反应的化学方程式是 。
(拓展思考)出土的青铜器文物表面会有铜绿[Cu2(OH)2CO3],铜生锈的条件是 ,写出反应的化学方程式 。
(提出问题)一段时间后溶液颜色为什么由黄色变为浅绿色?
(查阅资料)(1)Fe2O3+6HCl═2FeCl3+3H2O
(2)FeCl3的溶液呈黄色
(提出猜想)
Ⅰ.溶液变浅绿色与盐酸有关;
Ⅱ. ;
Ⅲ.溶液变浅绿色与水有关。
(设计方案)为验证猜想,设计如下方案:
| 实验操作 | 实验现象 | 结论 |
| (1)取FeCl3固体于试管中,加入 ,振荡完全溶解,静置。 | 溶液为黄色 | 猜想Ⅰ不成立。 |
| (2)向盛有少量FeCl3固体的试管中加入 直至溶解,静置。 | 溶液为 色 | 猜想Ⅲ不成立。 |
| (3)向盛有FeCl3溶液的试管中加入足量铁粉,静置。 | 溶液由黄色变为浅绿色 | 猜想 成立 |
(实验结论)盐酸除去铁钉表面的铁锈后,Fe与FeCl3反应使溶液由黄色变为浅绿色。
(交流讨论)查阅资料知,FeCl2溶液为绿色,Fe与FeCl3反应的化学方程式是 。
(拓展思考)出土的青铜器文物表面会有铜绿[Cu2(OH)2CO3],铜生锈的条件是 ,写出反应的化学方程式 。
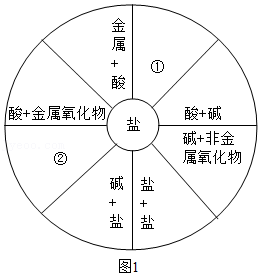
20.小丽学习了单质、氧化物、酸、碱、盐的性质后,发现许多不同类别的物质间反应都生成盐,于是她构建了如图1所示的知识网络图.借助网络图回答:
(1)若盐是碳酸钙,写出利用盐和碱反应制备的化学方程式 .
(2)图中①②处应补充的文字(不能与图中已有信息重复).① ;② .
(3)根据网络图也可获得金属.图2是某工厂利用含铜电缆废料进行回收铜的方案: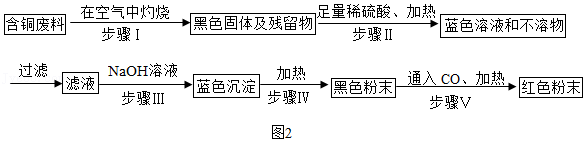
①过滤操作所需玻璃仪器有:漏斗、烧杯和 .
②写出步骤Ⅲ发生反应的化学方程式 ,属于 反应(基本反应类型).
③上述方案中,可能会造成空气污染的是步骤 ;还可以将步骤Ⅲ、Ⅳ和Ⅴ合并,即直接在过滤后的滤液中加入 得到红色粉末,实现方案简化.
(1)若盐是碳酸钙,写出利用盐和碱反应制备的化学方程式 .
(2)图中①②处应补充的文字(不能与图中已有信息重复).① ;② .
(3)根据网络图也可获得金属.图2是某工厂利用含铜电缆废料进行回收铜的方案:

①过滤操作所需玻璃仪器有:漏斗、烧杯和 .
②写出步骤Ⅲ发生反应的化学方程式 ,属于 反应(基本反应类型).
③上述方案中,可能会造成空气污染的是步骤 ;还可以将步骤Ⅲ、Ⅳ和Ⅴ合并,即直接在过滤后的滤液中加入 得到红色粉末,实现方案简化.

21.家庭食用碱的主要成分是Na2CO3,为测定该食用碱中Na2CO3的质量分数,某同学进行了以下实验:取48g食用碱,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见如表(假设该食用碱中不含难溶性杂质且杂质均不与CaCl2溶液产生沉淀)。请分析表中数据回答并计算:
(1)m= g。
(2)48g该食用碱与足量加入CaCl2溶液反应,最多生成沉淀的质量为 g。
(3)该食用碱中Na2CO3的质量分数是多少?(写出计算过程,答案精确到0.1%)
(4)根据表中实验数据以及适当的计算,请画出生成沉淀的质量和加入CaCl2溶液的质量的坐标关系图,请标出拐点数据。
| 实验一 | 实验二 | 实验三 | 实验四 | |
| 食用碱的质量 | 12g | 12g | 12g | 12g |
| 加入CaCl2溶液的质量 | 20g | 40g | 60g | 80g |
| 生成沉淀的质量 | 4g | m | 10g | 10g |
(1)m= g。
(2)48g该食用碱与足量加入CaCl2溶液反应,最多生成沉淀的质量为 g。
(3)该食用碱中Na2CO3的质量分数是多少?(写出计算过程,答案精确到0.1%)
(4)根据表中实验数据以及适当的计算,请画出生成沉淀的质量和加入CaCl2溶液的质量的坐标关系图,请标出拐点数据。

查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解