下载高清试卷
【2021年江苏省南通市中考化学模拟训练试卷(B卷)】-第1页
试卷格式:2021年江苏省南通市中考化学模拟训练试卷(B卷).PDF
试卷热词:最新试卷、2021年、江苏试卷、南通市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.下列变化属于化学变化的是( )
- A.
 冰雪融化
冰雪融化 - B.
 燃料燃烧
燃料燃烧 - C.
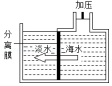 淡化海水
淡化海水 - D.
 品红扩散
品红扩散
2.分类思想是化学学习中的一种重要思想,下列物质分类不正确的一组是( )
- A. 氧化物:水、石灰石
- B. 酸:硫酸、醋酸
- C. 碱:苛性钠、熟石灰
- D. 盐:氯化钠、亚硝酸钠
3.下列实验基本操作正确的是( )
- A.
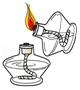 点燃酒精灯
点燃酒精灯 - B.
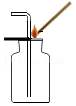 验满CO2
验满CO2 - C.
 从滴瓶里取出液体
从滴瓶里取出液体 - D.
 稀释浓硫酸
稀释浓硫酸
4.下列说法正确的是( )
- A. 金刚石、石墨和C60物理性质差异大是因为碳原子结构不同
- B. 活性炭可用于吸附水中的钙、镁化合物降低水的硬度
- C. 工业上将煤块粉碎后燃烧主要是为了提高燃烧效率
- D. 高炉炼铁的原理是用焦炭将铁矿石中的铁置换出来
5.下列有关物质用途与性质具有对应关系的是( )
- A. 用汽油去除油污﹣﹣汽油密度比水小
- B. 在铁栏杆表面刷铝粉漆防生锈﹣﹣铝是一种银白色金属
- C. 用熟石灰改良酸性土壤﹣﹣熟石灰具有碱性
- D. 用金刚石切割大理石﹣﹣金刚石的熔点高
6.下列实验现象和对应结论的描述都正确的是( )
- A. 向碳酸钠溶液中滴加无色酚酞溶液,溶液变成红色,说明碳酸钠属于碱类
- B. 将氢氧化钠固体放入稀盐酸中,放出热量,该反应一定是放热反应
- C. 向某无色溶液中滴入硝酸钡溶液,产生白色沉淀,该溶液一定是硫酸溶液
- D. 一定温度下向饱和的石灰水加入氧化钙,溶质、溶剂的质量一定减小
7.某兴趣小组做了以下实验,根据实验过程分析下列说法正确的是( )
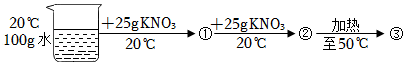
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| 溶解度/g | 20.9 | 31.6 | X | 63.9 | 85.5 |
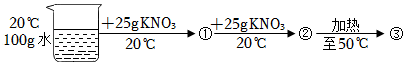
- A. 溶液①溶质质量分数为25%
- B. 溶液②中溶质与溶液的质量比为1:2
- C. 溶液③中再溶解20.5g KNO3可成为饱和溶液
- D. 硝酸钾溶解度随温度的降低而减小
8.下列物质提纯所用的实验方法正确的是( )
| 选项 | 物质(括号内为杂质) | 实验方法 |
| A | CaCl2溶液(稀盐酸) | 加过量的CaCO3固体,过滤 |
| B | CO2(H2O) | 通过装有氢氧化钠固体的干燥管 |
| C | N2(O2) | 通过炽热的木炭层 |
| D | NaCl溶液(Na2SO4) | 加入适量的Ba(NO3)2溶液,过滤 |
- A. A
- B. B
- C. C
- D. D
9.下列实验能达到实验目的的是( )
- A.
 比较吸入空气与呼出气体中CO2含量
比较吸入空气与呼出气体中CO2含量 - B.
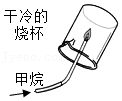 验证甲烷中含有氢元素
验证甲烷中含有氢元素 - C.
 验证可燃物燃烧的条件
验证可燃物燃烧的条件 - D.
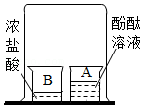 验证分子是运动的
验证分子是运动的
10.资料:①Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物;
②已知Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃。实验室有氢氧化铜和碳酸铜的固体混合物。设其组成为aCu(OH)2•bCuCO3,小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,下列说法正确的是( )
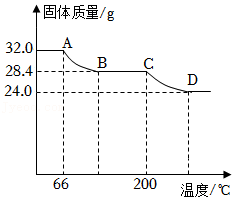
②已知Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃。实验室有氢氧化铜和碳酸铜的固体混合物。设其组成为aCu(OH)2•bCuCO3,小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,下列说法正确的是( )

- A. BC段的固体为纯净物
- B. b:a=2:1
- C. 往32.0g的固体中加入足量的稀盐酸,会生成CO2的质量为8.0g
- D. 反应过程中元素的化合价不变
11.建立宏观与微观之间的联系,是化学学科特有的思维方式。
(1)如图甲是钙元素在元素周期表中的相关信息,图乙是几种常见的原子结构示意图。
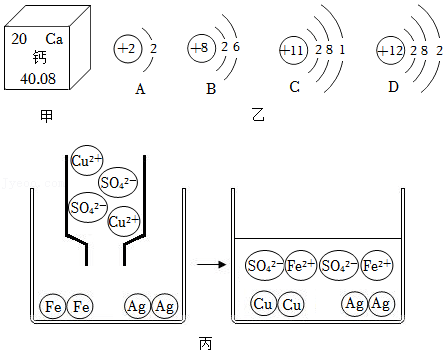
①由图甲可知,钙元素原子核内质子数为 。
②钙原子在化学反应中易 (填“失去”或“得到”)电子,其化学性质与图乙中的 (填字母)微粒的化学性质相似。
③钙是人体必需的 (填“常量”或“微量”)元素。人体缺钙易引起的疾病有 。
(2)将硫酸铜溶液与烧杯中Fe、Ag两种金属相混合,微观变化情况如图丙:则变化过程中的微观反应实质是 ,并写出本质相同的另一个化学反应方程式 (反应物之一必须为铁)。
(1)如图甲是钙元素在元素周期表中的相关信息,图乙是几种常见的原子结构示意图。

①由图甲可知,钙元素原子核内质子数为 。
②钙原子在化学反应中易 (填“失去”或“得到”)电子,其化学性质与图乙中的 (填字母)微粒的化学性质相似。
③钙是人体必需的 (填“常量”或“微量”)元素。人体缺钙易引起的疾病有 。
(2)将硫酸铜溶液与烧杯中Fe、Ag两种金属相混合,微观变化情况如图丙:则变化过程中的微观反应实质是 ,并写出本质相同的另一个化学反应方程式 (反应物之一必须为铁)。
12.工业上利用生产钛白的副产品硫酸亚铁制备还原铁粉的流程如图:
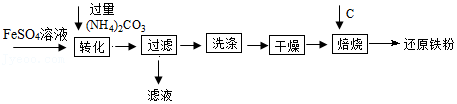
(1)“转化”时在溶液中生成了FeCO3沉淀,该反应的基本类型是 ;
(2)“过滤”用到的玻璃仪器有烧杯、 ,滤液中含有的物质是 ;
(3)“洗涤”时如何判断沉淀已洗涤干净,你的方法是 ;
(4)“干燥”过程中有少量的FeCO3在加热条件下与水和氧气反应生成FeOOH和CO2,此过程的化学方程式为 ;FeCO3和FeOOH在空气中焙烧转化为Fe2O3,Fe2O3在高温条件下与C反应生成Fe,此过程体现了碳的 性;
(4)制得的还原铁粉中含有Fe和少量FexC,为确定FexC的化学式,进行如下实验:
①取56.24g还原铁粉在氧气流中充分加热,得到0.88g CO2;
②另取相同质量的还原铁粉与足量稀硫酸充分反应(FexC与稀硫酸不反应),得到1.92g H2,则FexC的化学式是 。

(1)“转化”时在溶液中生成了FeCO3沉淀,该反应的基本类型是 ;
(2)“过滤”用到的玻璃仪器有烧杯、 ,滤液中含有的物质是 ;
(3)“洗涤”时如何判断沉淀已洗涤干净,你的方法是 ;
(4)“干燥”过程中有少量的FeCO3在加热条件下与水和氧气反应生成FeOOH和CO2,此过程的化学方程式为 ;FeCO3和FeOOH在空气中焙烧转化为Fe2O3,Fe2O3在高温条件下与C反应生成Fe,此过程体现了碳的 性;
(4)制得的还原铁粉中含有Fe和少量FexC,为确定FexC的化学式,进行如下实验:
①取56.24g还原铁粉在氧气流中充分加热,得到0.88g CO2;
②另取相同质量的还原铁粉与足量稀硫酸充分反应(FexC与稀硫酸不反应),得到1.92g H2,则FexC的化学式是 。
13.请利用化学知识分析回答下列问题。
Ⅰ:用化学学学科观点认识物质。
(1)科学家最新研制出5个氮原子构成的带一个单位正电荷的原子团 (填符号)。
(2)人体胃液中含有适量的盐酸,在医疗上可用碳酸氢钠治疗胃酸过多症,是因为: (用化学方程式表示)。
(3)我国在可燃冰开采领域取得重大突破,可燃冰主要成分是甲烷水合物,化学式为CH4•8H2O。甲烷水合物燃烧的化学方程式为 。为防止燃气泄漏造成危险,使用天然气的家庭报警器应安装在燃气灶附近墙壁的 (填“上”或“下”)方。
(4)月球土壤中有天然的铁、铝、银等金属颗粒。根据铁锈蚀的条件分析,铁在月球上不易锈蚀的原因可能是 。
Ⅱ:化学材料的使用方便了人类的生活。
(5)食品包装袋一般是塑料制品,通常采用热封口,原因是该塑料具有 (填“热塑性”或“热固性”)。
(6)新冠肺炎防疫期间,常用75%酒精溶液消毒,在室内不要喷洒过多,因为酒精遇到明火易发生燃烧或爆炸,从燃烧的条件分析,明火起到的作用是 。
Ⅰ:用化学学学科观点认识物质。
(1)科学家最新研制出5个氮原子构成的带一个单位正电荷的原子团 (填符号)。
(2)人体胃液中含有适量的盐酸,在医疗上可用碳酸氢钠治疗胃酸过多症,是因为: (用化学方程式表示)。
(3)我国在可燃冰开采领域取得重大突破,可燃冰主要成分是甲烷水合物,化学式为CH4•8H2O。甲烷水合物燃烧的化学方程式为 。为防止燃气泄漏造成危险,使用天然气的家庭报警器应安装在燃气灶附近墙壁的 (填“上”或“下”)方。
(4)月球土壤中有天然的铁、铝、银等金属颗粒。根据铁锈蚀的条件分析,铁在月球上不易锈蚀的原因可能是 。
Ⅱ:化学材料的使用方便了人类的生活。
(5)食品包装袋一般是塑料制品,通常采用热封口,原因是该塑料具有 (填“热塑性”或“热固性”)。
(6)新冠肺炎防疫期间,常用75%酒精溶液消毒,在室内不要喷洒过多,因为酒精遇到明火易发生燃烧或爆炸,从燃烧的条件分析,明火起到的作用是 。
14.某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的SO2[Na2SO3+H2SO4(浓)═Na2SO4+SO2↑+H2O]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
【提出问题】①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
【查阅资料】
1.Na2SO3有较强还原性,在空气中易被氧气氧化:2Na2SO3+O2═2Na2SO4;
2.Na2SO3能与酸反应产生SO2气体;
3.SO32﹣、SO42﹣均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(1)【作出猜想】猜想1:没有变质,成分是Na2SO3;
猜想2:完全变质,成分是Na2SO4;
猜想3: 。
【实验探究1】甲组设计实验探究溶液是否变质:
(2)溶液中含有
(3)
(4)实验结论是 。
【实验探究2】乙组设计如图实验测定Na2SO3溶液的溶质质量分数。

(5)连好装置并 (填操作),在锥形瓶中放入126g该样品,通入氮气。
称量C装置的质量为128.8g。
(6)关闭活塞K,用注射器推入浓硫酸至不再产生气泡,注射器可以换为 ,也能控制液体试剂的滴加速率。
打开活塞K,再缓缓鼓入一定量的氮气。
再次称量C装置的质量为135.2g。
(7)计算出该溶液中Na2SO3的质量分数为 。若不通入氮气,实验结果将 (填“偏大”“不变”或“偏小”)。
(8)【总结反思】由此可得出,保存亚硫酸钠时应 。
【提出问题】①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
【查阅资料】
1.Na2SO3有较强还原性,在空气中易被氧气氧化:2Na2SO3+O2═2Na2SO4;
2.Na2SO3能与酸反应产生SO2气体;
3.SO32﹣、SO42﹣均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(1)【作出猜想】猜想1:没有变质,成分是Na2SO3;
猜想2:完全变质,成分是Na2SO4;
猜想3: 。
【实验探究1】甲组设计实验探究溶液是否变质:
| 步骤 | 实验操作 | 现象 | 结论 |
| 步骤1 | 取少量样品于试管中加入过量稀盐酸; | 产生气泡 | (2)溶液中含有________ |
| 步骤2 | 在步骤1试管中继续滴加BaCl2溶液。 | (3)________ | 溶液中含有Na2SO4 |
(2)溶液中含有
(3)
(4)实验结论是 。
【实验探究2】乙组设计如图实验测定Na2SO3溶液的溶质质量分数。

(5)连好装置并 (填操作),在锥形瓶中放入126g该样品,通入氮气。
称量C装置的质量为128.8g。
(6)关闭活塞K,用注射器推入浓硫酸至不再产生气泡,注射器可以换为 ,也能控制液体试剂的滴加速率。
打开活塞K,再缓缓鼓入一定量的氮气。
再次称量C装置的质量为135.2g。
(7)计算出该溶液中Na2SO3的质量分数为 。若不通入氮气,实验结果将 (填“偏大”“不变”或“偏小”)。
(8)【总结反思】由此可得出,保存亚硫酸钠时应 。
15.某化肥由(NH4)2SO4、NH4NO3、KCl混合而成,对提高作物产量有重要作用。
(1)该化肥施用后,植物无法达到的效果是 (填序号)。
A.茎叶生长茂盛
B.增强抗寒抗旱能力
C.增强抗倒伏,抗虫害能力
(2)(NH4)2SO4中N、S、O三种元素的质量比为 (最简整数比)。
(3)为测定该化肥样品中氮元素的质量分数,小王和小李分别按自己设计的方案进行了实验。
方案1:小王取10.0g样品溶于水,加入足量的BaCl2溶液,充分反应后,过滤、洗涤、干燥、称量得固体质量为13.98g。
方案2:小李另取等质量的样品,加入足量的Ca(OH)2加热,将气体通过氢氧化钠固体和浓硫酸,氢氧化钠固体增重2.88g,浓硫酸增重2.72g(假设气体全部吸收)。
请你用方案1计算该化肥样品中氮元素的质量分数。
上述方案中较合理的 ,理由是
(1)该化肥施用后,植物无法达到的效果是 (填序号)。
A.茎叶生长茂盛
B.增强抗寒抗旱能力
C.增强抗倒伏,抗虫害能力
(2)(NH4)2SO4中N、S、O三种元素的质量比为 (最简整数比)。
(3)为测定该化肥样品中氮元素的质量分数,小王和小李分别按自己设计的方案进行了实验。
方案1:小王取10.0g样品溶于水,加入足量的BaCl2溶液,充分反应后,过滤、洗涤、干燥、称量得固体质量为13.98g。
方案2:小李另取等质量的样品,加入足量的Ca(OH)2加热,将气体通过氢氧化钠固体和浓硫酸,氢氧化钠固体增重2.88g,浓硫酸增重2.72g(假设气体全部吸收)。
请你用方案1计算该化肥样品中氮元素的质量分数。
上述方案中较合理的 ,理由是
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解