下载高清试卷
【2022年黑龙江省绥化市中考化学一模试卷】-第1页
试卷格式:2022年黑龙江省绥化市中考化学一模试卷.PDF
试卷热词:最新试卷、2022年、黑龙江试卷、绥化市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.下列化学实验操作中错误的是( )
- A.
 称取固体
称取固体 - B.
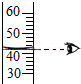 量取液体
量取液体 - C.
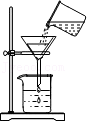 过滤
过滤 - D.
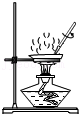 蒸发
蒸发
2.下列物质的用途和性质对应关系错误的是( )
- A. 钨——作灯丝——熔点高
- B. 一氧化碳——冶炼金属——可燃性
- C. 氮气——作保护气——化学性质不活泼
- D. 二氧化碳——人工降雨——固体升华时吸热
3.下列变化一定属于化学变化的是( )
- A. 固体碘受热升华
- B. 酒精挥发
- C. 葡萄酿酒
- D. 工业制取氧气
4.下列实验现象叙述正确的是( )
- A. 铁钉放入硫酸铜溶液中,溶液由蓝色变为浅绿色
- B. 红磷在空气中燃烧,产生大量白色烟雾
- C. 将空气中燃着的硫伸入氧气瓶中,火焰由黄色变为蓝紫色
- D. 氯化铁溶液和氢氧化钠溶液反应生成红褐色的氢氧化铁沉淀
5.下列物质分别属于单质、混合物、化合物的是( )
- A. 水、石灰石、小苏打
- B. 氧气、空气、干冰
- C. 氮气、五氧化二磷、稀盐酸
- D. 氨气、乙醇、食盐
6.苏州的“碧螺春”享誉全国.“碧螺春”茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46.下列说法错误的是( )
- A. 单宁酸由碳、氢、氧三种元素组成
- B. 单宁酸中氢元素的质量分数最小
- C. 一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成
- D. 单宁酸中碳、氧元素的质量比为57:23
7.善于归纳知识,利于培养素质。下面是某同学对部分化学知识的归纳,其中有不正确的一组是( )
| A.化学与健康 | B.实验记录 |
| ①人体缺铁会引起贫血症②多吃水果蔬菜利于补充维生素③用活性炭净水器可净化饮用水 | ①用10mL量筒量取7.25mL 水②用pH试纸测得苹果汁的pH为3.2③用托盘天平称取5.6g铁粉 |
| C.化学与能源 | D.安全常识 |
| ①煤、石油、天然气﹣﹣不可再生的化石燃料②风能、水能、太阳能﹣﹣未充分利用的绿色能源③使用氢能源﹣﹣可以缓解温室效应,减少酸雨 | ①厨房煤气管漏气﹣﹣关闭阀门并开窗通风②实验时碰倒酒精灯着火﹣﹣用湿抹布盖灭③冬天用煤炉取暖﹣﹣保证室内通风 |
- A. A
- B. B
- C. C
- D. D
8.下列各组物质分别加入到足量的水中,能共存且得到无色透明溶液的是( )
- A. KOH HNO3 NH4Cl
- B. K2CO3 Ba(NO3)2 NaCl
- C. KNO3 HCl NaNO3
- D. FeCl3 NaNO3 KCl
9.推理是化学学习常用的思维方法。下列推理中不正确的是( )
- A. 饱和溶液析出晶体后溶质减少,则溶质的质量分数一定变小
- B. 金属与酸反应中固体逐渐溶解,则反应后溶液的质量一定变大
- C. 化学反应中元素化合价不一定发生改变,则置换反应前后元素的化合价不一定发生改变
- D. 某物质在氧气中燃烧生成CO2和H2O,则该物质中一定含有碳元素和氢元素
10.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
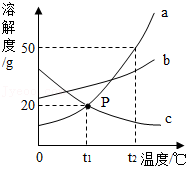

- A. P点表示t1℃时,a、c饱和溶液中溶质质量相等
- B. 将c的不饱和溶液变为饱和溶液,可采用降温的方法
- C. t2℃时等质量的三种物质的饱和溶液降温至t1℃,所得溶液中溶剂质量大小关系为:c>b>a
- D. 将t1℃时a、b、c三种物质的溶液分别升温至t2℃,其溶质质量分数都不可能发生变化
11.下列实验方案不能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别尿素和氯化铵 | 取样后加熟石灰研磨,闻气味 |
| B | 区别棉纤维和羊毛纤维 | 抽丝灼烧,闻气味 |
| C | 除去氢氧化钠溶液中的碳酸钠 | 加适量氢氧化钙溶液充分反应后过滤 |
| D | 除去氯化钙固体中的碳酸钙 | 加足量的水溶解、过滤、洗涤、干燥 |
- A. A
- B. B
- C. C
- D. D
12.下面是对四个实验绘制的图形,其中实验结果与图形对应准确的是( )
- A.
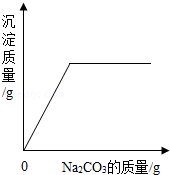 向一定量的稀盐酸和氯化钙混合溶液中不断滴入碳酸钠溶液至过量
向一定量的稀盐酸和氯化钙混合溶液中不断滴入碳酸钠溶液至过量 - B.
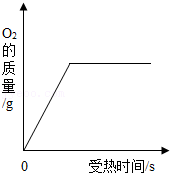 给氯酸钾和二氧化锰的混合物加热制氧气
给氯酸钾和二氧化锰的混合物加热制氧气 - C.
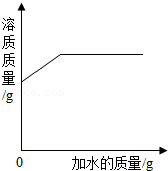 向饱和的氯化钠溶液中不断加水
向饱和的氯化钠溶液中不断加水 - D.
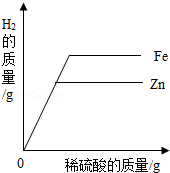 等质量的锌、铁与足量的相同溶质质量分数的稀硫酸反应
等质量的锌、铁与足量的相同溶质质量分数的稀硫酸反应
13.请用化学用语填空。
(1)不含金属元素的碱 。
(2)标出高锰酸钾中锰元素的化合价 。
(1)不含金属元素的碱 。
(2)标出高锰酸钾中锰元素的化合价 。
14.生活与化学息息相关,请用学过的化学知识回答下列问题。
(1)合理膳食有益健康,牛肉富含的营养素是 。
(2)天然水多为硬水,生活中可通过 方法使其转化为软水。
(3)农作物出现倒伏现象,应该施用下列化肥中的 。
A.尿素
B.硝酸铵
C.碳酸钾
D.磷酸二氢铵
(4)火箭发射的液体推进剂为偏二甲肼(C2H8N2)和四氧化二氮,发射时发生如下反应:C2H8N2+2N2O4═3N2+2X+4H2O,其中X的化学式为 。
(1)合理膳食有益健康,牛肉富含的营养素是 。
(2)天然水多为硬水,生活中可通过 方法使其转化为软水。
(3)农作物出现倒伏现象,应该施用下列化肥中的 。
A.尿素
B.硝酸铵
C.碳酸钾
D.磷酸二氢铵
(4)火箭发射的液体推进剂为偏二甲肼(C2H8N2)和四氧化二氮,发射时发生如下反应:C2H8N2+2N2O4═3N2+2X+4H2O,其中X的化学式为 。
15.宏观元素和微观粒子是化学中重要的问题。请回答下列问题。
(1)如图中,①是钠元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图:
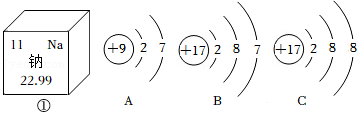
①钠元素的原子序数为 。
②A和B两种粒子的 相同,所以它们有相似的化学性质。
③C所表示的粒子是(填“原子”或“离子”) 。
(2)在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如图所示。下列说法错误的是 。
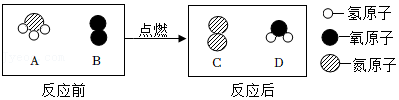
A.该反应为置换反应
B.反应前后各元素的质量不变
C.反应中生成C和D的质量比为14:27
D.该反应中A与B的化学计量数之比为3:4
(1)如图中,①是钠元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图:
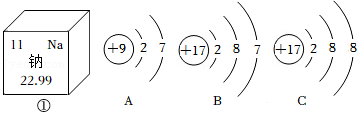
①钠元素的原子序数为 。
②A和B两种粒子的 相同,所以它们有相似的化学性质。
③C所表示的粒子是(填“原子”或“离子”) 。
(2)在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如图所示。下列说法错误的是 。

A.该反应为置换反应
B.反应前后各元素的质量不变
C.反应中生成C和D的质量比为14:27
D.该反应中A与B的化学计量数之比为3:4
16.金属和金属材料和人类生活、生产密切相关,
(1)铁生锈是铁与空气中的 共同接触。
(2)下列材料:金刚石、玻璃钢、不锈钢属于金属材料的是 。
(3)在某次实验课上,小东同学把一包铁粉和镁粉的混合物放入一定量的AgNO3溶液中,使其充分反应后过滤,得到滤渣和浅绿色滤液,据此回答下列问题:
①滤渣中可能含有 (填化学式,下同)。
②滤液中可能含有的溶质是 。
(1)铁生锈是铁与空气中的 共同接触。
(2)下列材料:金刚石、玻璃钢、不锈钢属于金属材料的是 。
(3)在某次实验课上,小东同学把一包铁粉和镁粉的混合物放入一定量的AgNO3溶液中,使其充分反应后过滤,得到滤渣和浅绿色滤液,据此回答下列问题:
①滤渣中可能含有 (填化学式,下同)。
②滤液中可能含有的溶质是 。
17.A~E是初中化学常见的物质,其中 E是大理石的主要成分,B用于玻璃、造纸、纺织和洗涤剂的生产。A、B、C、D分别是氧化物、酸、碱、盐中的一种。(图中“—”表示相连物质间能发生反应,“→”表示物质间有相应的转化关系)请回答下列问题。
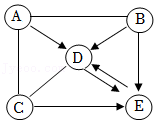
(1)B的化学式: 。
(2)写出C→E的化学方程式 。
(3)A的物质类别是 。(填“酸”“碱”“盐”或“氧化物”)
(4)D的一种用途 。

(1)B的化学式: 。
(2)写出C→E的化学方程式 。
(3)A的物质类别是 。(填“酸”“碱”“盐”或“氧化物”)
(4)D的一种用途 。
18.同学们将初中所学习的常见气体的制取与性质相关知识进行整理。请根据如图回答问题。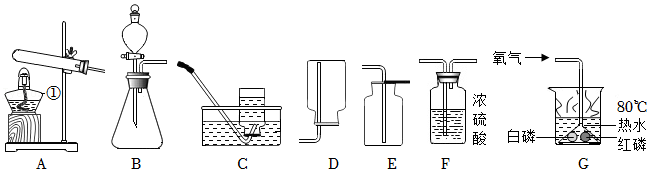
(1)写出标号①仪器的名称: 。
(2)实验室制取二氧化碳应选用的装置是 (填字母),反应的化学方程式为 。用A装置制氧气,反应的化学方程式为 。试管口略向下倾斜的原因 。
(3)若将B和C或B和E连接均可制取某种气体,则分液漏斗中应装的药品为 ,若用C装置收集气体,当观察到 时,则该气体已收集满;若要制取干燥的氧气,装置的连接顺序为:发生装置→ 。(用字母和箭头表示)
(4)将制得的氧气通入装置G中,发现只有白磷燃烧,对比通氧气前后白磷与红磷的现象,说明可燃物燃烧需要满足的条件是 。

(1)写出标号①仪器的名称: 。
(2)实验室制取二氧化碳应选用的装置是 (填字母),反应的化学方程式为 。用A装置制氧气,反应的化学方程式为 。试管口略向下倾斜的原因 。
(3)若将B和C或B和E连接均可制取某种气体,则分液漏斗中应装的药品为 ,若用C装置收集气体,当观察到 时,则该气体已收集满;若要制取干燥的氧气,装置的连接顺序为:发生装置→ 。(用字母和箭头表示)
(4)将制得的氧气通入装置G中,发现只有白磷燃烧,对比通氧气前后白磷与红磷的现象,说明可燃物燃烧需要满足的条件是 。
19.有一包白色粉末,可能含有氢氧化钠、碳酸钠、氯化钙、碳酸钙中的一种或几种。为了确定其成分,某兴趣小组进行了如下实验(微溶性物质按可溶处理)。
【查阅资料】氯化钡溶液呈中性。
【实验探究】
实验一:取一定量白色粉末放入烧杯中,加入足量水,搅拌,静置,观察到烧杯中有白色不溶物。由此小明得出白色粉末中一定含有碳酸钙。
(1)【讨论交流】有的同学对小明的结论提出了质疑,认为其结论不一定正确,理由是 (用化学方程式表示)。
实验二:为进一步确定白色粉末成分,继续进行实验。
(2)白色粉末中一定含有
(3)
(4)【实验结论】综合以上探究,同学们通过讨论确定了白色粉末的组成,其可能的组成有 种情况。
【反思评价】
(5)步骤Ⅰ中加入过量的氯化钡溶液的目的是 。
(6)下列物质能替代步骤Ⅱ中酚酞溶液达到实验目的的是 (填序号)。
①石蕊溶液
②氧化铜
③二氧化碳
④硫酸镁溶液
⑤稀盐酸
【查阅资料】氯化钡溶液呈中性。
【实验探究】
实验一:取一定量白色粉末放入烧杯中,加入足量水,搅拌,静置,观察到烧杯中有白色不溶物。由此小明得出白色粉末中一定含有碳酸钙。
(1)【讨论交流】有的同学对小明的结论提出了质疑,认为其结论不一定正确,理由是 (用化学方程式表示)。
实验二:为进一步确定白色粉末成分,继续进行实验。
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤Ⅰ:取实验一中的上层清液少量于试管中,加入过量的氯化钡溶液,过滤 | 产生白色沉淀 | (2)白色粉末中一定含有________ |
| 步骤Ⅱ:取步骤Ⅰ中的滤液少量于试管中,滴加酚酞溶液 | (3)________ | 白色粉末中一定含有氢氧化钠 |
(2)白色粉末中一定含有
(3)
(4)【实验结论】综合以上探究,同学们通过讨论确定了白色粉末的组成,其可能的组成有 种情况。
【反思评价】
(5)步骤Ⅰ中加入过量的氯化钡溶液的目的是 。
(6)下列物质能替代步骤Ⅱ中酚酞溶液达到实验目的的是 (填序号)。
①石蕊溶液
②氧化铜
③二氧化碳
④硫酸镁溶液
⑤稀盐酸
20.铜、铁是人类使用最早、应用广泛的金属。
【探究一】
(1)铁生锈主要跟空气中的 有关,用稀硫酸除铁锈的化学方程式为 。
(2)小茜同学发现自己的铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称“铜绿”,主要成分为Cu2(OH)2CO3,该反应的化学方程式为:2Cu+O2+H2O+X═Cu2(OH)2CO3,则X的化学式为 。
【探究二】
以黄铜矿(CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,原理为:
4CuFeS2+17O2+2H2SO4
4CuSO4+2Fe2(SO4)3+2H2O,向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu。
(3)CuFeS2为二硫化亚铁铜,也可以表示为CuS•FeS,其中S元素的化合价为 。
(4)发生主要反应的两个化学方程式为:①Fe+Fe2(SO4)3=3FeSO4; ② 。
(5)FeSO4溶液经蒸发浓缩、 、过滤等操作得到硫酸亚铁晶体(FeSO4•xH2O)。
【探究三】
硫酸亚铁晶体(FeSO4•xH2O)是一种重要的食品和饲料添加剂,对其进行热分解研究。
【查阅资料】①硫酸铜粉末为白色,吸水后变成蓝色晶体。
②二氧化硫能使高锰酸钾溶液褪色
③硫酸亚铁晶体加热会先失去结晶水,高温会继续分解产生一种金属氧化物和两种非金属氧化物。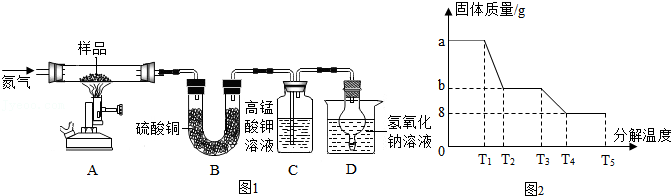
称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出x的值。
(6)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有 ,装置C中高锰酸钾溶液褪色,说明产物中还有 ;装置D球形干燥管的作用 ;实验中要持续通入氮气,否则测出的x会 (填“偏大”、“偏小”或“不变”)。
(7)硫酸亚铁晶体完全分解后,装置A中残留红棕色固体,另从理论上分析得出硫酸亚铁分解还生成另一物质SO3,写出FeSO4分解的化学方程式 。
(8)某研究所利用热分析仪对硫酸亚铁晶体(FeSO4•xH2O)进行热分解,获得相关数据,绘制成固体质量﹣﹣分解温度的关系图如图2,根据图2中有关数据,可计算出FeSO4•xH2O中的x= 。
【探究一】
(1)铁生锈主要跟空气中的 有关,用稀硫酸除铁锈的化学方程式为 。
(2)小茜同学发现自己的铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称“铜绿”,主要成分为Cu2(OH)2CO3,该反应的化学方程式为:2Cu+O2+H2O+X═Cu2(OH)2CO3,则X的化学式为 。
【探究二】
以黄铜矿(CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,原理为:
4CuFeS2+17O2+2H2SO4
| 耐酸、铜细菌 |
(3)CuFeS2为二硫化亚铁铜,也可以表示为CuS•FeS,其中S元素的化合价为 。
(4)发生主要反应的两个化学方程式为:①Fe+Fe2(SO4)3=3FeSO4; ② 。
(5)FeSO4溶液经蒸发浓缩、 、过滤等操作得到硫酸亚铁晶体(FeSO4•xH2O)。
【探究三】
硫酸亚铁晶体(FeSO4•xH2O)是一种重要的食品和饲料添加剂,对其进行热分解研究。
【查阅资料】①硫酸铜粉末为白色,吸水后变成蓝色晶体。
②二氧化硫能使高锰酸钾溶液褪色
③硫酸亚铁晶体加热会先失去结晶水,高温会继续分解产生一种金属氧化物和两种非金属氧化物。

称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出x的值。
(6)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有 ,装置C中高锰酸钾溶液褪色,说明产物中还有 ;装置D球形干燥管的作用 ;实验中要持续通入氮气,否则测出的x会 (填“偏大”、“偏小”或“不变”)。
(7)硫酸亚铁晶体完全分解后,装置A中残留红棕色固体,另从理论上分析得出硫酸亚铁分解还生成另一物质SO3,写出FeSO4分解的化学方程式 。
(8)某研究所利用热分析仪对硫酸亚铁晶体(FeSO4•xH2O)进行热分解,获得相关数据,绘制成固体质量﹣﹣分解温度的关系图如图2,根据图2中有关数据,可计算出FeSO4•xH2O中的x= 。
21.按要求回答下列问题。
(1)新冠肺炎疫情期间,为了做好自我防护,可用酒精溶液消毒,乙醇俗称酒精(化学式为C2H5OH)。
①乙醇分子中C、H、O原子个数比为 。
②92g乙醇中碳元素的质量为 。
(2)请根据如图所示的实验过程和提供的数据。解答下列问题。
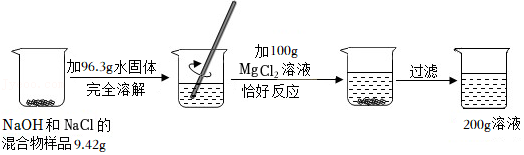
①写出该反应的化学方程式 。
②实验过程中,产生沉淀的质量为 g。
③设反应中生成氯化钠的质量为x,原固体中氢氧化钠的质量为y,列出求解生成氯化钠质量的比例式为 ;列出求解原固体中氢氧化钠质量的比例式为 。
④最终所得溶液中溶质的质量分数 。
(1)新冠肺炎疫情期间,为了做好自我防护,可用酒精溶液消毒,乙醇俗称酒精(化学式为C2H5OH)。
①乙醇分子中C、H、O原子个数比为 。
②92g乙醇中碳元素的质量为 。
(2)请根据如图所示的实验过程和提供的数据。解答下列问题。

①写出该反应的化学方程式 。
②实验过程中,产生沉淀的质量为 g。
③设反应中生成氯化钠的质量为x,原固体中氢氧化钠的质量为y,列出求解生成氯化钠质量的比例式为 ;列出求解原固体中氢氧化钠质量的比例式为 。
④最终所得溶液中溶质的质量分数 。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解