下载高清试卷
【2020年安徽省六区联考中考化学二模试卷】-第1页
试卷格式:2020年安徽省六区联考中考化学二模试卷.PDF
试卷热词:最新试卷、2020年、安徽试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.化学与人类生活密切相关,下列情况会对人体健康造成较大危害的是( )
- A. 用食醋清洗热水瓶内胆的水垢
- B. 用小苏打发面制作馒头
- C. 为了预防龋齿,使用含氟牙膏
- D. 用工业食盐腌制咸菜
2.联合国决议将每年的4月22日定为“世界地球日”.活动旨在唤起人类爱护地球、保护家园的意识,以促进资源开发与环境保护的协调发展,进而改善地球的整体环境,下列不符合主旨的做法是( )
- A. 垃圾分类回收处理,保护自然生态环境
- B. 禁止使用化石燃料,以减少雾霾的形成
- C. 合理开采和利用稀土资源,保障科学发展
- D. 促进生态文明,共建美丽中国
3.2020年,《中国诗词大会》再次如约而至,该节目弘扬了中华传统诗词之美,促进中华传统文化的继承和发扬。下列古诗词只涉及物理变化的是( )
- A. 千锤万凿出深山,烈火焚烧若等闲
- B. 有麝自来香,不用大风扬
- C. 白日登山望烽火,黄昏饮马傍交河
- D. 粉骨碎身浑不怕,要留清白在人间
4.如图所示实验操作不正确的是( )
- A.
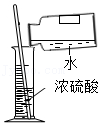 稀释浓硫酸
稀释浓硫酸 - B.
 蒸发食盐水
蒸发食盐水 - C.
 测定溶液的pH
测定溶液的pH - D.
 监控氧气的流速
监控氧气的流速
5.为了纪念元素周期表诞生150周年,如图是中国新命名的中文名新元素。下列有关说法正确的是( )
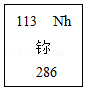

- A. 属于非金属元素
- B. 原子核内中子数为173
- C. 该物质单质的化学式为Nh2
- D. 相对原子质量为286g
6.今年,在对抗新型冠状病毒的战役中,科学家发现瑞德西韦这种药物对抵抗病毒有一定的作用,其化学式为C27H35N6O8P。下列有关瑞德西韦的叙述正确的是( )
- A. 不属于氧化物
- B. 瑞德西韦由77个原子构成
- C. 该物质完全燃烧的产物是二氧化碳和水
- D. 该分子中含有4个氧分子
7.甲和乙在一定条件下反应生成丙和丁。结合微观示意图分析,下列说法错误的是( )


- A. 反应前后原子的种类没有发生改变
- B. 参加反应的甲、乙的分子个数比为1:1
- C. 该反应中有一种有机物
- D. 反应前后都含有氧化物
8.模型建构是学习化学的重要方法之一,下列模型正确的是( )
 |  | 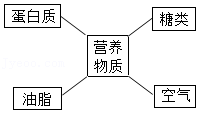 |  |
| A、溶液的酸碱性 | B、反应的关系 | C、重要的营养物质 | D、金属化学性质 |
- A. A
- B. B
- C. C
- D. D
9.学习化学,提高学科核心素养,学会从化学的角度分析问题。下列说法正确的是( )
- A. 溶液的特征是均一稳定,所以均一、稳定的液体一定是溶液
- B. 过氧化氢溶液能分解出氧气,是因为过氧化氢中含有氧分子
- C. 氦、氖等稀有气体化学性质比较稳定,是因为它们原子最外层都有8个电子
- D. 用木条蘸取少量浓硫酸,木条变黑,说明浓硫酸具有腐蚀性
10.以“铁氧化物”为催化剂,利用太阳能将CO2热解为碳和氧气,这一转化过程(如图),下列说法错误的是( )
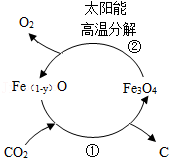

- A. 反应①中铁元素化合价升高
- B. 反应②属于分解反应
- C. 此反应可用于减少温室气体排放
- D. 太阳能热解CO2反应中催化剂没有参与化学反应
11.如表是NaCl、NH4Cl在不同温度时的溶解度。则下列说法正确的是( )
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| NaCl | 35.7g | 36.0g | 36.6g | 37.3g | 38.4g |
| NH4Cl | 29.4g | 37.2g | 45.8g | 55.2g | 65.6g |
- A. 两种物质的溶解度受温度影响较大的是NaCl
- B. 两物质的溶解度相等的温度范围在0﹣﹣20℃之间
- C. 20'C时,NaCl饱和溶液的溶质质量分数为36%
- D. 当NH4Cl中含有少量的NaCl时可以采取蒸发结晶的方式提纯NH4Cl
12.下列四个图象中能正确表示对应变化关系的是( )
- A.
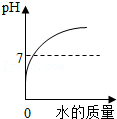 向一定量稀盐酸中加水稀释
向一定量稀盐酸中加水稀释 - B.
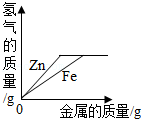 向足量的稀硫酸中分别加入等质量的锌粉和铁粉
向足量的稀硫酸中分别加入等质量的锌粉和铁粉 - C.
 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 - D.
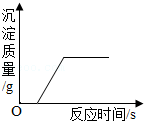 向氢氧化钠和氯化钡的混合溶液中逐渐加入稀硫酸
向氢氧化钠和氯化钡的混合溶液中逐渐加入稀硫酸
13.实验室常用下列装置来制取、收集气体,请回答以下问题。
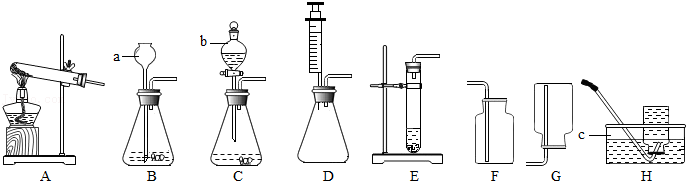
(1)写出标号仪器的名称:b ;
(2)装置C可用于实验室制取CO2,该反应的化学方程式是 ,选择该装置的优点是 。一般不使用H作为收集装置,其原因是 。
(3)要得到少量H2应选择的较简单的发生装置是 (填字母序号)。
(4)NH4Cl是一种常见的氮肥,在实验室中,可以利用NH4Cl和熟石灰固体共热制备氨气,则应该选用的发生装置是 。

(1)写出标号仪器的名称:b ;
(2)装置C可用于实验室制取CO2,该反应的化学方程式是 ,选择该装置的优点是 。一般不使用H作为收集装置,其原因是 。
(3)要得到少量H2应选择的较简单的发生装置是 (填字母序号)。
(4)NH4Cl是一种常见的氮肥,在实验室中,可以利用NH4Cl和熟石灰固体共热制备氨气,则应该选用的发生装置是 。
14.尿素[CO(NH2)2]是一种常用化肥。如图为利用天然气制尿素的主要流程。
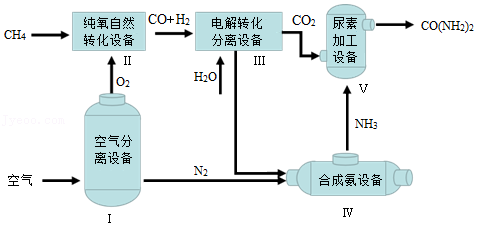
(1)NH3中氮元素的化合价是 ;流程中所涉及的氧化物有 (填1种即可)。
(2)设备Ⅲ中产生并分离出CO2和H2两种物质,依据流程图判断进入设备Ⅳ的是 。
(3)在一定条件下,设备V中发生反应生成尿素和一种常温下为液体的氧化物,写出相应的化学方程式: 。
(4)本流程中可以循环利用的物质是 ;利用空气和天然气作原料来生产尿素,你从中得到的启示是 。

(1)NH3中氮元素的化合价是 ;流程中所涉及的氧化物有 (填1种即可)。
(2)设备Ⅲ中产生并分离出CO2和H2两种物质,依据流程图判断进入设备Ⅳ的是 。
(3)在一定条件下,设备V中发生反应生成尿素和一种常温下为液体的氧化物,写出相应的化学方程式: 。
(4)本流程中可以循环利用的物质是 ;利用空气和天然气作原料来生产尿素,你从中得到的启示是 。
15.兴趣小组的同学对铝的某些性质进行相关探究。
(1)铝与稀盐酸反应。
请写出铝与稀盐酸反应的化学方程式为 。如图1是小倩将一根铝丝与过量的稀盐酸混合在一密闭容器内,利用压强和温度传感器测出的反应变化过程(上面是压强变化曲线、下面是温度变化曲线)。请解释:
①压强曲线AB段变化不明显的原因 ;
②BC段变化除生成气体外的另一原因 。

(2)铝与水能否反应
查阅资料:1.
(1)铝与稀盐酸反应。
请写出铝与稀盐酸反应的化学方程式为 。如图1是小倩将一根铝丝与过量的稀盐酸混合在一密闭容器内,利用压强和温度传感器测出的反应变化过程(上面是压强变化曲线、下面是温度变化曲线)。请解释:
①压强曲线AB段变化不明显的原因 ;
②BC段变化除生成气体外的另一原因 。

(2)铝与水能否反应
查阅资料:1.
| 物质 | 钠与水 | 铝与水 | 汞与水 |
| 能否发生反应 | 能反应 | 能反应 | 不反应 |
16.某化学兴趣小组同学用不同浓度的碳酸氢钠溶液和氯化钙溶液混合,出现不同的现象,如下:
①10g/L氯化钙+10g/L碳酸氢钠,有沉淀出现;
②5g/L氯化钙+8g/L碳酸氢钠,有沉淀出现;
③8g/L氯化钙+1g/L碳酸氢钠,无沉淀出现;
④1g/L氯化钙+8g/L碳酸氢钠,无沉淀出现。
【查阅资料】20℃,氯化钙的溶解度为74.5g;碳酸氢钙的溶解度为16.6g;氯化钠的溶解度为35.9g;碳酸氢钠的溶解度为9.6g。从溶解度来看,碳酸氢钠溶液和氯化钙溶液 (填“能”或“不能”)发生复分解反应。
【提出问题】碳酸氢钠溶液和氯化钙溶液反应产生的沉淀究竟是什么物质呢?
【猜想假设】猜想1:碳酸氢钙;猜想2:碳酸氢钠;猜想3:碳酸钙。
【实验探究】
【拓展研究】上述实验①中产生的气体是什么?
【交流讨论】上述实验,可以把这个反应理解为碳酸氢钙在浓度较高或者加热时发生分解。可知氯化钙溶液跟碳酸氢钠溶液反应的原理为CaCl2+2NaHCO3═ 。
【反思交流】1、实际实验中,鉴别碳酸钠和碳酸氢钠溶液 (填“可以”或“不可以”)选用氯化钙溶液;
2、饱和浓澄清石灰水,通入过量二氧化碳,现象为 。
①10g/L氯化钙+10g/L碳酸氢钠,有沉淀出现;
②5g/L氯化钙+8g/L碳酸氢钠,有沉淀出现;
③8g/L氯化钙+1g/L碳酸氢钠,无沉淀出现;
④1g/L氯化钙+8g/L碳酸氢钠,无沉淀出现。
【查阅资料】20℃,氯化钙的溶解度为74.5g;碳酸氢钙的溶解度为16.6g;氯化钠的溶解度为35.9g;碳酸氢钠的溶解度为9.6g。从溶解度来看,碳酸氢钠溶液和氯化钙溶液 (填“能”或“不能”)发生复分解反应。
【提出问题】碳酸氢钠溶液和氯化钙溶液反应产生的沉淀究竟是什么物质呢?
【猜想假设】猜想1:碳酸氢钙;猜想2:碳酸氢钠;猜想3:碳酸钙。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取3.0mL 10g/L碳酸氢钠于试管中,并向其中滴加5滴10g/L的氯化钙溶液 | 溶液中出现白色沉淀的同时又有持续性气泡产生 | |
| ②过滤,取少量沉淀于试管中,加入足量水 | 固体不溶解 | |
| ③再取少量沉淀,逐渐滴入稀盐酸 | 白色沉淀为碳酸钙 |
【拓展研究】上述实验①中产生的气体是什么?
| 实验步骤 | 实验现象 | 实验结论 |
| 重复实验①,再对浑浊液稍稍加热 | 溶液有气泡冒出,同时白色沉淀明显增加 | |
| 产生气体通入澄清石灰水 | 产生了CO2 |
【交流讨论】上述实验,可以把这个反应理解为碳酸氢钙在浓度较高或者加热时发生分解。可知氯化钙溶液跟碳酸氢钠溶液反应的原理为CaCl2+2NaHCO3═ 。
【反思交流】1、实际实验中,鉴别碳酸钠和碳酸氢钠溶液 (填“可以”或“不可以”)选用氯化钙溶液;
2、饱和浓澄清石灰水,通入过量二氧化碳,现象为 。
17.为测定某久置稀盐酸的溶质质量分数,取100g稀盐酸样品于烧杯中,逐滴加入质量分数为5%的氢氧化钠溶液,恰好完全反应时,用去80g氢氧化钠溶液。
(1)氢氧化钠中钠元素的质量分数是 。
(2)计算原稀盐酸的溶质质量分数为多少?
(1)氢氧化钠中钠元素的质量分数是 。
(2)计算原稀盐酸的溶质质量分数为多少?
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解