下载高清试卷
【2020年浙江省嘉兴市海宁市中考化学二模试卷】-第1页
试卷格式:2020年浙江省嘉兴市海宁市中考化学二模试卷.PDF
试卷热词:最新试卷、2020年、浙江试卷、嘉兴市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.从大量的事实中寻找共同特征,可归纳出实物的本质属性。下列结论正确的是( )
- A. 含有氧元素的化合物都是氧化物
- B. 含有氢元素的化合物都是酸
- C. 酸和碱反应都会生成水
- D. 带电的微粒都是离子
2.下表客观事实的微观解释正确的是( )
| 选项 | 客观事实 | 微观解释 |
| A. | 金属能导电 | 内部存在大量的自由电子 |
| B. | H2O在通电条件下产生H2 | H2O分子中有H2 |
| C. | 两块铅柱的端面锉平,用力压在一起,发现能粘合 | 原子之间有空隙 |
| D. | 蜡烛燃烧时,蜡烛的质量变轻 | 化学反应前后原子质量减轻 |
- A. A
- B. B
- C. C
- D. D
3.“绿水青山就是金山银山”,所以环境保护非常重要。
(1)酸雨是指pH小于5.6的降水。煤燃烧时重要排放出 (写化学式)等污染性气体,这些气体或气体在空气中发生反应后的生成物溶于水,会形成酸雨。
(2)PM2.5是指大气中微粒直径小于2.5μm的颗粒物。下列物质中能形成PM2.5的是 (填序号)。
A.焚烧秸秆
B.汽车尾气排放
C.太阳能发电
(3)“三效催化转换器”可将汽车尾气中的有毒气体转化为无污染的气体,如图是某个反应的微观示意图如图。请写出该反应的化学方程式 。
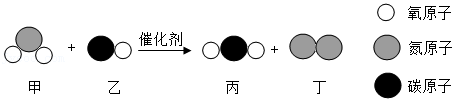
(1)酸雨是指pH小于5.6的降水。煤燃烧时重要排放出 (写化学式)等污染性气体,这些气体或气体在空气中发生反应后的生成物溶于水,会形成酸雨。
(2)PM2.5是指大气中微粒直径小于2.5μm的颗粒物。下列物质中能形成PM2.5的是 (填序号)。
A.焚烧秸秆
B.汽车尾气排放
C.太阳能发电
(3)“三效催化转换器”可将汽车尾气中的有毒气体转化为无污染的气体,如图是某个反应的微观示意图如图。请写出该反应的化学方程式 。

4.某校学习小组同学对锌与稀硫酸反应后的溶液中溶质成分进行探究。
【提出问题】锌与稀硫酸反应后溶液中溶质成分是什么?
【建立猜想】对反应后溶液中溶质成分进行如下猜想:
猜想一:硫酸和硫酸锌;
猜想二:硫酸锌。
【查阅资料】硫酸锌溶液的pH在5.2~5.4之间。
【实验验证】将上述锌与稀硫酸反应后的溶液均分成二等份,装入A、B二试管。
(1)为验证猜想一,小华向A试管液入紫色石蕊试液,试管中溶液红色,于是小华认为自己的猜想一是正确的。小明认为小华的实验不能证明猜想一,理由是 。
(2)为验证猜想二。小明取B试管,逐滴加入10%的Ba(OH)2溶液,得到如图的关系。请说明猜想二是否正确,并说明理由 。
【反思与交流】做好实验后,废液未经处理直接倒入下水道,可能造成的危害是 。

【提出问题】锌与稀硫酸反应后溶液中溶质成分是什么?
【建立猜想】对反应后溶液中溶质成分进行如下猜想:
猜想一:硫酸和硫酸锌;
猜想二:硫酸锌。
【查阅资料】硫酸锌溶液的pH在5.2~5.4之间。
【实验验证】将上述锌与稀硫酸反应后的溶液均分成二等份,装入A、B二试管。
(1)为验证猜想一,小华向A试管液入紫色石蕊试液,试管中溶液红色,于是小华认为自己的猜想一是正确的。小明认为小华的实验不能证明猜想一,理由是 。
(2)为验证猜想二。小明取B试管,逐滴加入10%的Ba(OH)2溶液,得到如图的关系。请说明猜想二是否正确,并说明理由 。
【反思与交流】做好实验后,废液未经处理直接倒入下水道,可能造成的危害是 。

5.花生,又名“长生果”等,因具有很高的营养价值而成为餐桌上常见的食品。某农场用如图所示的磷酸二氢钾(KH2PO4)晶体2包配制0.3%的溶液用于花生的增产,问需要加多少克水?(杂质不溶于水也不与水反应)


6.第26届国际计量大会决定将千克重新定义,并于2019年国际计量日(5月20日)起正式生效。原因是即便它是强抗氧化、耐腐蚀的铂铱合金且外加多重真空玻璃罩,国际千克原器(如图)的质量比1889年该大会批准时减少了约50毫克。
(1)铱元素由铱﹣191和铱﹣193两种同位素原子,两者的最本质区别是 不同。
(2)有科学家推断:减少的这50毫克质量可能是金属升华了。科学家的推断从微观角度分析是该铂铱合金的 减少。
(3)已知一个铂原子的原子质量为M kg,一个碳﹣12原子的质量为N kg,碳﹣12原子的
为标准,铂的相对原子质量是 (用含M、N的表达式表示)。

(1)铱元素由铱﹣191和铱﹣193两种同位素原子,两者的最本质区别是 不同。
(2)有科学家推断:减少的这50毫克质量可能是金属升华了。科学家的推断从微观角度分析是该铂铱合金的 减少。
(3)已知一个铂原子的原子质量为M kg,一个碳﹣12原子的质量为N kg,碳﹣12原子的
| 1 |
| 12 |

7.醋不仅是中国各大菜系中的传统的调味品,而且还具有抑菌杀菌、消除疲劳等功效。醋的主要成分是醋酸,其化学式为CH3COOH。
小明为判断厨房中4.5°的陈醋含酸量是否合格,取100mL陈醋(见标签)于锥形瓶中,然后向锥形瓶中缓慢加入一定溶质量分数的碳酸氢钠溶液,并用灵敏电子天平称出充分反应后锥形瓶内剩余物质的总质量,记录数据如下表。回答下列问题(化学方程式:CH3COOH+NaHCO3═CH3COONa+H2O+CO2↑)。
(1)生成物CH3COONa在物质分类上属于 (选填“酸”、“碱”或“盐”);实验中所用碳酸氢钠溶液的质量分数是 。
(2)分析表中数据可知,第几次实验醋酸已经完全反应?并分析理由: 。
(3)请通过计算判断该陈醋含酸量是否合格?(请写出详细的计算过程)
| XX牌酿造陈醋4.5°配料:水、糯米、麦麸、食用盐、白砂糖、大米总酸:≥4.5g/100mL密度:1g/mL保质期:5年贮存方法:阴凉、干燥、通风生产日期:见瓶盖 |
小明为判断厨房中4.5°的陈醋含酸量是否合格,取100mL陈醋(见标签)于锥形瓶中,然后向锥形瓶中缓慢加入一定溶质量分数的碳酸氢钠溶液,并用灵敏电子天平称出充分反应后锥形瓶内剩余物质的总质量,记录数据如下表。回答下列问题(化学方程式:CH3COOH+NaHCO3═CH3COONa+H2O+CO2↑)。
| 实验次数 | 一 | 二 | 三 | 四 | 五 |
| 加入碳酸氢钠溶液质量(g) | 40 | 80 | 120 | 125 | 160 |
| 锥形瓶内剩余物质总质量(g) | 138.9 | 177.8 | 216.7 | 221.7 | 256.7 |
(1)生成物CH3COONa在物质分类上属于 (选填“酸”、“碱”或“盐”);实验中所用碳酸氢钠溶液的质量分数是 。
(2)分析表中数据可知,第几次实验醋酸已经完全反应?并分析理由: 。
(3)请通过计算判断该陈醋含酸量是否合格?(请写出详细的计算过程)

8.为探究某石灰石的纯度,准确称取10g石灰石样品,缓慢加入一定浓度的稀盐酸至过量并依次记录四个不同时刻的相关数据,编号t1、t2、t3、t4.(方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑,杂质不溶于水也不参加反应)
请回答下列问题:
(1)该石灰石样品的纯度为 ;盐酸溶液的溶质质量分数为 。
(2)从上表相关数据分析,t3时刻所加入稀盐酸的总质量m至少为 g。
(3)为继续探究石灰石与稀盐酸反应后所得溶液中的溶质成分,将t3时刻所得溶液过滤,取滤液质量的
于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,生成沉淀质量的变化如图所示。求烧杯中A点处对应的溶液中溶质的质量是多少克?(写出计算过程)

| 反应时刻 | t1 | t2 | t3 | t4 |
| 加入稀盐酸的总质量 | 25g | 50g | m | 150g |
| 剩余固体的总质量 | 7.5g | 5g | 2g | 2g |
请回答下列问题:
(1)该石灰石样品的纯度为 ;盐酸溶液的溶质质量分数为 。
(2)从上表相关数据分析,t3时刻所加入稀盐酸的总质量m至少为 g。
(3)为继续探究石灰石与稀盐酸反应后所得溶液中的溶质成分,将t3时刻所得溶液过滤,取滤液质量的
| 1 |
| 4 |

查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解