下载高清试卷
【2022年广东省揭阳市中考化学一模试卷】-第1页
试卷格式:2022年广东省揭阳市中考化学一模试卷.PDF
试卷热词:最新试卷、2022年、广东试卷、揭阳市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.2022年2月4日20点,万众瞩目的第二十四届冬奥会在北京隆重开幕。在冬奥会开幕盛典中发生的化学变化是( )
- A. LED屏幕发光
- B. 点燃火炬
- C. 雕刻会徽
- D. 升起国旗
2.正确的实验操作对实验结果、人身安全都非常重要,下列实验操作正确的是( )
- A.

- B.
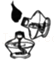
- C.

- D.

3.下列实验现象中,描述正确的是( )
- A. 木炭在氧气中燃烧,有无色刺激性气味气体生成
- B. 红磷在氧气中剧烈燃烧,有黄色火焰,有大量白色气体生成
- C. 镁条在空气中剧烈反应,发出耀眼的强光,生成白色固体
- D. 铁丝在空气中剧烈燃烧,放出大量的热,火星四射,有黑色熔融物溅落瓶底
4.下列符号中既表示一种元素,又表示一种原子,还可表示一种物质的是( )
- A. Cu
- B. N
- C. H
- D. O
5.《神农本草经》记载:“曾青,味酸小寒。主治目痛止泪,出风痹,利关节,通九窍,破症坚积聚。久服轻身不老。”曾青又叫朴青、层青,其为天然的硫酸铜(CuSO4)。其中硫元素的化合价为( )
- A. ﹣2
- B. +2
- C. +4
- D. +6
6.为强化地下水资源节约与保护,我国《地下水管理条例》自2021年12月1日起施行。下列说法或做法正确的是( )
- A. 可用活性炭吸附地下水中泥沙
- B. 利用高压泵把废水打入地下,避免污染河流
- C. 大力开采地下水,缓解水资源的短缺
- D. 利用化学技术,加强地下水监测
7.利用如图装置进行正确操作,来验证质量守恒定律。下列相关叙述中正确的是( )
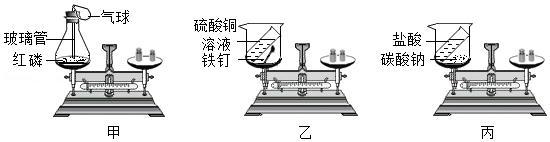

- A. 甲实验中可用少量水代替锥形瓶底部的细沙
- B. 丙实验中的化学反应不遵守质量守恒定律
- C. 乙实验中生成铜的质量等于参加反应的硫酸铜中铜元素的质量
- D. 充分反应后,冷却至室温,甲、乙、丙三个实验中的天平仍然都保持平衡
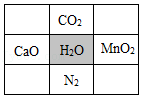
8.某同学设计化学“消消乐”游戏,点击灰色格,与该格中物质能反应的相邻物质就一起消失(反应条件为常温、加热或点燃),点击下图灰色格,剩余物质最少的是( )
- A.

- B.
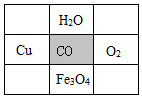
- C.
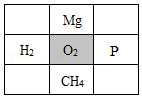
- D.
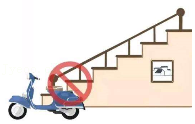
9.严禁在居民房楼道给电动车充电,否则具有极大的安全隐患。有以下说法:①可能引起电动车燃烧,会产生剧毒气体;②非常安全,不会出现事故;③可能引起爆炸;④可能造成短路、串电事故发生;⑤可能引起电池漏电。其中说法正确的是( )

- A. ①②⑤
- B. ①③④⑤
- C. ②④⑤
- D. 全部
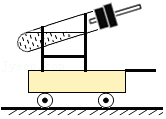
10.自制一个不使用电力的四轮小车(如图,往试管中加入一定量化学试剂,迅速塞紧单孔橡皮塞,反应产生气体对空气产生推力,空气对小车也产生等大反向推力,使小车在摩擦力很小的水平道路上运动。(已知:小车运动的快慢取决于产生气体的速度大小,小车运动距离的远近取决于产生气体量的多少)等质量的下列4种金属粉末和等质量等浓度足量的稀盐酸充分反应,能使小车运动得又快又远的金属是( )

- A. Mg
- B. Zn
- C. Fe
- D. Cu
11.小明用50℃的水泡了一杯蔗糖水,充分搅拌后,发现杯子底部还有部分蔗糖不能溶解。已知蔗糖的溶解度随温度的升高而增大。下列能使杯底的蔗糖继续溶解的方法是( )
- A. 把蔗糖水放入冰箱
- B. 给蔗糖水加热
- C. 往蔗糖水里继续加蔗糖
- D. 把蔗糖水放在通风处
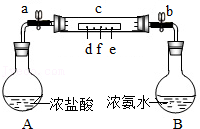
12.如图所示,烧瓶A中装的是浓盐酸(HCl气体的水溶液),烧瓶B中装的是浓氨水,长玻璃管C中间有一张滤纸条,每隔2cm滴有一滴无色酚酞溶液,实验前关闭开关a、b。实验开始同时打开开关a、b,看到滤纸大部分变红色,在玻璃管左端出现大量白烟(HCl与NH3相遇,生成NH4Cl固体)。下列有关说法正确的是( )

- A. 浓盐酸和浓氨水都易挥发
- B. 浓盐酸使酚酞溶液变红
- C. 该实验中,HCl分子比NH3分子运动快
- D. 实验过程中,酚酞分子没有运动
13.中考临近,小洁妈妈为了给小洁补充合适的蛋白质。她在给小洁做饭选材时应含的是( )
- A. 大白菜
- B. 鲈鱼
- C. 米饭
- D. 胡萝卜
14.下列离子在溶液中能大量共存的是( )
- A. K+、Na+、SO
、Cl﹣2- 4 - B. Na+、H+、NO
、CO- 3 2- 3 - C. NH
、K+、OH-、SO+ 4 2- 4 - D. Ag+、Mg2+、NO
、Cl﹣- 3
15.下列图象能正确反映对应变化的是( )
- A.
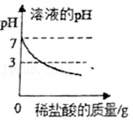 向水中加入pH=3的稀盐酸
向水中加入pH=3的稀盐酸 - B.
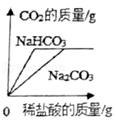 向等质量的碳酸钠、碳酸氢钠中加入等浓度的稀盐酸
向等质量的碳酸钠、碳酸氢钠中加入等浓度的稀盐酸 - C.
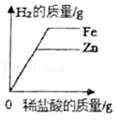 向等质量的铁粉、锌粉中分别加入等浓度的稀盐酸
向等质量的铁粉、锌粉中分别加入等浓度的稀盐酸 - D.
 向氢氧化钾、碳酸钾的混合溶液中滴加稀盐酸
向氢氧化钾、碳酸钾的混合溶液中滴加稀盐酸
16.“人间烟火,抚慰凡心”。疫情来袭,中国人仍可“医食无优”,岁月静好,是因为祖国的繁荣富强,国士的负重前行!
(1)疫情期间,外出一定要戴口罩。佩戴活性炭口罩有防毒、除臭、滤菌、阻尘等功效,这是利用活性炭的 性;
(2)测量体温,从微观角度看,水银体温计的原理是温度改变时 发生改变;
(3)治疗新冠肺炎的药物阿比多尔【其化学式为C22H25BrN2O3S】该物质中碳原子与氢原子的个数比为 ;该药物需遮光,密封保存的可能原因是 。
(4)84消毒液的有效成分是次氯酸钠(NaClO),电解饱和氯化钠溶液可制得次氯酸钠和一种可燃性气体,该反应的化学方程式为 。
(5)过氧乙酸(CH3COOOH)也是有效的消毒剂,某医疗小组用溶质质量分数为0.5%的过氧乙酸溶液200kg对环境进行消毒,需要溶质质量分数为20%的过氧乙酸溶液 kg。
(1)疫情期间,外出一定要戴口罩。佩戴活性炭口罩有防毒、除臭、滤菌、阻尘等功效,这是利用活性炭的 性;
(2)测量体温,从微观角度看,水银体温计的原理是温度改变时 发生改变;
(3)治疗新冠肺炎的药物阿比多尔【其化学式为C22H25BrN2O3S】该物质中碳原子与氢原子的个数比为 ;该药物需遮光,密封保存的可能原因是 。
(4)84消毒液的有效成分是次氯酸钠(NaClO),电解饱和氯化钠溶液可制得次氯酸钠和一种可燃性气体,该反应的化学方程式为 。
(5)过氧乙酸(CH3COOOH)也是有效的消毒剂,某医疗小组用溶质质量分数为0.5%的过氧乙酸溶液200kg对环境进行消毒,需要溶质质量分数为20%的过氧乙酸溶液 kg。
17.化学不断改变着人们的生活,让生活变得更美好。
(1)袁隆平院士是我国研究杂交水稻的开创者,被誉为“杂交水稻之父”。试结合所学知识回答下列问题。
①从营养物质角度:水稻中富含淀粉,淀粉属于 (填“有机物”或“无机物”)。
②从种植角度:为了提高水稻产量,种植过程中需要施用适量的化肥。某化肥销售处现有:Ca3(PO4)2、NH4NO3、KNO3、KCl四种化肥。上述四种化肥中属于复合肥料的是 (填化学式)。
(2)豆腐是一种营养价值高、颇受大家欢迎的食品,如表是豆腐中主要成分的平均质量分数。
由表可知,豆腐中含有的营养素中能提供能量的是糖类,油脂及 。
(3)近两年,福山区夹河两岸再填两座地标性建筑物。
①10月20日,福城桥正式通车。大桥两端分别摆放两处铸铜狮子雕塑。铜制品容易生锈,铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],是铜与空气中的氧气、水和 共同作用的结果。
②崇文街大桥围绕“飞鸟”特色主题,造型采用不锈钢制“双飞燕式”异形拱为装饰结构,而不采用普通生铁,主要利用了不锈钢的 性质。
③工业上用一氧化碳和赤铁矿炼铁的原理是 (写化学方程式),建造福城桥大约用了112t铁,理论需要含氧化铁80%的赤铁矿 t。
(1)袁隆平院士是我国研究杂交水稻的开创者,被誉为“杂交水稻之父”。试结合所学知识回答下列问题。
①从营养物质角度:水稻中富含淀粉,淀粉属于 (填“有机物”或“无机物”)。
②从种植角度:为了提高水稻产量,种植过程中需要施用适量的化肥。某化肥销售处现有:Ca3(PO4)2、NH4NO3、KNO3、KCl四种化肥。上述四种化肥中属于复合肥料的是 (填化学式)。
(2)豆腐是一种营养价值高、颇受大家欢迎的食品,如表是豆腐中主要成分的平均质量分数。
| 成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素B1 | 维生素B2 |
| 质量分数% | 89.3 | 4.7 | 1.3 | 2.8 | 0.24 | 0.064 | 1.4 | 0.00006 | 0.00003 |
由表可知,豆腐中含有的营养素中能提供能量的是糖类,油脂及 。
(3)近两年,福山区夹河两岸再填两座地标性建筑物。
①10月20日,福城桥正式通车。大桥两端分别摆放两处铸铜狮子雕塑。铜制品容易生锈,铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],是铜与空气中的氧气、水和 共同作用的结果。
②崇文街大桥围绕“飞鸟”特色主题,造型采用不锈钢制“双飞燕式”异形拱为装饰结构,而不采用普通生铁,主要利用了不锈钢的 性质。
③工业上用一氧化碳和赤铁矿炼铁的原理是 (写化学方程式),建造福城桥大约用了112t铁,理论需要含氧化铁80%的赤铁矿 t。
18.纯碱(Na2CO3)是一种重要的化工原料,科学家侯德榜创立的联合制碱法(侯氏制碱法) 为我国的制碱事业作出了杰出贡献,其生产流程可简要表示如图1:
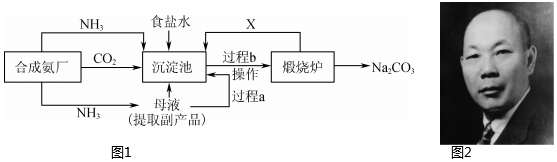
请回答下列问题:
(1)沉淀池中有碳酸氢钠晶体析出,则过程b中取出晶体碳酸氢钠采取的操作名称是 ,可知在该温度下,碳酸氢钠的溶解度 (填“大于”、“小于”或“等于”)另一种产品。
(2)碳酸氢钠晶体受热分解得到产物的同时生成二氧化碳,该流程中可以循环使用的物质是 。
(3)向母液中通氨气,加入食盐细小颗粒,冷却可析出副产品氯化铵,它的一种用途是 。
(4)写出沉淀池中发生反应的化学方程式: 。

请回答下列问题:
(1)沉淀池中有碳酸氢钠晶体析出,则过程b中取出晶体碳酸氢钠采取的操作名称是 ,可知在该温度下,碳酸氢钠的溶解度 (填“大于”、“小于”或“等于”)另一种产品。
(2)碳酸氢钠晶体受热分解得到产物的同时生成二氧化碳,该流程中可以循环使用的物质是 。
(3)向母液中通氨气,加入食盐细小颗粒,冷却可析出副产品氯化铵,它的一种用途是 。
(4)写出沉淀池中发生反应的化学方程式: 。
19.CO在工业上常用于冶炼金属,某化学兴趣小组的同学欲将CO2转化为CO并还原CuO,设计了以下实验:
步骤Ⅰ:制备并收集CO2。取一支试管,将制成糊状的CuO用毛笔刷在试管内壁,在试管底部加入少量炭粉,再用该试管收集CO2,实验装置如图。

步骤Ⅱ:用CO还原CuO。将步骤Ⅰ收集满CO2的试管套上气球,按图E组装。实验过程中用酒精灯先加热炭粉,再加热氧化铜,观察实验现象。
根据上述实验装置和操作,回答下列问题:
(1)为了收集干燥、纯净的CO2,步骤Ⅰ装置的连接顺序为:A→ → → ,制备CO2的化学方程式是 ,收集CO2时,若导管不伸入试管底部,会导致 。
(2)步骤Ⅱ中加热炭粉时,炭粉与CO2的反应属于基本反应类型中的 反应。再加热氧化铜时,1min左右观察到黑色固体变为紫红色,此时发生反应的化学方程式为 。
(3)实验结束后,挤压气球使气体进入试管,取下气球,立即在试管口放置点燃的酒精灯,其目的是 。
步骤Ⅰ:制备并收集CO2。取一支试管,将制成糊状的CuO用毛笔刷在试管内壁,在试管底部加入少量炭粉,再用该试管收集CO2,实验装置如图。

步骤Ⅱ:用CO还原CuO。将步骤Ⅰ收集满CO2的试管套上气球,按图E组装。实验过程中用酒精灯先加热炭粉,再加热氧化铜,观察实验现象。
根据上述实验装置和操作,回答下列问题:
(1)为了收集干燥、纯净的CO2,步骤Ⅰ装置的连接顺序为:A→ → → ,制备CO2的化学方程式是 ,收集CO2时,若导管不伸入试管底部,会导致 。
(2)步骤Ⅱ中加热炭粉时,炭粉与CO2的反应属于基本反应类型中的 反应。再加热氧化铜时,1min左右观察到黑色固体变为紫红色,此时发生反应的化学方程式为 。
(3)实验结束后,挤压气球使气体进入试管,取下气球,立即在试管口放置点燃的酒精灯,其目的是 。
20.金属镁可与热水反应生成氢氧化镁和氢气,所得溶液呈碱性,可使酚酞溶液显红色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液。变为红色:放置在空气中一段时同后,发现溶液的红色褪去了。
(1)镁与热水反应的化学方程式是: 。
查阅资料:溶液红色褪去的原因是溶液碱性减弱。
【提出问题】导致溶液碱性减弱的原因是什么?
【假设与分析】
假设1:可能是氢氧化镁与N2或O2发生了反应。
(2)假设2:可能是溶液吸收了空气中的 。
(3)假设3:可能是氢氧化镁的溶解度随温度的降低而 。
由碱的性质可知,假设1不成立。
(4)【实验探究】
【拓展延伸】
(5)将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。请解释其原因: 。
(6)除上述金属外,根据金属活动性顺序,预测 也能跟硫酸铜溶液反应产生上述现象(举一例即可)。
(1)镁与热水反应的化学方程式是: 。
查阅资料:溶液红色褪去的原因是溶液碱性减弱。
【提出问题】导致溶液碱性减弱的原因是什么?
【假设与分析】
假设1:可能是氢氧化镁与N2或O2发生了反应。
(2)假设2:可能是溶液吸收了空气中的 。
(3)假设3:可能是氢氧化镁的溶解度随温度的降低而 。
由碱的性质可知,假设1不成立。
(4)【实验探究】
| 实验操作 | 实验现象 | 结论 |
| 1.取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象 | ① | 假设2成立 |
| 2.取上述红色溶液,② ,③ ,观察现象 | 红色褪去 | 假设3成立 |
【拓展延伸】
(5)将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。请解释其原因: 。
(6)除上述金属外,根据金属活动性顺序,预测 也能跟硫酸铜溶液反应产生上述现象(举一例即可)。
21.为测定某碳酸钠溶液的溶质质量分数,他取出100g该溶液,向其中逐滴滴加溶质质量分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:(提示:碳酸钠与稀盐酸反应生成氯化钠、水及二氧化碳)
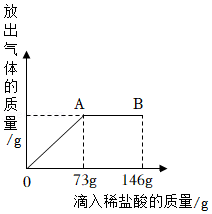
(1)当滴加稀盐酸至图中A点时,烧杯中所得溶液呈 (填“酸性”、“中性”或“碱性”)。当滴加稀盐酸至图中B点时,烧杯中所得溶液的溶质是 (填化学式)。
(2)请计算此碳酸钠溶液中溶质的质量分数 。

(1)当滴加稀盐酸至图中A点时,烧杯中所得溶液呈 (填“酸性”、“中性”或“碱性”)。当滴加稀盐酸至图中B点时,烧杯中所得溶液的溶质是 (填化学式)。
(2)请计算此碳酸钠溶液中溶质的质量分数 。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解