下载高清试卷
【2022年湖南省常德市中考化学模拟试卷】-第1页
试卷格式:2022年湖南省常德市中考化学模拟试卷.PDF
试卷热词:最新试卷、2022年、湖南试卷、常德市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.2022年4月16日,神舟十三号飞船返回舱在东风着陆场成功着陆。下列一定涉及化学变化的是( )
- A. 着陆场红旗飘扬
- B. 航天员出舱
- C. 航天员转运货物
- D. 遥十三运载火箭点火
2.下列符号表示“两个氢分子”的是( )
- A. H2
- B. H2O
- C. 2H2
- D. 2H
3.用溶质质量分数为36%的浓盐酸配制一定浓度的稀盐酸时,不会用到的仪器是( )
- A.
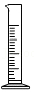
- B.
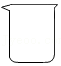
- C.
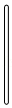
- D.
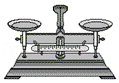
4.下列有关实验现象的描述,正确的是( )
- A. 硫在空气中燃烧,产生蓝紫色火焰
- B. 木炭在氧气中燃烧,产生有刺激性气味的气体
- C. 细铁丝在氧气中剧烈燃烧,火星四射,有黑色固体生成
- D. 红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾
5.鉴别O2、CO、CO2三种气体,可行简便的方法是( )
- A. 将气体分别通入澄清石灰水
- B. 将气体分别通入石蕊试液
- C. 试验三种气体在水中溶解性
- D. 用燃着的木条分别伸入瓶内
6.下列物质中属于氧化物的是( )
- A. 葡萄糖
- B. 液氧
- C. 干冰
- D. 苛性钠
7.据报道,一种新型铝离子电池,比现今普遍使用的锂离子电池具有更加优良的性能,未来,该铝离子电池或将成为下一代高性价比电池的理想选择,如图是元素周期表中锂、铝两种元素的有关信息,下列说法不正确的是( )
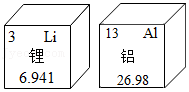

- A. 锂、铝元素在周期表中分别位于第二、三周期
- B. 相对原子质量铝比锂多20.039g
- C. 锂、铝两种元素都是金属元素
- D. 核外电子数Al3+比Li+多8
8.头孢类消炎药是日常生活中常用的一类抗菌药物,注射或口服头孢类药物后一段时间内不能饮酒,否则会出现心率加快、血压下降,严重者会出现心力衰竭导致死亡,下列关于头孢氨苄(化学式:C16H17N3O4S)的说法不正确的是( )
- A. 属于有机化合物
- B. 由C、H、N、O、S五种元素组成
- C. 氢元素的质量分数最小
- D. 完全燃烧时只生成二氧化碳和水
9.如图是五种微粒的结构示意图,下列说法不正确的是( )
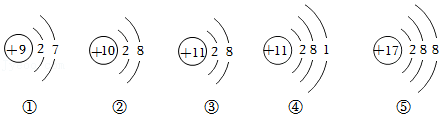
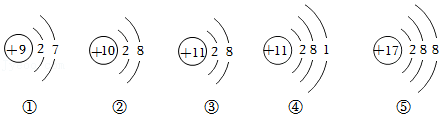
- A. ①⑤所表示的元素化学性质不相似
- B. ②③⑤表示的微粒性质较稳定
- C. ①②④属于原子,其中⑤属于阴离子,③属于阳离子
- D. ④⑤对应元素组成化合物的化学式为NaCl
10.下列实验方案正确的是( )
| 序号 | 实验目的 | 实验方案 |
| A | 鉴别CO2和N2 | 将燃着的木条分别伸入气体中,观察现象 |
| B | 鉴别NH4Cl和KCl两种白色固体肥料 | 加入熟石灰研磨后闻气味 |
| C | 除去CO2中混有的少量CO | 将气体通过灼热铜丝网 |
| D | 除去氢氧化钠溶液中的碳酸钠 | 加入过量的石灰水,充分反应后过滤 |
- A. A
- B. B
- C. C
- D. D
11.下面各组物质在水溶液中能大量共存的是( )
- A. NaCl、HCl、Na2CO3、NaOH
- B. H2SO4、BaCl2、KNO3、NaOH
- C. CuSO4、Na2CO3、NaOH、KCl
- D. NaCl、KCl、HCl、NaNO3
12.小东同学向盛有硝酸锌和硝酸银混合液的烧杯中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,有气泡产生。下列说法正确的是( )
- A. 滤液中一定含有硝酸亚铁,一定没有硝酸银和硝酸锌
- B. 滤液中一定含有硝酸锌,一定没有硝酸亚铁和硝酸银
- C. 滤渣中一定含有银和铁,一定没有锌
- D. 滤渣中一定含有银和铁,可能有锌
13.化学学习者常用化学思维去认识和理解世界。下列选项错误的是( )
- A. 变化与守恒:依据砂糖灼烧后得到黑色物质,可推测砂糖中含有碳元素
- B. 模型与推理:鱼类能在水中生活,证明水中溶有氧气
- C. 宏观与微观:一氧化碳和二氧化碳的化学性质不同,原因是构成物质的分子不同
- D. 探究与创新:探究氧化铜是否为过氧化氢分解的催化剂,只需设计实验证明氧化铜能否改变反应速率即可
14.如图一所示为稀盐酸和氢氧化钠溶液反应的实验操作,图二为反应过程中烧杯内溶液pH的变化曲线。下列说法不正确的是( )
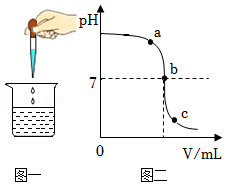

- A. 胶头滴管中所取的溶液为稀盐酸
- B. c点表示溶液中氢氧化钠和盐酸恰好完全反应
- C. a点表示的溶液能使酚酞溶液变红
- D. b点表示的溶液中溶质是NaCl
15.在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说 法错误的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 20 | 20 | 3 |
| 反应后质量/g | 待测 | 12 | 31 | 3 |
- A. 该反应是化合反应,丁可能是催化剂
- B. 甲、乙两种物质中元素种类一定与丙物质中元素种类相同
- C. 乙物质可能是单质
- D. 反应后甲物质的质量为3g
16.用化学用语填空:
(1)2个氢原子 。
(2)3个氧分子 。
(3)4个铵根离子 。
(4)甲烷 。
(1)2个氢原子 。
(2)3个氧分子 。
(3)4个铵根离子 。
(4)甲烷 。
17.中国高铁正式走出国门参与国际竞争,合作设计建造俄罗斯首条高铁。如图是“和谐号”高铁车头的示意图。

(1)高铁车头的玻璃是用无机玻璃(主要成分为二氧化硅)、树脂、塑料等粘合而成,能耐受强大的撞击力。这种玻璃属于 材料。
(2)为适应火车提速,高速铁路的短轨已全部连接为超长轨。焊接钢轨的反应原理可用化学方程式表示为2Al+Fe2O3
X+2Fe,则该反应中物质X的化学式为 ,并说明铝的金属活动性比铁要 (填“强”或“弱”)。
(3)高铁采用铝合金车厢。常温下,铝具有很好的抗腐蚀性能,用化学方程式解释原因为 。

(1)高铁车头的玻璃是用无机玻璃(主要成分为二氧化硅)、树脂、塑料等粘合而成,能耐受强大的撞击力。这种玻璃属于 材料。
(2)为适应火车提速,高速铁路的短轨已全部连接为超长轨。焊接钢轨的反应原理可用化学方程式表示为2Al+Fe2O3
| 高温 |
(3)高铁采用铝合金车厢。常温下,铝具有很好的抗腐蚀性能,用化学方程式解释原因为 。
18.化学与生活密切相关。回答下列问题:
(1)某学校为学生准备的午餐食谱如下:米饭、红烧肉、清蒸鱼、凉拌黄瓜、豆腐汤,其中富含糖类的是 。
(2)在治疗胃酸过多症的药物成分中,含有的物质不可能是 (填字母)。
A.碳酸氢钠 B.氢氧化铝 C.氢氧化钠 D.碳酸钙
(3)自来水硬度较大不宜直接饮用。为了降低水的硬度,生活中常采用的方法是 。
(4)扑灭森林火灾时,通常将大火蔓延路线前的一片树木砍掉,其灭火原理是 。
(5)“垃圾是放错了地方的资源”,生活垃圾提倡分类处理,分类的目的是提高垃圾的资源价值和经济价值。饮料罐、矿泉水瓶、废纸等应放入标识 的垃圾桶中。

(1)某学校为学生准备的午餐食谱如下:米饭、红烧肉、清蒸鱼、凉拌黄瓜、豆腐汤,其中富含糖类的是 。
(2)在治疗胃酸过多症的药物成分中,含有的物质不可能是 (填字母)。
A.碳酸氢钠 B.氢氧化铝 C.氢氧化钠 D.碳酸钙
(3)自来水硬度较大不宜直接饮用。为了降低水的硬度,生活中常采用的方法是 。
(4)扑灭森林火灾时,通常将大火蔓延路线前的一片树木砍掉,其灭火原理是 。
(5)“垃圾是放错了地方的资源”,生活垃圾提倡分类处理,分类的目的是提高垃圾的资源价值和经济价值。饮料罐、矿泉水瓶、废纸等应放入标识 的垃圾桶中。

19.如图为A、B两种固体物质的溶解度曲线,请据图填空:
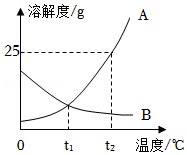
(1)在t1℃时,A、B两种物质的溶解度 。(填“相同”或“不相同”)
(2)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是 。
(3)t2℃时,把100克A物质的饱和溶液恒温蒸发10克水,可析出A物质 克,此时溶液中溶质的质量分数为 。

(1)在t1℃时,A、B两种物质的溶解度 。(填“相同”或“不相同”)
(2)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是 。
(3)t2℃时,把100克A物质的饱和溶液恒温蒸发10克水,可析出A物质 克,此时溶液中溶质的质量分数为 。
20.燃料是工农业生产和人民生活不可缺少的重要能源
(1)汽油中加入适量乙醇得到乙醇汽油,关于乙醇汽油的说法中不正确的是 。
A.乙醇属于可再生性能源 B.乙醇汽油不能用作汽车燃料
C.使用乙醇汽油可减少大气污染 D.使用乙醇汽油可节省石油资源
(2)汽车尾气中含有CO、NO,一种新型催化剂能使二者发生反应,生成两种常见的无毒气体,反应的化学方程式为 。
(3)以下是家用燃料的更新历程:

下列有关家用燃料更新的理由正确的是 。
A.符合低碳经济 B.气体燃料燃烧的更充分
C.天然气是可再生的能源 D.减少煤燃烧过程中产生的污染物
(4)天然气(主要成分是甲烷)和液化石油气(主要成分是丙烷和丁烷)中碳元素的质量分数分别约为75%和82.3%,通过该数据分析,相同条件下,用天然气作燃料比液化石油气更环保的理由是: ,甲烷在空气中完全燃烧的化学方程式为 ,天然气需经过除杂,添加无毒臭味剂,减压等处理后才能输送到家中,请用分子的观点解释天然气减压后体积会膨胀的原因 。
(1)汽油中加入适量乙醇得到乙醇汽油,关于乙醇汽油的说法中不正确的是 。
A.乙醇属于可再生性能源 B.乙醇汽油不能用作汽车燃料
C.使用乙醇汽油可减少大气污染 D.使用乙醇汽油可节省石油资源
(2)汽车尾气中含有CO、NO,一种新型催化剂能使二者发生反应,生成两种常见的无毒气体,反应的化学方程式为 。
(3)以下是家用燃料的更新历程:

下列有关家用燃料更新的理由正确的是 。
A.符合低碳经济 B.气体燃料燃烧的更充分
C.天然气是可再生的能源 D.减少煤燃烧过程中产生的污染物
(4)天然气(主要成分是甲烷)和液化石油气(主要成分是丙烷和丁烷)中碳元素的质量分数分别约为75%和82.3%,通过该数据分析,相同条件下,用天然气作燃料比液化石油气更环保的理由是: ,甲烷在空气中完全燃烧的化学方程式为 ,天然气需经过除杂,添加无毒臭味剂,减压等处理后才能输送到家中,请用分子的观点解释天然气减压后体积会膨胀的原因 。
21.某经济开发区将钛(Ti)冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如右图所示),大大提高了资源利用率,减少了环境污染。请填写:
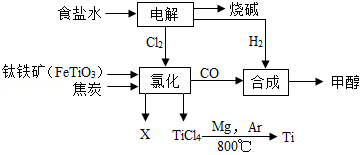
(1)氯碱厂用电解饱和食盐水的方法制取烧碱,同时得到氯气和氢气。写出其化学方程式: 。
(2)钛冶炼厂氯化车间的氯化过程发生如下反应:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X的化学式为 。已知FeTiO3中铁元素显+2价,则钛元素的化合价为 。
(3)试写出TiCl4与Mg反应生成金属Ti的化学方程式 ,该反应的基本反应类型是 。上述反应需在氩气环境中进行,理由是 。

(1)氯碱厂用电解饱和食盐水的方法制取烧碱,同时得到氯气和氢气。写出其化学方程式: 。
(2)钛冶炼厂氯化车间的氯化过程发生如下反应:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X的化学式为 。已知FeTiO3中铁元素显+2价,则钛元素的化合价为 。
(3)试写出TiCl4与Mg反应生成金属Ti的化学方程式 ,该反应的基本反应类型是 。上述反应需在氩气环境中进行,理由是 。
22.根据下列装置,结合所学化学知识回答下列问题:
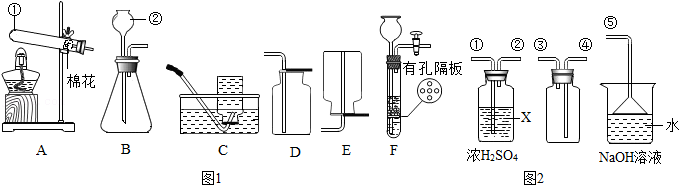
(1)写出有标号的仪器名称:① ,② 。
(2)实验室用高锰酸钾制取并收集较纯净O2可选用的收集装置是 (填字母代号),
(3)实验室用B、D装置制取CO2的化学方程式为 ,若将发生装置由B改为F,其优点是 。
(4)SO2是无色有刺激性气味的有毒气体,密度比空气大,易溶于水。SO2的某些化学性质与CO2相似,实验中常用NaOH溶液吸收SO2尾气。用如图2所示装置收集一瓶干燥的SO2,装置中导管按气流方向连接顺序是①→②→④→③→⑤;图中漏斗的作用是 ;烧杯中NaOH溶液的作用 。

(1)写出有标号的仪器名称:① ,② 。
(2)实验室用高锰酸钾制取并收集较纯净O2可选用的收集装置是 (填字母代号),
(3)实验室用B、D装置制取CO2的化学方程式为 ,若将发生装置由B改为F,其优点是 。
(4)SO2是无色有刺激性气味的有毒气体,密度比空气大,易溶于水。SO2的某些化学性质与CO2相似,实验中常用NaOH溶液吸收SO2尾气。用如图2所示装置收集一瓶干燥的SO2,装置中导管按气流方向连接顺序是①→②→④→③→⑤;图中漏斗的作用是 ;烧杯中NaOH溶液的作用 。
23.现有一瓶稀盐酸和一瓶碳酸钠溶液,请设计简单的实验将它们鉴别开(写出实验操作、实验现象、实验结论)。
| 实验操作 | 实验现象 | 实验结论 |
24.不用火不用电,只需拆开发热包倒入凉水,就能享用美食的自热食品,受到消费者的追捧。
[查阅资料]I.发热包中物质的主要成分是生石灰,碳酸钠、铝粒。
Ⅱ.铝和强碱溶液反应生成氢气。
探究一:发热包的发热原理
(1)小明买了一盒自热米饭,取出发热包加入凉水,发生剧烈反应,迅速放出大量的热,写出产生该现象的主要化学反应方程式 ;同时发热包内固体物质变硬、结块,依据观察到的实验现象,小明猜想发热包内的物质可能发生多个化学反应,写出其中一个反应的化学方程式 。
(2)发热包上的安全警示图标有“禁止明火”,其原因可能是 。
小明向使用后的发热包中加入稀盐酸,并对产生的气体展开进一步探究。
探究二:确定气体的成分

(3)[猜想与假设]小明认为该气体可能是a.H2;b. ;c.CO2和H2的混合气体。
[实验设计]小明同学设计如图实验装置,对气体成分进行探究。
(4)[实验验证]甲装置中的实验现象是 ,丁装置中黑色的粉末逐渐变为红色,试管口有水珠产生,证明猜想c正确。若甲、乙装置交换位置,(填“能“或不能”) 确定气体中含有CO2,写出化学方程式并说明理由 。
[总结与反思]通过以上探究,小明做出如下反思:
a.发热包应密封防潮保存
b.能与水混合放出热量的物质均可做发热包的发热材料
c.使用后的发热包应包好按照垃级分类投放
(5)你认为其中正确的是 。
| 食品专用发热包FOOD HEATER BAG 禁止热水;禁止明火;禁止食用;小心烫伤 储存条件:存放于阴凉、干燥处 使用方法:撕去塑料袋后,放入适量冷水中 注意事项: 1.请勿湿手接触发热包。 2.使用过程中,禁止食用热水,小心高温烫、注意通风并远离明火。 3.使用前后,如有发现破袋污染食品,请勿使用。 4.如有发热包内物质误入口、眼、鼻,请立即使用清水冲洗、催吐或医院就医。 5.未成年人请勿独自使用。 |
[查阅资料]I.发热包中物质的主要成分是生石灰,碳酸钠、铝粒。
Ⅱ.铝和强碱溶液反应生成氢气。
探究一:发热包的发热原理
(1)小明买了一盒自热米饭,取出发热包加入凉水,发生剧烈反应,迅速放出大量的热,写出产生该现象的主要化学反应方程式 ;同时发热包内固体物质变硬、结块,依据观察到的实验现象,小明猜想发热包内的物质可能发生多个化学反应,写出其中一个反应的化学方程式 。
(2)发热包上的安全警示图标有“禁止明火”,其原因可能是 。
小明向使用后的发热包中加入稀盐酸,并对产生的气体展开进一步探究。
探究二:确定气体的成分

(3)[猜想与假设]小明认为该气体可能是a.H2;b. ;c.CO2和H2的混合气体。
[实验设计]小明同学设计如图实验装置,对气体成分进行探究。
(4)[实验验证]甲装置中的实验现象是 ,丁装置中黑色的粉末逐渐变为红色,试管口有水珠产生,证明猜想c正确。若甲、乙装置交换位置,(填“能“或不能”) 确定气体中含有CO2,写出化学方程式并说明理由 。
[总结与反思]通过以上探究,小明做出如下反思:
a.发热包应密封防潮保存
b.能与水混合放出热量的物质均可做发热包的发热材料
c.使用后的发热包应包好按照垃级分类投放
(5)你认为其中正确的是 。
25.实验室需要3.2g氧气,若用加热分解氯酸钾和二氧化锰的方法制取这些氧气,消耗氯酸钾的质量是多少?
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解