下载高清试卷
【2021年北京市石景山区中考化学二模试卷】-第1页
试卷格式:2021年北京市石景山区中考化学二模试卷.PDF
试卷热词:最新试卷、2021年、北京试卷、石景山区试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.空气成分中体积分数最大的是( )
- A. N2
- B. O2
- C. CO2
- D. 稀有气体
2.下列属于化学变化的是( )
- A. 冰雪融化
- B. 纸张燃烧
- C. 水分蒸发
- D. 矿石粉碎
3.温泉水富含钾、钠、钙、镁、锌等矿物质,这里的“钾、钠、钙、镁、锌”指的是( )
- A. 元素
- B. 原子
- C. 单质
- D. 分子
4.废弃的易拉罐和塑料瓶属于( )
- A. 厨余垃圾
- B. 其他垃圾
- C. 可回收物
- D. 有害垃圾
5.能闻到花香的原因是( )
- A. 分子的质量变小
- B. 分子间有间隔
- C. 分子在不断运动
- D. 分子由原子构成
6.下列物质在氧气中燃烧,产生大量白烟的是( )
- A. 木炭
- B. 甲烷
- C. 蜡烛
- D. 红磷
7.碳酸氢钠常用于焙制糕点,其俗称是( )
- A. 熟石灰
- B. 小苏打
- C. 烧碱
- D. 纯碱
8.下列物质的用途中,利用其物理性质的是( )
- A. 干冰用作冷冻剂
- B. 甲烷用作燃料
- C. 氧气用于炼钢
- D. 硫酸用于处理碱性废液
9.下列属于氧化物的是( )
- A. O2
- B. SO2
- C. K2CO3
- D. NaOH
10.下列原子中的粒子,带负电荷的是( )
- A. 电子
- B. 中子
- C. 质子
- D. 原子核
11.下列属于纯净物的是( )
- A. 加碘食盐
- B. 氧气
- C. 硬水
- D. 食醋
12.下列实验操作中,正确的是( )
- A.
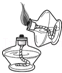 点燃酒精灯
点燃酒精灯 - B.
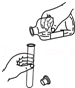 倾倒液体
倾倒液体 - C.
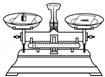 称量固体
称量固体 - D.
 加热液体
加热液体
13.下列气体能使紫色石蕊溶液变红的是( )
- A. CO2
- B. O2
- C. H2
- D. N2
14.下列物质能与NaOH反应的是( )
- A. Fe
- B. CO2
- C. Fe2O3
- D. NaCl
15.下列符号中,表示2个氢原子的是( )
- A. H2
- B. 2H2
- C. 2H
- D. H2O
16.电解水实验如图。下列说法不正确的是( )


- A. 试管2中得到O2
- B. 产生H2与O2的体积比约为1:2
- C. 该实验说明水由氢元素和氧元素组成
- D. 可用带火星的木条检验生成的O2
17.在氯酸钾(
ClO3)中,氯元素的化合价是( )
+1 |
- A. +1
- B. +3
- C. +5
- D. +7
18.检验二氧化碳是否收集满的方法是( )
- A. 将带火星的木条伸入集气瓶口
- B. 将燃着的木条伸至集气瓶口
- C. 向集气瓶中加入澄清石灰水
- D. 将燃着的木条伸入集气瓶中
19.下列说法不正确的是( )
- A. 浓硫酸有吸水性
- B. H2O2能分解
- C. H2O是常用的溶剂
- D. Al在常温下不能与O2反应
20.下列物质必须密封保存的是( )
- A. 木炭
- B. 氢氧化钠
- C. 石灰石
- D. 氯化钠
21.配制50g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )
- A. 蒸发皿
- B. 玻璃棒
- C. 烧杯
- D. 量筒
22.能与无色硝酸银溶液反应,使溶液变为蓝色的金属是( )
- A. 铝
- B. 铁
- C. 铜
- D. 银
23.下列有关“CO2”的说法正确的是( )
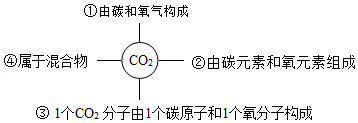

- A. ①
- B. ②
- C. ③
- D. ④
24.甲、乙的溶解度曲线如图所示。下列说法正确的是( )
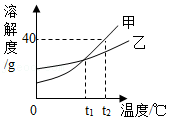

- A. 甲的溶解度大于乙的溶解度
- B. t1℃时,甲、乙两种饱和溶液中溶质质量分数相等
- C. t2℃时,甲的饱和溶液中溶质和溶液的质量比为2:5
- D. 甲的饱和溶液从t2℃降温到t1℃,溶液中溶质质量分数不变
25.甲和乙在一定条件下反应生成丙和丁。结合微观示意图分析,下列结论不正确的是( )
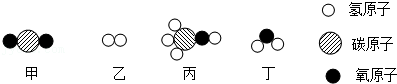

- A. 甲为二氧化碳分子
- B. 丙的1个分子由6个原子构成
- C. 反应前后分子总数不变
- D. 生成的丙和丁的分子个数比为1:1
26.化学物质及元素与人体健康密切相关。
(1)下列食物中富含蛋白质的是 (填序号)。

(2)为了防止骨质疏松,人体每日必须摄入足够量的 元素。
(1)下列食物中富含蛋白质的是 (填序号)。

(2)为了防止骨质疏松,人体每日必须摄入足够量的 元素。
27.家用清洁剂在使用时有不同的注意事项。
(1)水垢清除剂的主要成分是柠檬酸(C6H8O7),C6H8O7由 种元素组成,其中碳、氢元素的质量比为 。
(2)厨房用的重油污清洗剂主要成分是NaOH,使用时禁止与皮肤接触,其原因是 。
(3)洁厕灵的主要成分是盐酸,能除去铁制品表面的锈迹,但不能长时间浸泡。用化学方程式解释原因: , 。
(1)水垢清除剂的主要成分是柠檬酸(C6H8O7),C6H8O7由 种元素组成,其中碳、氢元素的质量比为 。
(2)厨房用的重油污清洗剂主要成分是NaOH,使用时禁止与皮肤接触,其原因是 。
(3)洁厕灵的主要成分是盐酸,能除去铁制品表面的锈迹,但不能长时间浸泡。用化学方程式解释原因: , 。
28.兴趣小组用pH传感器对市售的两种抗酸胃药(碳酸氢钠片和氢氧化铝片)的抗酸性能进行研究。用pH为1.5的盐酸模拟胃酸,按说明书上的使用剂量,将药片研成粉末,在相同条件下进行实验,结果如图。
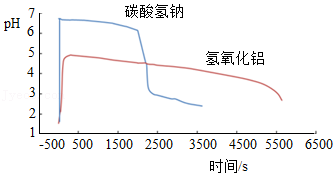
(1)用化学方程式表示碳酸氢钠抗酸的原理: 。
(2)依据图示得出的结论正确的是 (填序号)。
A. 服用碳酸氢钠片,能快速降低酸性
B. 服用氢氧化铝片,药效持续时间长
C. 服用时,能引起胃胀的是氢氧化铝片

(1)用化学方程式表示碳酸氢钠抗酸的原理: 。
(2)依据图示得出的结论正确的是 (填序号)。
A. 服用碳酸氢钠片,能快速降低酸性
B. 服用氢氧化铝片,药效持续时间长
C. 服用时,能引起胃胀的是氢氧化铝片
29.阅读下面科普短文。
大豆起源于中国,至今已有5000年的种植历史,并流传到世界各地。大豆具有很高的营养价值,在很多古籍中,均有记载大豆对身体健康的重要作用,如《本草纲目》中“性味甘平,致健脾开中,润燥,利水,排浓解毒,消肿止痛功效”。大豆富含蛋白质,是人体中蛋白质补充的重要来源,常见作物中蛋白质含量如图1。
以大豆为原料的大豆制品在生活中很常见,如豆腐、豆浆、腐竹、豆油等。豆腐是一种营养丰富、物美价廉、风味独特、历史悠久的中国传统大豆蛋白制品。制作过程如图3:

浸泡大豆是豆浆制备最重要的预处理环节之一。下面是研究浸泡时间对豆浆中蛋白质含量的影响:称取150g大豆,用450mL 0.5% NaHCO3溶液于25℃下浸泡,测得豆浆中蛋白质含量随浸泡时间的变化如图2。
大豆除作为供人类食用的粮食作物外,还广泛用在畜牧业的蛋白质饲料,大豆深加工产品还应用于生产保健品和医药、大豆蛋白胶胶黏剂等方面。
(原文作者王军、唐楠楠、杨道强等,有删改)
依据文章内容回答下列问题。
(1)图1常见作物中,蛋白质含量最高的是 。
(2)做豆腐过程中,过筛的目的是 。
(3)0.5%碳酸氢钠溶液中溶质为 。
(4)由图2得出的结论是 。
(5)下列说法正确的是 (填序号)。
A. 大豆起源于中国,种植历史悠久
B. 豆腐是一种营养丰富的大豆蛋白制品
C. 大豆制品是人体中蛋白质补充的来源之一
D. 大豆只供人类做成食品食用
大豆起源于中国,至今已有5000年的种植历史,并流传到世界各地。大豆具有很高的营养价值,在很多古籍中,均有记载大豆对身体健康的重要作用,如《本草纲目》中“性味甘平,致健脾开中,润燥,利水,排浓解毒,消肿止痛功效”。大豆富含蛋白质,是人体中蛋白质补充的重要来源,常见作物中蛋白质含量如图1。
以大豆为原料的大豆制品在生活中很常见,如豆腐、豆浆、腐竹、豆油等。豆腐是一种营养丰富、物美价廉、风味独特、历史悠久的中国传统大豆蛋白制品。制作过程如图3:

浸泡大豆是豆浆制备最重要的预处理环节之一。下面是研究浸泡时间对豆浆中蛋白质含量的影响:称取150g大豆,用450mL 0.5% NaHCO3溶液于25℃下浸泡,测得豆浆中蛋白质含量随浸泡时间的变化如图2。
大豆除作为供人类食用的粮食作物外,还广泛用在畜牧业的蛋白质饲料,大豆深加工产品还应用于生产保健品和医药、大豆蛋白胶胶黏剂等方面。
(原文作者王军、唐楠楠、杨道强等,有删改)
依据文章内容回答下列问题。
(1)图1常见作物中,蛋白质含量最高的是 。
(2)做豆腐过程中,过筛的目的是 。
(3)0.5%碳酸氢钠溶液中溶质为 。
(4)由图2得出的结论是 。
(5)下列说法正确的是 (填序号)。
A. 大豆起源于中国,种植历史悠久
B. 豆腐是一种营养丰富的大豆蛋白制品
C. 大豆制品是人体中蛋白质补充的来源之一
D. 大豆只供人类做成食品食用
30.燃煤烟气中含有大量CO2,以石灰石为原料从燃煤烟气中吸收CO2的流程如图,排出的高浓度CO2(>95%)回收再利用。

(1)生石灰的主要成分是 。
(2)将生石灰在研磨机中磨碎的目的是 。
(3)吸收反应器中发生的反应属于基本反应类型中的 反应。

(1)生石灰的主要成分是 。
(2)将生石灰在研磨机中磨碎的目的是 。
(3)吸收反应器中发生的反应属于基本反应类型中的 反应。
31.CuO是某种无机胶黏剂的组分之一,其制备的部分流程如图。
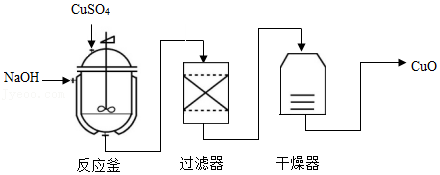
已知:CuO难溶于水。
(1)反应釜中,发生的反应有:①NaOH与CuSO4发生复分解反应,反应的化学方程式为 ;②Cu(OH)2
CuO+H2O。
(2)过滤器分离出的滤液中一定含有的溶质是 。

已知:CuO难溶于水。
(1)反应釜中,发生的反应有:①NaOH与CuSO4发生复分解反应,反应的化学方程式为 ;②Cu(OH)2
| △ |
(2)过滤器分离出的滤液中一定含有的溶质是 。
32.请从A、B两题中任选一个作答。
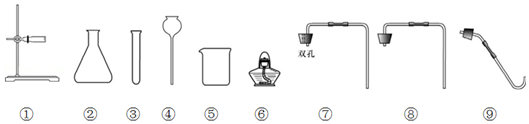

| A.实验室用高锰酸钾制取氧气 | B.实验室制取二氧化碳 |
| (1)发生装置所用仪器有 (填序号)。 (2)反应的化学方程式为 。 | (3)发生装置所用仪器有 (填序号)。 (4)反应的化学方程式为 。 |
33.根据如图回答问题。

(1)实验1中,观察到的现象有 ;发生反应的化学方程式为 , 。
(2)实验2中,将紫色石蕊溶液浸泡并晾干的小花,一半喷水后放入集气瓶中,该实验的目的是 。
(3)实验3中,观察到蜡烛由低到高依次熄灭,实验得出的结论是 。

(1)实验1中,观察到的现象有 ;发生反应的化学方程式为 , 。
(2)实验2中,将紫色石蕊溶液浸泡并晾干的小花,一半喷水后放入集气瓶中,该实验的目的是 。
(3)实验3中,观察到蜡烛由低到高依次熄灭,实验得出的结论是 。
34.用如图装置进行实验(夹持仪器略去)。加热一段时间,蜡烛掉落,铜片中间火柴燃烧,又一会儿右端火柴燃烧,熄灭酒精灯。
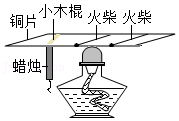
(1)能说明铜具有导热性的现象是 。
(2)对比小木棍和火柴的现象,得出可燃物燃烧的条件之一是 。

(1)能说明铜具有导热性的现象是 。
(2)对比小木棍和火柴的现象,得出可燃物燃烧的条件之一是 。
35.粗盐中难溶性杂质的去除。
(1)过滤时,用到的玻璃仪器有烧杯、玻璃棒和 。
(2)蒸发过程中,需不断进行搅拌,其原因是 。
(1)过滤时,用到的玻璃仪器有烧杯、玻璃棒和 。
(2)蒸发过程中,需不断进行搅拌,其原因是 。
36.进行如图实验,研究氢氧化钙的性质。
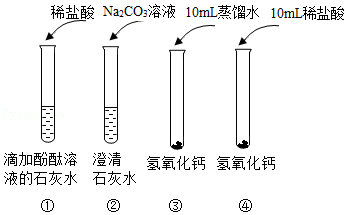
(1)能证明①中发生反应的现象是 。
(2)②中反应的化学方程式为 。
(3)观察到③中固体几乎不溶解,④中固体溶解,对比③和④得出的结论是 。

(1)能证明①中发生反应的现象是 。
(2)②中反应的化学方程式为 。
(3)观察到③中固体几乎不溶解,④中固体溶解,对比③和④得出的结论是 。
37.利用表中装置进行实验。
已知:集气瓶容积为350mL,集气瓶中水为100mL。
(1)加入足量红磷的目的是 。
(2)集气瓶中,O2的体积分数约为 %。
已知:集气瓶容积为350mL,集气瓶中水为100mL。
| 装置 | 实验 |
 | 集气瓶中盛有用排空气法收集的氧气,燃烧匙中为足量红磷。Ⅰ.关闭止水夹,点燃红磷迅速塞紧胶塞。Ⅱ.待冷却后,打开止水夹。当烧杯中液面不再变化时,测得烧杯中减少了200mL水。 |
(1)加入足量红磷的目的是 。
(2)集气瓶中,O2的体积分数约为 %。
38.课外小组对铜能否与盐酸和硫酸反应进行如下探究。
【进行实验】
取10支试管,分别加入大小相同的光亮铜片,配制不同浓度的盐酸和硫酸分别倒入试管,浸没铜片,用酒精灯加热(其中倒入盐酸的试管中:加一层石蜡油液封,用小火持续加热,使盐酸处于微沸状态30min)。
【解释与结论】
(1)浓硫酸稀释时的操作是 。
(2)盐酸加热时,用石蜡油液封的目的是 。
(3)由实验得出,盐酸与铜不反应的浓度范围是 。
(4)铜与81%的硫酸反应后的溶液变为蓝色,原因是 。
【反思与评价】
(5)铜与98%硫酸反应生成的气体为SO2。铜与37%盐酸反应产生的气体是否为同一种气体,并说明理由: 。
(6)从金属活动性角度解释,铜与17%的稀硫酸不反应的原因是 。
【进行实验】
取10支试管,分别加入大小相同的光亮铜片,配制不同浓度的盐酸和硫酸分别倒入试管,浸没铜片,用酒精灯加热(其中倒入盐酸的试管中:加一层石蜡油液封,用小火持续加热,使盐酸处于微沸状态30min)。
| 硫酸浓度% | 17 | 63 | 65 | 81 | 98 |
| 现象 | 加热20min铜表面光亮 | 加热20min,铜表面光亮 | 加热15min,铜表面变黑 | 加热5min,铜表面变黑,10min后反应剧烈 | 加热1min,铜表面变黑,3min后反应剧烈 |
| 铜片表面都有气泡产生,有刺激性气味,溶液变为蓝色 | |||||
| 盐酸浓度% | 12 | 14 | 16 | 27 | 37 |
| 现象 | 溶液无色,铜片没有变化 | 溶液几乎呈无色,铜片没有变化 | 溶液呈很淡的黄色,铜片没有变化 | 溶液呈淡黄色,铜片表面有极细小的极少气泡 | 溶液呈明显的黄色,铜片表面气泡明显 |
【解释与结论】
(1)浓硫酸稀释时的操作是 。
(2)盐酸加热时,用石蜡油液封的目的是 。
(3)由实验得出,盐酸与铜不反应的浓度范围是 。
(4)铜与81%的硫酸反应后的溶液变为蓝色,原因是 。
【反思与评价】
(5)铜与98%硫酸反应生成的气体为SO2。铜与37%盐酸反应产生的气体是否为同一种气体,并说明理由: 。
(6)从金属活动性角度解释,铜与17%的稀硫酸不反应的原因是 。
39.高纯度的硅是太阳能电池和电脑芯片不可缺少的材料。生产高纯硅的反应为2H2+SiCl4
Si+4HCl。请计算:
(1)SiCl4中硅元素的质量分数为 %(计算结果精确到0.1%)。
(2)生产28kg硅至少需要氢气的质量。
| △ |
(1)SiCl4中硅元素的质量分数为 %(计算结果精确到0.1%)。
(2)生产28kg硅至少需要氢气的质量。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解