下载高清试卷
【2022年湖北省武汉市中考化学试卷】-第1页
试卷格式:2022年湖北省武汉市中考化学试卷.PDF
试卷热词:最新试卷、2022年、湖北试卷、武汉市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.笔、墨、纸、砚并称文房四宝,其中“墨”的主要成分是炭黑。炭黑的下列性质中属于化学性质的是( )
- A. 熔点高
- B. 可燃性
- C. 难溶于水
- D. 常温下呈固态
2.下列图示实验操作中,错误的是( )
- A.

点燃酒精灯 - B.
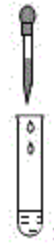
滴加液体 - C.
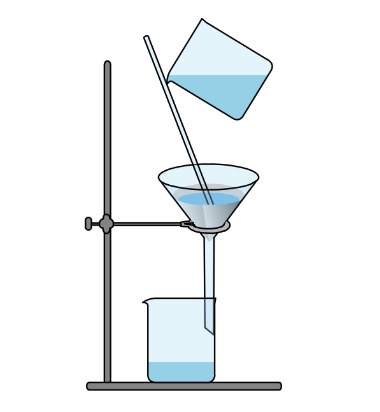
过滤 - D.
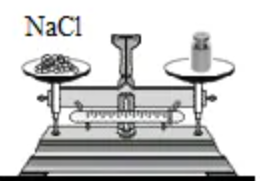
称量氯化钠
3.化学与生活息息相关。下列有关说法错误的是( )
- A. 软水和硬水可用肥皂水区分
- B. 糖类和油脂能为人体提供能量
- C. 化肥和农药可以任意施用
- D. 回收废弃塑料可以节约资源
4.碳酸氢钠(NaHCO3)是焙制糕点所用发酵粉的主要成分之一,下列有关说法正确的是( )
- A. NaHCO3中的阳离子为Na+2
- B. NaHCO3中碳元素的化合价为+2价
- C. 氧原子的结构示意图为
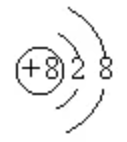
- D. NaHCO3中含有一种金属元素
5.一氧化氮是一种大气污染物。工业上利用氢气消除一氧化氮污染的微观示意图如图所示。
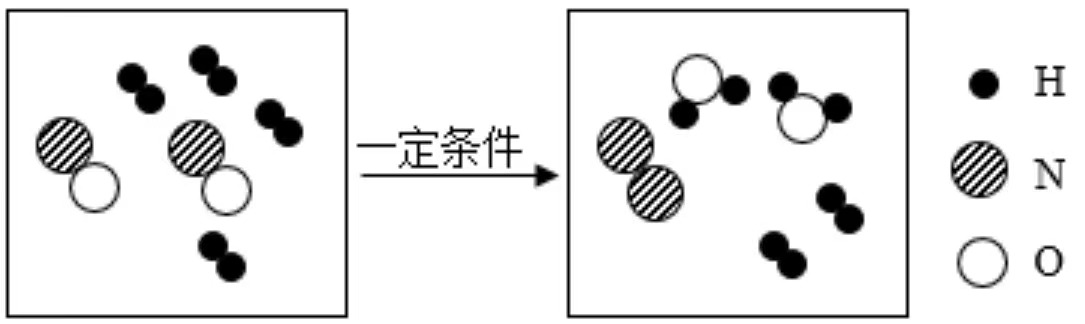
关于该反应说法错误的是( )

关于该反应说法错误的是( )
- A. 分子数目保持不变
- B. 体现了氢气的还原性
- C. 生成物中氮气和水的分子个数比为1:2
- D. 参加反应的氢气和一氧化氮的质量比为1:15
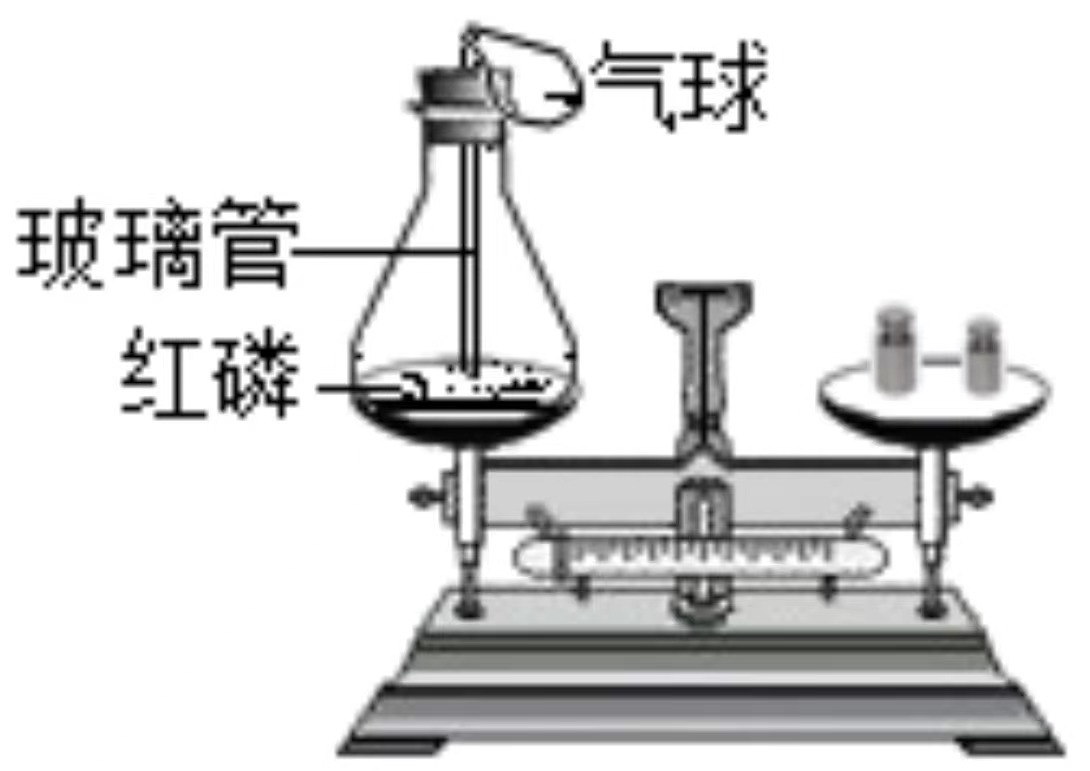
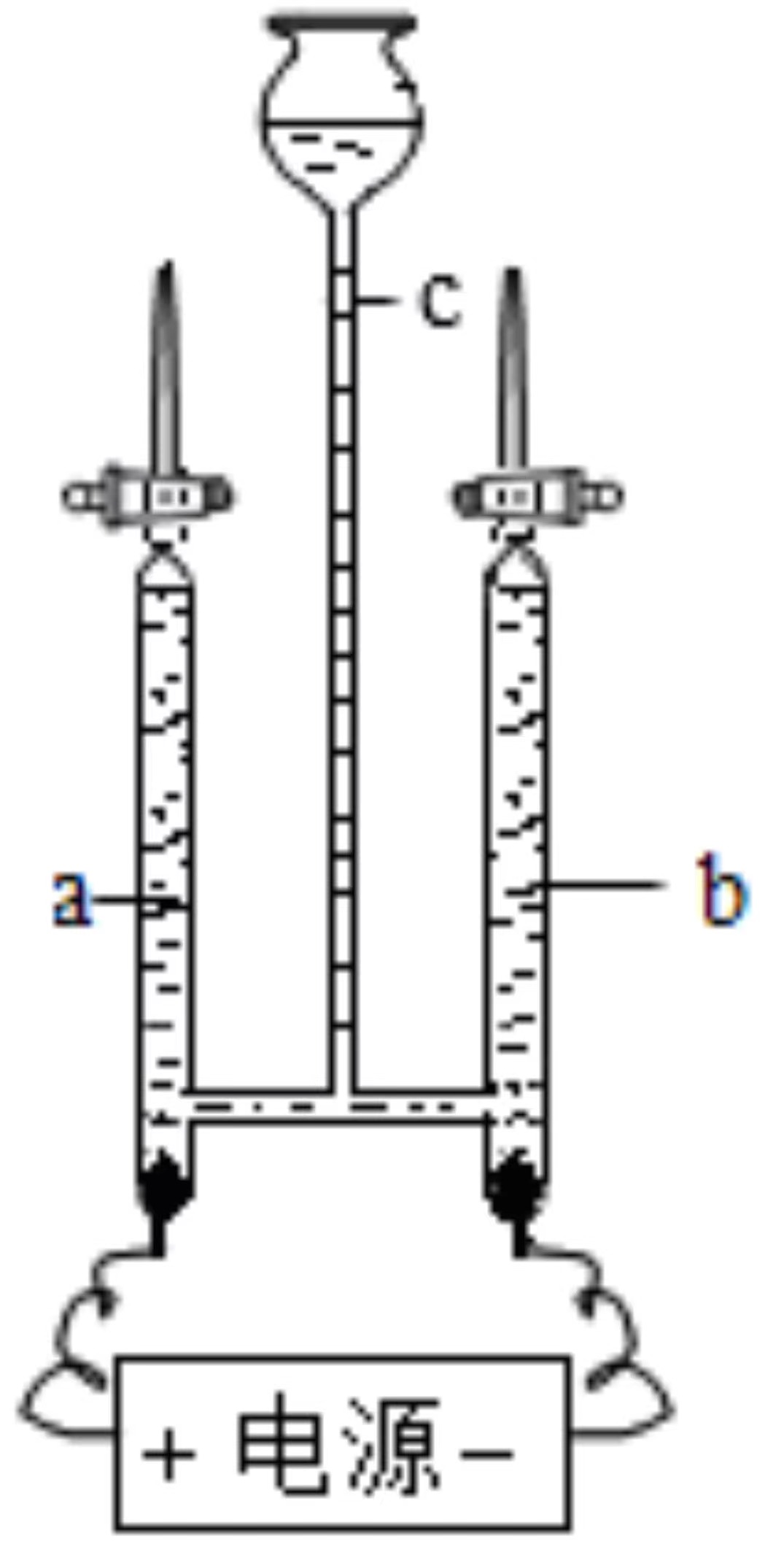
6.实验是学习化学的重要途径。如图均为初中化学探究实验。
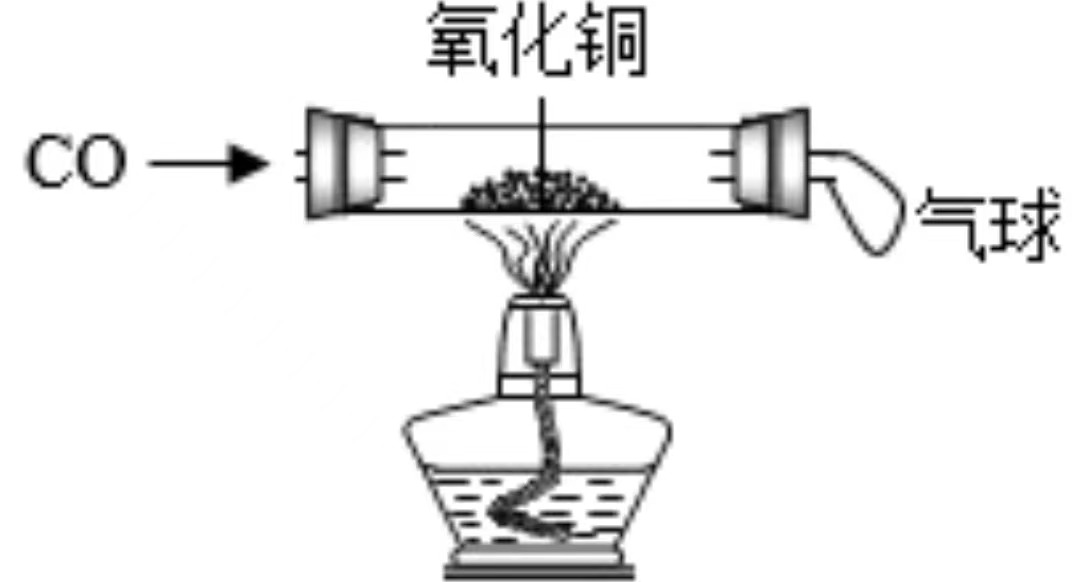
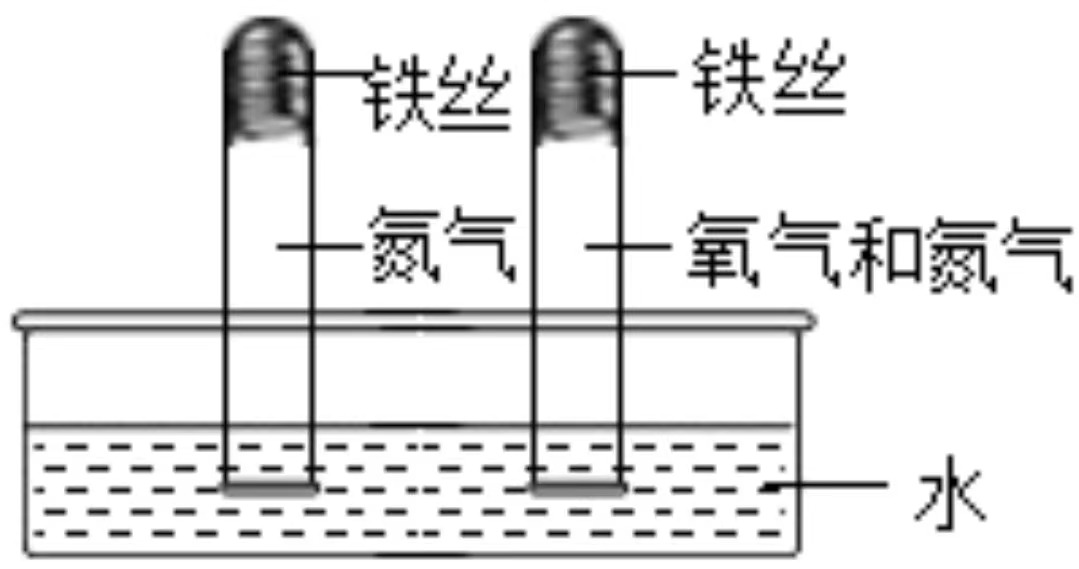
下列说法错误的是( )




下列说法错误的是( )
- A. 图甲验证质量守恒定律时红磷量不足,最终天平仍然保持平衡
- B. 图乙电解水一段时间后,管内液面高度:a>b>c
- C. 图丙反应后玻璃管内固体减少的质量小于生成气体中氧元素的质量
- D. 图丁实验可用于探究铁生锈是否需要氧气参与
7.分类、归纳是学习化学的有效方法,如图中物质甲、乙和反应Ⅰ、Ⅱ为初中化学常见的物质和反应。
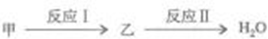
下列说法错误的是( )
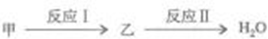
下列说法错误的是( )
- A. 若乙是光合作用的原料,则甲可以为有机化合物
- B. 若反应Ⅱ属于中和反应,则甲、乙可以均为碱
- C. 若反应Ⅰ、Ⅱ均属于复分解反应且甲属于盐,则乙可以为非金属氧化物
- D. 若反应Ⅰ、Ⅱ均属于置换反应且甲为金属单质,则乙可以为非金属单质
8.某兴趣小组发现实验室有一瓶忘了塞瓶塞的氢氧化钠溶液。为探究该溶液的变质程度并测定溶液中各成分的质量分数,进行了如下实验:
Ⅰ.取20.00g该溶液,加入过量的氯化钡溶液,过滤,得到滤渣和滤液。将滤渣洗涤、干燥后称量,其质量为1.97g。
Ⅱ.向滤液中逐滴加入质量分数为5%的硫酸镁溶液,生成沉淀的质量与加入硫酸镁溶液的质量关系如图所示。
下列说法正确的是( )
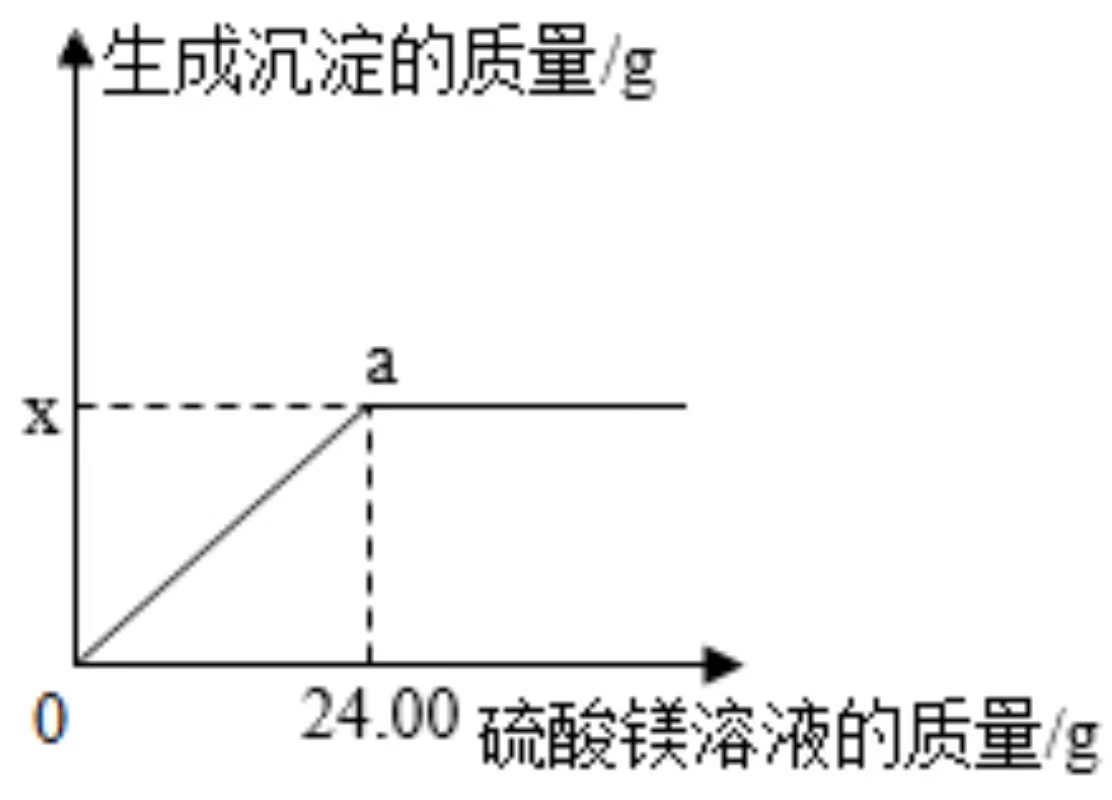
Ⅰ.取20.00g该溶液,加入过量的氯化钡溶液,过滤,得到滤渣和滤液。将滤渣洗涤、干燥后称量,其质量为1.97g。
Ⅱ.向滤液中逐滴加入质量分数为5%的硫酸镁溶液,生成沉淀的质量与加入硫酸镁溶液的质量关系如图所示。
下列说法正确的是( )

- A. 该溶液中碳酸钠的质量分数为10.6%
- B. 若x=2.91,则a点对应的溶液中只有一种溶质
- C. 若x=2.33,则该溶液部分变质
- D. 实验1中,可用稀硝酸和硝酸银溶液验证滤液中含有氯化钡
9.如图所示实验可以探究燃烧的条件。
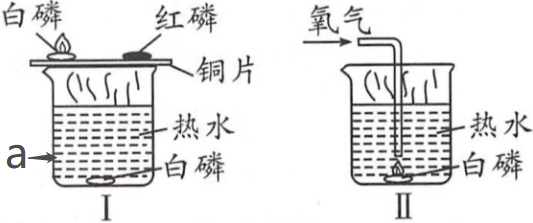
回答问题:
(1)仪器a的名称为 (填“烧杯”或“试管”)。
(2)实验1铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要 (填标号)。
A.可燃物
B.氧气(或空气)
C.达到可燃物的着火点
(3)实验2通入氧气,水中的白磷燃烧生成五氧化二磷(P2O5),该反应的化学方程式为 。

回答问题:
(1)仪器a的名称为 (填“烧杯”或“试管”)。
(2)实验1铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要 (填标号)。
A.可燃物
B.氧气(或空气)
C.达到可燃物的着火点
(3)实验2通入氧气,水中的白磷燃烧生成五氧化二磷(P2O5),该反应的化学方程式为 。
10.溶液在日常生活、工农业生产和科学研究中具有广泛用途。氢氧化钙、硝酸钾、氯化钠的溶解度如下表所示。
回答问题:
(1)氢氧化钙的溶解度随温度的升高而 (填“增大”或“减小”)。
(2)将接近饱和的硝酸钾溶液变为饱和溶液,可以采用的一种方法是 。
(3)农业上常用质量分数为16%的氯化钠溶液选种。20℃时,将136g饱和氯化钠溶液稀释成质量分数为16%的氯化钠溶液,需加水的质量为 。
(4)下列有关说法正确的是 (填标号)。
A.40℃时,向氢氧化钙饱和溶液中加入少量硝酸钾,溶液质量变大
B.60℃时,将100g硝酸钾饱和溶液恒温蒸发10g水,析出11g硝酸钾
C.某物质的不饱和溶液,其溶质的质量分数可能比该物质的饱和溶液大
D.将80℃时上述三种物质的饱和溶液各mg分别降温至20℃,所得溶液中,氯化钠溶液的质量最大
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | 氢氧化钙 | 0.18 | 0.16 | 0.14 | 0.11 | 0.09 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
| 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | |
回答问题:
(1)氢氧化钙的溶解度随温度的升高而 (填“增大”或“减小”)。
(2)将接近饱和的硝酸钾溶液变为饱和溶液,可以采用的一种方法是 。
(3)农业上常用质量分数为16%的氯化钠溶液选种。20℃时,将136g饱和氯化钠溶液稀释成质量分数为16%的氯化钠溶液,需加水的质量为 。
(4)下列有关说法正确的是 (填标号)。
A.40℃时,向氢氧化钙饱和溶液中加入少量硝酸钾,溶液质量变大
B.60℃时,将100g硝酸钾饱和溶液恒温蒸发10g水,析出11g硝酸钾
C.某物质的不饱和溶液,其溶质的质量分数可能比该物质的饱和溶液大
D.将80℃时上述三种物质的饱和溶液各mg分别降温至20℃,所得溶液中,氯化钠溶液的质量最大
11.某化工厂以废金属(主要成分为Fe和Cu,表面有少量油污)为原料回收海绵铜,并制备氯化铁的工艺流程如图所示。
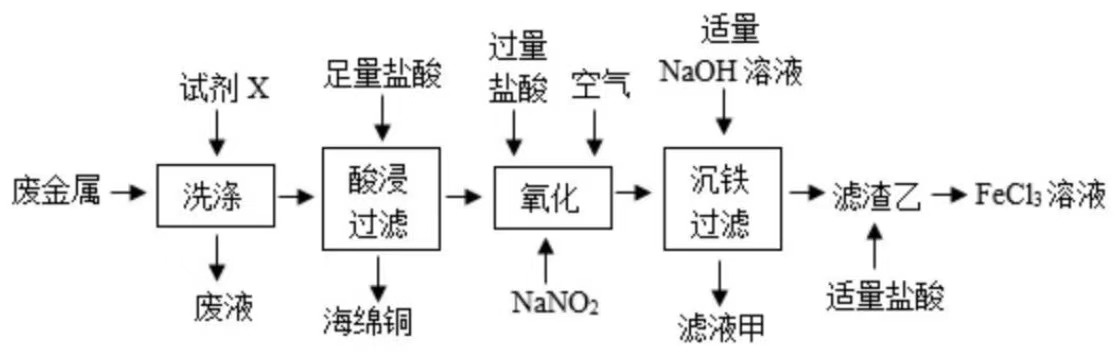
已知:NaNO2易溶于水且不与氢氧化钠反应,在“氧化”中起催化作用,该反应的化学方程式为:4FeCl2+4HCl+O2
4FeCl3+2H2O
回答问题:
(1)废金属属于 (填“纯净物”或“混合物”)。
(2)“洗涤”的目的是去除废金属表面的油污,试剂X最好选用 (填标号)。
A.水
B.氢氧化钠溶液
C.稀硫酸
D.氯化钠溶液
(3)“酸浸”中发生反应的化学方程式为 。
(4)“滤液甲”中一定含有的溶质是 。
(5)向“滤渣乙”中加入适量盐酸,可以观察到的现象是 。

已知:NaNO2易溶于水且不与氢氧化钠反应,在“氧化”中起催化作用,该反应的化学方程式为:4FeCl2+4HCl+O2
| NaNO2 |
回答问题:
(1)废金属属于 (填“纯净物”或“混合物”)。
(2)“洗涤”的目的是去除废金属表面的油污,试剂X最好选用 (填标号)。
A.水
B.氢氧化钠溶液
C.稀硫酸
D.氯化钠溶液
(3)“酸浸”中发生反应的化学方程式为 。
(4)“滤液甲”中一定含有的溶质是 。
(5)向“滤渣乙”中加入适量盐酸,可以观察到的现象是 。
12.某学习小组仿照拉姆塞发现稀有气体的实验原理,用如图所示装置测定空气中氧气的质量分数,并制备少量氮化镁。(碱石灰是氧化钙和氢氧化钠的混合物,装置气密性良好,夹持装置已略去,忽略气体密度变化)

已知:①点燃或加热时,镁与氮气反应生成氮化镁固体(其中氮元素为-3价)。
②装置丁内收集到气体的密度为ρg/mL。
部分实验步骤:
Ⅰ.装入药品,连接装置,点燃甲处酒精灯,通入一段时间空气。
Ⅱ.点燃丙处酒精灯,继续通入一段时间空气。
Ⅲ.停止通入空气,熄灭酒精灯,冷却至室温。
实验测得数据:装置甲、丙硬质玻璃管内固体质量分别增加m1g、m2g;装置乙质量增加m3g;最终装置戊量筒里水的体积为VmL。
回答问题:
(1)空气中能供给呼吸的气体是 (填化学式)。
(2)装置甲硬质玻璃管内观察到的实验现象是 。
(3)装置丙硬质玻璃管内发生反应的化学方程式为 。
(4)步骤Ⅰ中点燃甲处酒精灯,通入一段时间空气的目的是 。
(5)空气中氧气的质量分数为 (用m1、m2、m3、ρ、V的代数式表示)。

已知:①点燃或加热时,镁与氮气反应生成氮化镁固体(其中氮元素为-3价)。
②装置丁内收集到气体的密度为ρg/mL。
部分实验步骤:
Ⅰ.装入药品,连接装置,点燃甲处酒精灯,通入一段时间空气。
Ⅱ.点燃丙处酒精灯,继续通入一段时间空气。
Ⅲ.停止通入空气,熄灭酒精灯,冷却至室温。
实验测得数据:装置甲、丙硬质玻璃管内固体质量分别增加m1g、m2g;装置乙质量增加m3g;最终装置戊量筒里水的体积为VmL。
回答问题:
(1)空气中能供给呼吸的气体是 (填化学式)。
(2)装置甲硬质玻璃管内观察到的实验现象是 。
(3)装置丙硬质玻璃管内发生反应的化学方程式为 。
(4)步骤Ⅰ中点燃甲处酒精灯,通入一段时间空气的目的是 。
(5)空气中氧气的质量分数为 (用m1、m2、m3、ρ、V的代数式表示)。
13.某兴趣小组用氧化铜和稀硫酸制取硫酸铜溶液。向盛有一定质量氧化铜的烧杯中加入100.0g稀硫酸,恰好完全反应,得到104.0g溶液。
回答问题:
(1)稀硫酸的pH 7(填“<”“=”或“>”)。
(2)求所得溶液中硫酸铜的质量分数(精确到0.1%)。
回答问题:
(1)稀硫酸的pH 7(填“<”“=”或“>”)。
(2)求所得溶液中硫酸铜的质量分数(精确到0.1%)。
查看全部题目