下载高清试卷
【2022年河南省中考化学试卷】-第1页
试卷格式:2022年河南省中考化学试卷.PDF
试卷热词:最新试卷、2022年、河南试卷、化学试卷、九年级试卷、中考试卷、初中试卷

扫码查看解析
试卷题目
1.中原大地物产丰富。下列食材或食品中富含蛋白质的是( )
- A. 原阳大米
- B. 灵宝苹果
- C. 叶县岩盐
- D. 固始鸡蛋
2.元素周期表是学习化学的工具。发现元素周期律并编制元素周期表的化学家是( )
- A. 拉瓦锡
- B. 道尔顿
- C. 门捷列夫
- D. 阿伏加德罗
3.酸雨对农作物以及一些建筑有不利影响。下列措施中与酸雨的防治有关的是( )
- A. 控制二氧化碳的排放量
- B. 减少使用一次性塑料制品
- C. 分类回收处理生活垃圾
- D. 减少含硫化石燃料的燃烧
4.《天工开物》中记载了古法造纸工艺。下列步骤中一定发生了化学变化的是( )
- A. 煮楻足火
- B. 斩竹槌洗
- C. 日晒成干
- D. 覆帘压纸
5.装运汽油或乙醇的运输车上,所贴的危险化学品标志为( )
- A.

- B.

- C.

- D.

6.有机合成材料的应用和发展方便了人类的生活。下列不属于有机合成材料的是( )
- A. 塑料
- B. 陶瓷
- C. 合成橡胶
- D. 合成纤维
7.物质由微观粒子构成。下列都由离子构成的一组物质是( )
- A. 氯化钠、硫酸铜
- B. 水、干冰
- C. 金刚石、氧化汞
- D. 氦气、氨气
8.粮食产量增长的主要动力是化肥。下列化肥(用化学式表示)属于复合肥料的是( )
- A. CO(NH2)2
- B. K2SO4
- C. KNO3
- D. C a(H2PO4)2
9.正确的实验操作是实验成功的重要保证。下列实验操作中正确的是( )
- A.
 熄灭酒精灯
熄灭酒精灯 - B.
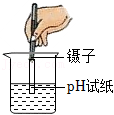 测溶液的pH
测溶液的pH - C.
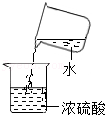 稀释浓硫酸
稀释浓硫酸 - D.
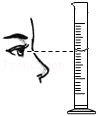 读液体体积
读液体体积
10.日常生活中,人们常用84消毒液对环境进行消毒。84消毒液是常见的含氯消毒剂,其有效成分中的氯元素为+1价,则84消毒液的有效成分是( )
- A. 氯化钠(NaCl)
- B. 次氯酸钠(NaClO)
- C. 氯酸钠(NaClO3)
- D. 亚氯酸钠(NaClO2)
11.人类的日常生活和工农业生产离不开水。下列关于水的叙述不正确的是( )
- A. 水与冰块混合得到混合物
- B. 净水常用方法有沉淀、过滤、吸附、蒸馏等
- C. 硬水是指含有较多可溶性钙、镁化合物的水
- D. 水电解时所产生的氢气和氧气的质量比为1:8
12.某金属混合物由Mg、Al、Zn、Cu四种金属中的两种组成。6.5g该金属混合物与足量的盐酸反应,可得到0.2g氢气,则该金属混合物中一定不含有的金属是( )
- A. Mg
- B. Al
- C. Zn
- D. Cu
13.甲、乙、丙的转化关系如图所示(“→”表示反应能一步实现,部分物质和反应条件已略去),则符合要求的甲、乙、丙依次为( )


- A. CaO、Ca(OH)2、CaCO3
- B. H2、H2O、H2O2
- C. CuO、Cu(OH)2、CuSO4
- D. C、CO2、H2CO3
14.天然气的主要成分是甲烷(CH4)。当氧气不足时,甲烷燃烧会生成CO2、CO和H2O,若16g甲烷燃烧生成CO2和CO的质量比为11:7,则参加反应的O2的质量为( )
- A. 48g
- B. 56g
- C. 64g
- D. 72g
15.在空气中含量高且化学性质不活泼的气体是 ;地壳中含量最高的金属元素是 ;形成化合物种类最多的元素是 。
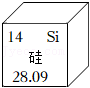
16.如图是元素周期表中的一格。硅的相对原子质量为 ;硅原子核外电子有三层,最外层有4个电子,其原子结构示意图为 ;硅元素在元素周期表中位于第 周期。

17.氢氧化钙固体的溶解度曲线如图所示。
(1)由图可知,氧氧化钙的溶解度随着温度的升高而 (填“增大“或“减小”)。
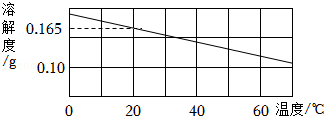
(2)20℃时,氢氧化钙饱和溶液中溶质的质量分数为 (写出计算式即可)。
(1)由图可知,氧氧化钙的溶解度随着温度的升高而 (填“增大“或“减小”)。

(2)20℃时,氢氧化钙饱和溶液中溶质的质量分数为 (写出计算式即可)。
18.实验室用氯化钠固体配制50g质量分数为6%的溶液,实验步骤为计算、 、量取、溶解;水的密度近似看做1g/cm3,量取水时所选用量筒的规格应为 (填“10mL”“50mL”或“100mL”)。
19.如图是某胃药标签的部分文字说明。碳酸氢钠与胃酸(含盐酸)作用的化学方程式为 ;如果将该胃药中的碳酸氢钠用相同质量的碳酸镁代替,则每次用药量应 (填“增加”“减少”或“不变”)。


20.A﹣F是含同一种金属元素的物质,它们的转化关系如图所示(“→”表示反应能一步实现,部分物质和反应条件已略去),图中标注了物质类别和这种金属元素的化合价。已知A与一氧化碳反应是工业制取B的主要原理,B是目前世界年产量最高的金属。
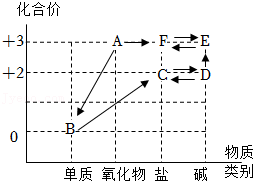
(1)这种金属元素属于人体必需的 (填“常量元素”或“微量元素”)。
(2)A的化学式为 ;B与稀硫酸反应生成C的化学方程式为 。
(3)D与氧气、水可以发生化合反应生成E,该反应的化学方程式为 。

(1)这种金属元素属于人体必需的 (填“常量元素”或“微量元素”)。
(2)A的化学式为 ;B与稀硫酸反应生成C的化学方程式为 。
(3)D与氧气、水可以发生化合反应生成E,该反应的化学方程式为 。
21.从分子的角度解释下列生活中的现象。
(1)墙内开花墙外可以闻到花香。
(2)一壶水烧开后,壶盖会被顶开。
(1)墙内开花墙外可以闻到花香。
(2)一壶水烧开后,壶盖会被顶开。
22.某化学小组用如图所示装置进行探究实验。
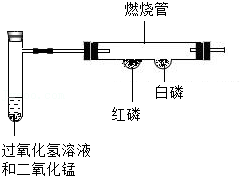
(1)写出试管中所发生反应的化学方程式。
(2)均匀微热燃烧管,观察到白磷燃烧而红磷不燃烧,由此说明燃烧需要什么条件?

(1)写出试管中所发生反应的化学方程式。
(2)均匀微热燃烧管,观察到白磷燃烧而红磷不燃烧,由此说明燃烧需要什么条件?
23.金属用途广泛,金属的用途与其性质密切相关。
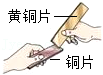
(1)如图中将两块金属片相互刻画,该实验的目的是什么?
(2)某同学在Cu(NO3)2和AgNO3的混合溶液中加入一定质量的锌粉,充分反应后过滤,发现滤液仍呈蓝色。分析滤液中溶质的成分,并写出Zn与AgNO3溶液反应的化学方程式。

(1)如图中将两块金属片相互刻画,该实验的目的是什么?
(2)某同学在Cu(NO3)2和AgNO3的混合溶液中加入一定质量的锌粉,充分反应后过滤,发现滤液仍呈蓝色。分析滤液中溶质的成分,并写出Zn与AgNO3溶液反应的化学方程式。
24.实验室可选用如图所示装置制取气体。
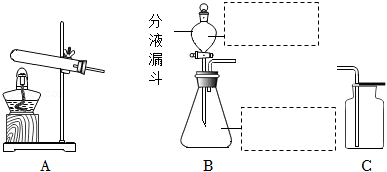
(1)写出利用A制取O2的化学方程式。
(2)若利用B制取CO2,请将开始时所加的药品分别填写在图中相应的虚线框内。
(3)若利用C收集到一瓶无色无味的气体。猜想一种气体并用简单方法加以验证。

(1)写出利用A制取O2的化学方程式。
(2)若利用B制取CO2,请将开始时所加的药品分别填写在图中相应的虚线框内。
(3)若利用C收集到一瓶无色无味的气体。猜想一种气体并用简单方法加以验证。
25.酸、碱、盐是几类重要化合物,它们与人类日常生活和工农业生产关系十分密切。
(1)在实验室常用浓硫酸做干燥剂,这是因为浓硫酸具有 (填字母)。
a.酸性
b.吸水性
c.氧化性
d.脱水性
(2)请简述氢氧化钙(俗称熟石灰)在生产或生活中的一种用途。
(3)中和反应是化学学习和研究的重要内容。
①如图是氢氧化钠溶液与盐酸反应的示意图。用实际参加反应的离子符号来表示该反应的式子可写为 。
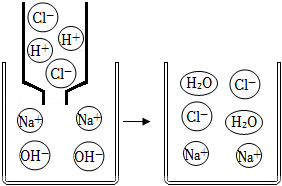
②若向稀氢氧化钠溶液中滴入几滴酚酞溶液,然后再向其中滴入稀盐酸至过量,则观察到溶液颜色的变化是 。
(4)食盐(主要成分是NaCl)除可用作调味品外,还是一种重要化工原料。晾晒海水所得到的粗盐中含有不溶性杂质(泥沙)和可溶性杂质(CaCl2、MgCl2、Na2SO4),如图是某化学小组在实验室对粗盐样品进行除杂提纯的过程。
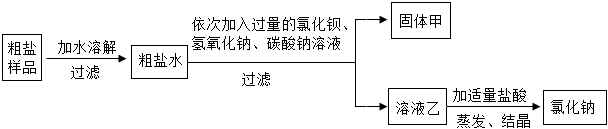
①溶解、过滤、蒸发的操作中都需要用到的一种玻璃仪器为 (填“烧杯”“漏斗”或“玻璃棒”)。
②固体甲中所含有的难溶性物质为BaSO4、 、CaCO3和BaCO3。
③请设计实验验证溶液乙中所含有的杂质。(简要叙述实验步骤及现象)
(5)工业废水需处理达到标准后再排放,以免造成水体污染。某造纸厂欲排放200t含NaOH的废水,其中NaOH的质量分数为1.6%,用废硫酸(H2SO4的质量分数为20%)来处理该废水至中性,需要这种废硫酸的质量是多少?
(1)在实验室常用浓硫酸做干燥剂,这是因为浓硫酸具有 (填字母)。
a.酸性
b.吸水性
c.氧化性
d.脱水性
(2)请简述氢氧化钙(俗称熟石灰)在生产或生活中的一种用途。
(3)中和反应是化学学习和研究的重要内容。
①如图是氢氧化钠溶液与盐酸反应的示意图。用实际参加反应的离子符号来表示该反应的式子可写为 。

②若向稀氢氧化钠溶液中滴入几滴酚酞溶液,然后再向其中滴入稀盐酸至过量,则观察到溶液颜色的变化是 。
(4)食盐(主要成分是NaCl)除可用作调味品外,还是一种重要化工原料。晾晒海水所得到的粗盐中含有不溶性杂质(泥沙)和可溶性杂质(CaCl2、MgCl2、Na2SO4),如图是某化学小组在实验室对粗盐样品进行除杂提纯的过程。

①溶解、过滤、蒸发的操作中都需要用到的一种玻璃仪器为 (填“烧杯”“漏斗”或“玻璃棒”)。
②固体甲中所含有的难溶性物质为BaSO4、 、CaCO3和BaCO3。
③请设计实验验证溶液乙中所含有的杂质。(简要叙述实验步骤及现象)
(5)工业废水需处理达到标准后再排放,以免造成水体污染。某造纸厂欲排放200t含NaOH的废水,其中NaOH的质量分数为1.6%,用废硫酸(H2SO4的质量分数为20%)来处理该废水至中性,需要这种废硫酸的质量是多少?
查看全部题目