下载高清试卷
【2021-2022学年江苏省扬州市广陵区九年级(上)期末化学试卷】-第1页
试卷格式:2021-2022学年江苏省扬州市广陵区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2021年、江苏试卷、扬州市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷

扫码查看解析
试卷题目
1.2021年世界环境日中国主题是“人与自然和谐共生”。下列做法不符合此主题的是( )
- A. 长江十年禁捕
- B. 爱护鸟类及动物
- C. 焚烧秸秆归田
- D. 循环利用水资源
2.生活中的很多现象与物质变化有关,下列属于化学变化的是( )
- A. 水结成冰
- B. 汽油挥发
- C. 干冰升华
- D. 煤油燃烧
3.人体中含有多种元素。下列属于人体必需微量元素的是( )
- A. 碳
- B. 氢
- C. 氧
- D. 锌
4.下列物质由分子构成的是( )
- A. 氢气
- B. 铜片
- C. 石墨
- D. 氯化钠
5.生活中用到的下列物质,属于纯净物的是( )
- A. 温度计中水银
- B. 取暖用的煤炭
- C. 调味用的食醋
- D. 饮料用的果汁
6.下列物质分别加入适量水中充分搅拌,能得到溶液的是( )
- A. 粉笔灰
- B. 植物油
- C. 蔗糖
- D. 面粉
7.金属镁可以发生反应:2Mg+X
2MgO+C,则X的化学式为( )
点燃 |
- A. O2
- B. CO2
- C. CO
- D. CH4
8.下列实验操作正确的是( )
- A.
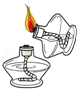 点燃酒精灯
点燃酒精灯 - B.
 向试管中加入固体
向试管中加入固体 - C.
 闻气体气味
闻气体气味 - D.
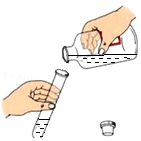 倾倒液体
倾倒液体
9.铜锌合金又称之为“假黄金”。下列辨别真、假黄金的方法中错误的是( )
- A. 加盐酸
- B. 测密度
- C. 用火烧
- D. 看颜色
10.传统中药“金银花”的有效成分中含有一种名为绿原酸(C16H18O9) 的物质,下列说法正确的是( )
- A. 绿原酸由三种元素组成
- B. 绿原酸的相对分子质量为354g
- C. 绿原酸中氢元素的质量分数最大
- D. 绿原酸由16个碳原子、18个氢原子和9个氧原子构成
11.下列说法正确的是( )
- A. 煮沸的鸡汤比煮沸的水温度高
- B. 溶液都具有导电性
- C. 溶液都是均一、稳定、无色的液体
- D. 汽油洗去手上的油污属于乳化
12.某化学反应的微观示意图如图,下列说法正确的是( )
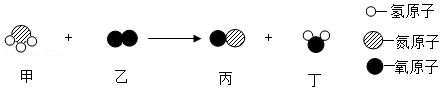

- A. 反应前后分子总数不变
- B. 甲分子中氮、氢原子个数比为3:1
- C. 甲、乙两物质反应的质量比为17:40
- D. 氮元素的化合价在反应前后没有变化
13.下列实验现象的描述错误的是( )
- A. 铁丝在氧气中燃烧发出白光,生成白色固体
- B. 把铁粉放入稀硫酸中可以看到有气泡产生,溶液逐渐由无色变为浅绿色
- C. 将铜片在空气中加热,表面逐渐变黑
- D. 镁带在空气中燃烧,发出耀眼白光,生成白色固体
14.为了防止钢铁制品锈蚀,下列做法不当的是( )
- A. 在铁制品表面镀上一层锌
- B. 在车船的表面喷涂油漆
- C. 将使用后的菜刀用布擦干
- D. 用洗涤剂把铁制品表面的油膜洗净
15.“绿色化学”的特点之一是“零排放”,即只生成一种产物。在一定条件下,CO2和H2按适当比例反应就能实现“零排放”,该产物化学式是( )
- A. CH4O
- B. CH2O2
- C. C2H6O
- D. C2H4O2
16.海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各离子不能通过淡化膜,从而得到淡水,对加压后右侧海水成分变化进行分析,正确的是( )
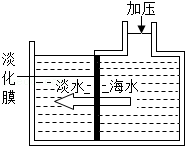

- A. 溶质质量增加
- B. 溶剂质量减少
- C. 溶液质量不变
- D. 溶质质量分数不变
17.物质的性质决定用途。下列说法错误的是( )
- A. 氮气化学性质稳定,可作食品保护气
- B. 干冰升华吸热,可用于人工降雨
- C. 氧气具有助燃性,可用作烹饪燃料
- D. 盐溶液凝固点降低,可用于融雪剂
18.硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是( )
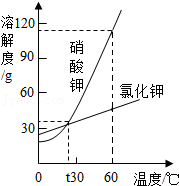

- A. 硝酸钾的溶解度一定大于氯化钾的溶解度
- B. 降低温度可使接近饱和的硝酸钾溶液变饱和
- C. t℃时,硝酸钾和氯化钾两种溶液的溶质质量分数一定相等
- D. 60℃时,100g水中加入90g硝酸钾,充分搅拌,可得到硝酸钾的饱和溶液
19.某碳酸钙和氧化钙组成的固体混合物中钙元素的质量分数为60%,将50g该混合物高温煅烧至固体质量不再改变(已知CaCO3
CaO+CO2↑),则生成二氧化碳的质量是( )
| 高温 |
- A. 6g
- B. 13.2g
- C. 20g
- D. 8g
20.氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示。下列说法错误的是( )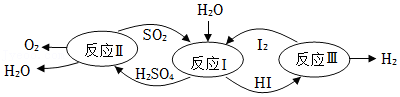

- A. 反应I、II、III都是分解反应
- B. 总反应是H2O分解产生H2和O2
- C. 理论上,每产生1kg氢气需消耗9kg的水
- D. 此制氢方法可解决能源危机问题
21.化学用语是学习化学的重要工具。请用化学用语表示下列物质:
(1)空气中含量最高的气体 ;
(2)氧化亚铁中铁显+2价 ;
(3)能供给呼吸的气体是 ;
(4)稀硫酸中含有大量的阴离子是 ;
(5)人体含量最多的金属元素 ;
(6)含氧量最高的氧化物 ;
(7)生铁和钢都是铁与 的合金;
(8)用于制造光导纤维的石英砂,其主要成分是 。
(1)空气中含量最高的气体 ;
(2)氧化亚铁中铁显+2价 ;
(3)能供给呼吸的气体是 ;
(4)稀硫酸中含有大量的阴离子是 ;
(5)人体含量最多的金属元素 ;
(6)含氧量最高的氧化物 ;
(7)生铁和钢都是铁与 的合金;
(8)用于制造光导纤维的石英砂,其主要成分是 。
22.化学源于生活又服务于生活。请用化学知识解释下列问题:
(1)喝了汽水后常常打嗝,原因是温度升高使气体溶解度 ;
(2)食物保存在冰箱中不易变质,是化学反应速率与 有关;
(3)铁元素是人体必需的一种微量元素。食用“加铁酱油”可预防 ;
(4)加碘食盐中的“碘”是指 (填“原子”、“分子”或“元素”)。
(1)喝了汽水后常常打嗝,原因是温度升高使气体溶解度 ;
(2)食物保存在冰箱中不易变质,是化学反应速率与 有关;
(3)铁元素是人体必需的一种微量元素。食用“加铁酱油”可预防 ;
(4)加碘食盐中的“碘”是指 (填“原子”、“分子”或“元素”)。
23.多彩的“碳”带来多姿的生活。请用“碳”的化学知识回答下列问题:
(1)根据下表中提供的信息,填写有关含碳物质的对应性质
(2)液态二氧化碳可用于扑救图书、档案资料室发生的火灾,下列说法正确的是 。
A.液态二氧化碳汽化后不留有水分而使图书、档案资料保持干燥
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低了周围环境温度
(3)二氧化碳是一种宝贵的资源。固定和利用CO2成功典范之一是在阳光下,绿色植物通过光合作用把CO2和H2O合成 ,同时生成O2.成功典范之二在高温高压下,CO2和NH3合成尿素〔CO(NH2)2〕,同时生成水,该反应的化学方程式为 。
(4)目前城市居民主要以天然气为燃料,天然气的主要成分是甲烷(CH4),请写出甲烷在空气中燃烧的化学反应方程式 。
(5)空气中CO2含量过高就会导致 ,“低碳”生活是现代公民必须倡导的生活理念,下列做法符合“坚持绿色发展,建设生态扬州”宗旨的是 。
A.建设生态绿地,打造绿色家园
B.发展电动公交,减少尾气排放
C.鼓励燃煤发电,保障电力供应
(1)根据下表中提供的信息,填写有关含碳物质的对应性质
| 物质用途 | 石墨作电极 | 金刚石切割玻璃 | 活性炭净水 |
| 对应性质 | 导电性 |
(2)液态二氧化碳可用于扑救图书、档案资料室发生的火灾,下列说法正确的是 。
A.液态二氧化碳汽化后不留有水分而使图书、档案资料保持干燥
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低了周围环境温度
(3)二氧化碳是一种宝贵的资源。固定和利用CO2成功典范之一是在阳光下,绿色植物通过光合作用把CO2和H2O合成 ,同时生成O2.成功典范之二在高温高压下,CO2和NH3合成尿素〔CO(NH2)2〕,同时生成水,该反应的化学方程式为 。
(4)目前城市居民主要以天然气为燃料,天然气的主要成分是甲烷(CH4),请写出甲烷在空气中燃烧的化学反应方程式 。
(5)空气中CO2含量过高就会导致 ,“低碳”生活是现代公民必须倡导的生活理念,下列做法符合“坚持绿色发展,建设生态扬州”宗旨的是 。
A.建设生态绿地,打造绿色家园
B.发展电动公交,减少尾气排放
C.鼓励燃煤发电,保障电力供应
24.阅读科普短文,并回答相关问题:
金属材料就像人类的左臂右膀,伴随着我们从原始的荒蛮社会,一起走进今天的现代化文明世界。人类最早发现和使用的金属是紫铜,紫铜就是纯铜,硬度低,最终没有能取代石器成为主要的工具材料。后来人们发现了另外一种金属﹣锡(Sn),这种柔软的银白色金属熔点很低(231℃),它们大多数以氧化物的形式分布在锡石中,因为它软及低温下不易被氧化,于是被人们碾成极薄的薄片用来包裹物品或器具,直到后来被“铝箔纸”替代,以致现在的“铝箔纸”俗称“锡纸”。
金一直被视为财富的象征。现在的金大多数是地球形成初期小天体撞击地球时被熔化留下的,且密度大而沉往地心,因而很难开采。金还是天然货币,金的贵重在于它的稀少和性质不活泼。汞是一种常温下呈液态的金属,凝固点为﹣38.87℃,如水又似银,温度对汞的体积变化影响明显。
随着时代科技的发展,柔软的纯金属逐渐被坚硬的合金替代。制备合金的原理很简单,把不同的金属单质放在一起加热成液态,形成均匀的液体并冷凝下来即可。合金一般以一种成分为主体,少量的其它金属或非金属掺杂其中,不过别小看这少量的杂质,让主体材料的性质发生翻天覆地的变化。以铜为例,铜的合金就有“青铜”、“黄铜”与“白铜”(铜镍合金),这些铜合金后来被用于铸造钱币和塑像。《本草纲目》记载:“炉甘石大小不一,状如羊脑,松如石脂,赤铜得之,即化为黄。今之黄铜皆此物点化也”。《天工开物》中也有详尽:“每红铜六斤,入倭铅四斤,先后入罐熔化,冷定取出,即成黄铜”。
(1)锡易被碾成极薄的薄片用来包裹物品或器具,说明锡具有 性;“锡纸”实质是金属 ,锡的化合价通常为+4价,则它的氧化物化学式为 ;
(2)金的元素符号为 ;
(3)“倭铅”是指金属 ,“青铜”是铜与 的合金;
(4)熔点:纯铜 黄铜(填“>”、“=”或“<”);
金属材料就像人类的左臂右膀,伴随着我们从原始的荒蛮社会,一起走进今天的现代化文明世界。人类最早发现和使用的金属是紫铜,紫铜就是纯铜,硬度低,最终没有能取代石器成为主要的工具材料。后来人们发现了另外一种金属﹣锡(Sn),这种柔软的银白色金属熔点很低(231℃),它们大多数以氧化物的形式分布在锡石中,因为它软及低温下不易被氧化,于是被人们碾成极薄的薄片用来包裹物品或器具,直到后来被“铝箔纸”替代,以致现在的“铝箔纸”俗称“锡纸”。
金一直被视为财富的象征。现在的金大多数是地球形成初期小天体撞击地球时被熔化留下的,且密度大而沉往地心,因而很难开采。金还是天然货币,金的贵重在于它的稀少和性质不活泼。汞是一种常温下呈液态的金属,凝固点为﹣38.87℃,如水又似银,温度对汞的体积变化影响明显。
随着时代科技的发展,柔软的纯金属逐渐被坚硬的合金替代。制备合金的原理很简单,把不同的金属单质放在一起加热成液态,形成均匀的液体并冷凝下来即可。合金一般以一种成分为主体,少量的其它金属或非金属掺杂其中,不过别小看这少量的杂质,让主体材料的性质发生翻天覆地的变化。以铜为例,铜的合金就有“青铜”、“黄铜”与“白铜”(铜镍合金),这些铜合金后来被用于铸造钱币和塑像。《本草纲目》记载:“炉甘石大小不一,状如羊脑,松如石脂,赤铜得之,即化为黄。今之黄铜皆此物点化也”。《天工开物》中也有详尽:“每红铜六斤,入倭铅四斤,先后入罐熔化,冷定取出,即成黄铜”。
(1)锡易被碾成极薄的薄片用来包裹物品或器具,说明锡具有 性;“锡纸”实质是金属 ,锡的化合价通常为+4价,则它的氧化物化学式为 ;
(2)金的元素符号为 ;
(3)“倭铅”是指金属 ,“青铜”是铜与 的合金;
(4)熔点:纯铜 黄铜(填“>”、“=”或“<”);
25.水是维系生命的重要物质,生活与化学实验中都会用到水。
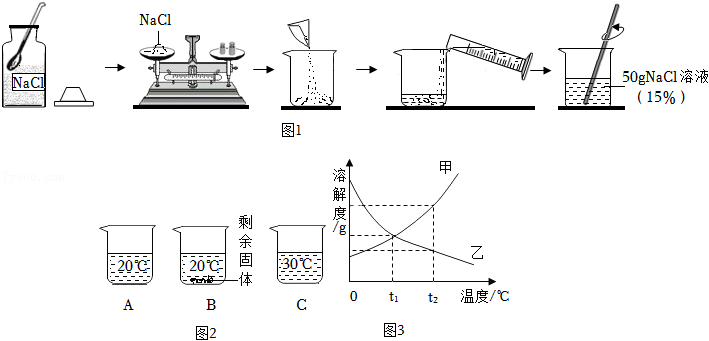
(1)实验室配制一定溶质质量分数的NaCl溶液的流程图如图1:
①应称量 g NaCl固体。
②若称量NaCl固体时指针略向右偏转,其实验操作方法: 。
③实验中加快NaCl固体溶解,合理的方法有 (填序号)。
A.用玻璃棒搅拌
B.用热水溶解
C.用研钵将NaCl固体研碎
④下列操作中可能导致配制NaCl溶液的溶质质量分数偏小的是 (填序号)。
A.NaCl中含有少量杂质
B.量取水时仰视
C.内壁蘸有少量水的烧杯溶解NaCl
D.转移时,有少量溶液溅出
⑤若取上述溶液20g,将其稀释为5%的NaCl溶液,则需加 g水。
(2)装有等量的水的A、B、C烧杯中分别加入10g、20g、25g某固体物质,充分溶解后,现象如图2所示。
①三个烧杯中溶质质量分数最大的溶液 (填“A”“B”或“C”)。
②A、B、C中一定属于饱和溶液的是 (填“A”“B”或“C”)。
③如图3中能表示该固体溶解度曲线的是 (填“甲”或“乙”)。

(1)实验室配制一定溶质质量分数的NaCl溶液的流程图如图1:
①应称量 g NaCl固体。
②若称量NaCl固体时指针略向右偏转,其实验操作方法: 。
③实验中加快NaCl固体溶解,合理的方法有 (填序号)。
A.用玻璃棒搅拌
B.用热水溶解
C.用研钵将NaCl固体研碎
④下列操作中可能导致配制NaCl溶液的溶质质量分数偏小的是 (填序号)。
A.NaCl中含有少量杂质
B.量取水时仰视
C.内壁蘸有少量水的烧杯溶解NaCl
D.转移时,有少量溶液溅出
⑤若取上述溶液20g,将其稀释为5%的NaCl溶液,则需加 g水。
(2)装有等量的水的A、B、C烧杯中分别加入10g、20g、25g某固体物质,充分溶解后,现象如图2所示。
①三个烧杯中溶质质量分数最大的溶液 (填“A”“B”或“C”)。
②A、B、C中一定属于饱和溶液的是 (填“A”“B”或“C”)。
③如图3中能表示该固体溶解度曲线的是 (填“甲”或“乙”)。
26.实验室中,利用下列装置进行化学实验,请回答下列问题。
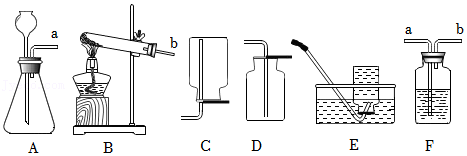
(1)实验室制取O2若采用B装置,加热仪器的名称为 ,试管中发生的化学反应方程式: ,收集装置为 (填字母编号)。
(2)实验室用 装置制取CO2,其化学反应方程式: ,收集装置通常是 (填字母编号);若用F装置收集,需要在F装置内的水面上放入少量植物油,其目的是 ,将发生装置与装置F相连时,装置F内的水将从导管 (填“a”或“b”)端排出。

(1)实验室制取O2若采用B装置,加热仪器的名称为 ,试管中发生的化学反应方程式: ,收集装置为 (填字母编号)。
(2)实验室用 装置制取CO2,其化学反应方程式: ,收集装置通常是 (填字母编号);若用F装置收集,需要在F装置内的水面上放入少量植物油,其目的是 ,将发生装置与装置F相连时,装置F内的水将从导管 (填“a”或“b”)端排出。
27.钢铁是日常生活中应用最为广泛的金属材料。
I、工业炼铁的原理是,高温下焦炭在高炉中生成的一氧化碳跟铁矿石反应生成铁。请回答下列问题:
(1)写出以赤铁矿为原料在高温下炼铁的化学方程式: ;
(2)加入焦炭,其作用除了可以生成一氧化碳外,还能 。
II、某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。所用装置如图所示。
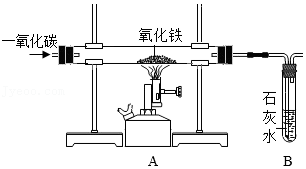
(3)如果实验成功,请回答下列问题:
①实验过程中产生的现象: 、 。
②B装置中发生反应的化学方程式 。
③该实验的操作步骤: 。
A点燃A处酒精喷灯
B.通入CO气体
C.停止通入CO气体
D.熄灭酒精喷灯
④该装置设计有一个明显缺陷,你认为是 。
实验时准确称取一定质量纯净的Fe2O3固体和相关装置的质量按上图进行实验,当固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。实验测得部分数据如下:
实验分析
查阅资料:
①Fe2O3与CO反应的固体生成物可能情况如下:
Fe2O3
Fe3O4
FeO(黑色)
Fe
②铁的氧化物在足量的稀盐酸中均能全部溶解;③石灰水只能吸收部分CO2
(4)实验结论:根据可靠实验数据计算得出反应后的黑色固体成分: ;此时玻璃管中发生的化学反应方程式: 。
(5)分析推断:①装置B试管中增加的质量一定会小于理论产生的CO2质量,可能原因是 。
A.未参加反应的CO通过B时带走了水蒸气
B.石灰水浓度小没有将二氧化碳完全吸收
C.石灰水吸收了空气中的二氧化碳气体
I、工业炼铁的原理是,高温下焦炭在高炉中生成的一氧化碳跟铁矿石反应生成铁。请回答下列问题:
(1)写出以赤铁矿为原料在高温下炼铁的化学方程式: ;
(2)加入焦炭,其作用除了可以生成一氧化碳外,还能 。
II、某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。所用装置如图所示。

(3)如果实验成功,请回答下列问题:
①实验过程中产生的现象: 、 。
②B装置中发生反应的化学方程式 。
③该实验的操作步骤: 。
A点燃A处酒精喷灯
B.通入CO气体
C.停止通入CO气体
D.熄灭酒精喷灯
④该装置设计有一个明显缺陷,你认为是 。
实验时准确称取一定质量纯净的Fe2O3固体和相关装置的质量按上图进行实验,当固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。实验测得部分数据如下:
| 玻璃管中固体的质量 | 装置B试管及其中物质的总质量 | |
| 反应前 | 32g | 300g |
| 反应后 | 28.8g | 308g |
实验分析
查阅资料:
①Fe2O3与CO反应的固体生成物可能情况如下:
Fe2O3
400℃−500℃ |
500℃−600℃ |
700℃−800℃ |
②铁的氧化物在足量的稀盐酸中均能全部溶解;③石灰水只能吸收部分CO2
(4)实验结论:根据可靠实验数据计算得出反应后的黑色固体成分: ;此时玻璃管中发生的化学反应方程式: 。
(5)分析推断:①装置B试管中增加的质量一定会小于理论产生的CO2质量,可能原因是 。
A.未参加反应的CO通过B时带走了水蒸气
B.石灰水浓度小没有将二氧化碳完全吸收
C.石灰水吸收了空气中的二氧化碳气体
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解