下载高清试卷
【2021-2022学年辽宁省沈阳市和平区九年级(上)期末化学试卷】-第1页
试卷格式:2021-2022学年辽宁省沈阳市和平区九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2021年、辽宁试卷、沈阳市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷

扫码查看解析
试卷题目
1.下列变化属于化学变化的是( )
- A. 甘蔗榨汁
- B. 自行车胎爆裂
- C. 滴水成冰
- D. 鲜奶制成酸奶
2.地壳中含量最多的金属元素是( )
- A. Al
- B. Si
- C. Fe
- D. O
3.规范操作是实验顺利进行和人身安全的保证,下列操作正确的是( )
- A.
 点燃酒精灯
点燃酒精灯 - B.
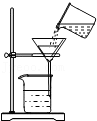 过滤
过滤 - C.
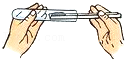 向试管里加粉末
向试管里加粉末 - D.
 量取液体
量取液体
4.习近平总书记在党的十九大报告中指出到本世纪中叶,要把我国建成富强民主文明和谐美丽的社会主义现代化强国。下列做法与“美丽”不相符的是( )
- A. 垃圾分类回收
- B. 随意丢弃废旧电池
- C. 开发利用清洁能源
- D. 燃料脱硫以减少酸雨的产生
5.普通玻璃是混合物,其成分有二氧化硅(SiO2)、硅酸钠(Na2SiO3)、硅酸钙(CaSiO3),其中硅元素的化合价均为( )
- A. ﹣2
- B. +2
- C. +3
- D. +4
6.物质的性质决定用途,用途体现物质的性质,下列有关物质的性质和用途叙述不正确的是( )
- A. 氮气在常温常压下化学性质稳定,可用做保护气
- B. 氧气能支持可燃物燃烧,可用作燃料
- C. 金属钨的熔点高,可用于制作灯泡的钨丝
- D. 金刚石硬度最大,可用于刻划玻璃
7.如图所示,这四位同学描述的是同一化学式,此化学式是( )


- A. HClO
- B. O3
- C. NO2
- D. HCl
8.下列关于“燃烧和灭火”的叙述正确的是( )
- A. 煤炉生火时,用木材引燃是为了提高煤的着火点
- B. 档案室着火用水基型灭火器(泡沫灭火器)灭火
- C. 把煤做成蜂窝煤是增大煤与空气的接触面积,使煤燃烧更充分
- D. 炒菜时油锅着火,立即向油锅内浇水
9.2015年10月,中国女科学家屠呦呦因发现了青蒿素(C11H22O5)而获得诺贝尔生理学或医学奖。下列有关青蒿素的说法错误的是( )
- A. 青蒿素由碳、氢、氧三种元素组成
- B. 一个青蒿素分子由11个碳原子、22个氢原子和5个氧原子构成的
- C. 青蒿素中碳、氢、氧元素的质量比为11:22:5
- D. 青蒿素中氢元素的质量分数最小
10.可以一次鉴别出空气、氧气和二氧化碳等三瓶气体的正确方法( )
- A. 观察气体颜色
- B. 将燃着的木条分别伸入瓶中
- C. 闻气体的气味
- D. 将带火星的木条分别伸入瓶中
11.下列客观事实的微观解释正确的是( )
| 选项 | 客观事实 | 微观解释 |
| A | 墙内开花墙外香 | 分子间有空隙 |
| B | 600L氧气加压装入容积为4L的钢瓶中 | 分子在不断运动 |
| C | 用水银温度计测量体温时,汞柱会上升 | 汞原子的大小随温度的升高而增大 |
| D | O2和CO2的化学性质不同,如O2可供呼吸,CO2不能供呼吸 | 分子的构成不同 |
- A. A
- B. B
- C. C
- D. D
12.在一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示,下列说法中错误的是( )
| W | X | Y | Z | |
| 反应前质量/g | 2 | 22 | 34 | 0 |
| 反应后质量/g | 2 | 40 | 待测 | 16 |
- A. W在反应前后质量没有改变
- B. 该反应中Y全部参加反应
- C. 该反应属于分解反应
- D. 该反应中生成X的质量为40g
13.如图是测定空气中氧气含量的实验装置。下列说法正确的是( )
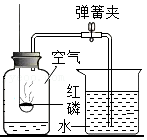

- A. 此实验不是制取气体,所以实验前不用检查装置的气密性
- B. 实验前没有将弹簧夹夹紧,会导致测定结果偏高
- C. 该实验可以说明空气中含有稀有气体
- D. 若把红磷换成木炭,也可得到相同实验结果
14.建立宏观、微观和符号之间的联系是化学学科的特点。
(1)请用化学用语和相应数字填空:
①氖元素: ;两个氢氧根离子 ;天然气的主要成分 。
②用“ ”表示一个氢原子,则:“
”表示一个氢原子,则:“ ”表示 ;“
”表示 ;“ ”表示 。
”表示 。
(2)锂电池开启了现代移动智能生活:
①锂相对原子质量为 。
②锂原子在化学反应中易 (填“得”或“失”)电子形成离子,其离子符号为 。
③在化学学习中有一个重要的观点是结构决定性质,对于(主族元素的)原子来说,也就是最外层电子数相同,则化学性质相似。据此,结合你自己的认知,请在下列元素的单质中找出与金属锂性质最接近的是 (填字母)。
A.H2
B.N2
C.Na
D.Mg
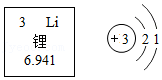
(3)在一定条件下,根据某化学反应画出如图2的某容器内微观变化图:
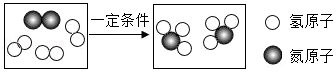
①写出“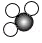 ”所表示的物质中氮元素与氢元素的质量比: 。
”所表示的物质中氮元素与氢元素的质量比: 。
②写出上述反应的化学方程式: 。
(1)请用化学用语和相应数字填空:
①氖元素: ;两个氢氧根离子 ;天然气的主要成分 。
②用“
 ”表示一个氢原子,则:“
”表示一个氢原子,则:“ ”表示 ;“
”表示 ;“ ”表示 。
”表示 。(2)锂电池开启了现代移动智能生活:
①锂相对原子质量为 。
②锂原子在化学反应中易 (填“得”或“失”)电子形成离子,其离子符号为 。
③在化学学习中有一个重要的观点是结构决定性质,对于(主族元素的)原子来说,也就是最外层电子数相同,则化学性质相似。据此,结合你自己的认知,请在下列元素的单质中找出与金属锂性质最接近的是 (填字母)。
A.H2
B.N2
C.Na
D.Mg
(3)在一定条件下,根据某化学反应画出如图2的某容器内微观变化图:

①写出“
 ”所表示的物质中氮元素与氢元素的质量比: 。
”所表示的物质中氮元素与氢元素的质量比: 。②写出上述反应的化学方程式: 。

15.多角度认识物质能帮助我们更全面地了解物质世界。以金属为例回答下列问题:
(1)认识金属元素的存在
①在自然界中,大多数金属以化合物形式存在,而金、铂等极少数金属因为化学性质不活泼,能以单质形式存在。其主要原因是他们的单质在常温下或加热条件下不能与自然界中的 (填化学式)反应。
②常见铁矿石有:黄铁矿(主要成分FeS2)、赤铁矿(主要成分Fe2O3)、磁铁矿(主要成分Fe3O4)等。这几种铁矿石的主要成分含铁元素质量分数较大的是 (填化学式)。
(2)认识金属的性质:用粗木棍在涂有蜡的锌板上写“和”、“平”两个字,露出下面的锌板。向“和”字上滴加稀盐酸,向“平”字上滴加CuSO4溶液。
①“和”字上的现象是 。
②“平”字上有红色物质析出,用化学方程式解释: 。
(3)认识金属的制备:工业上,金属银可由其氧化物(Ag2O)在高温下发生分解反应制得,反应化学方程式为 ,其中化合价升高的元素是 。
(4)认识金属的用途:烤制食物时常用到铝箔,高档装饰时用到金箔,主要利用了金属特性中的 (填物理性质)。
(1)认识金属元素的存在
①在自然界中,大多数金属以化合物形式存在,而金、铂等极少数金属因为化学性质不活泼,能以单质形式存在。其主要原因是他们的单质在常温下或加热条件下不能与自然界中的 (填化学式)反应。
②常见铁矿石有:黄铁矿(主要成分FeS2)、赤铁矿(主要成分Fe2O3)、磁铁矿(主要成分Fe3O4)等。这几种铁矿石的主要成分含铁元素质量分数较大的是 (填化学式)。
(2)认识金属的性质:用粗木棍在涂有蜡的锌板上写“和”、“平”两个字,露出下面的锌板。向“和”字上滴加稀盐酸,向“平”字上滴加CuSO4溶液。
①“和”字上的现象是 。
②“平”字上有红色物质析出,用化学方程式解释: 。
(3)认识金属的制备:工业上,金属银可由其氧化物(Ag2O)在高温下发生分解反应制得,反应化学方程式为 ,其中化合价升高的元素是 。
(4)认识金属的用途:烤制食物时常用到铝箔,高档装饰时用到金箔,主要利用了金属特性中的 (填物理性质)。
16.水是一种重要的资源,爱护水资源,人人有责。
(1)如图1所示,电解水的实验中,通电一段时间后,试管d中收集到的气体是 ;通过实验可以得出水是由 组成的。
(2)某学校饮水处可以将自来水净化为饮用水其中处理步骤如图2所示:其中活性炭对应的作用是 。
(3)日常生活中,常用 区分硬水和软水,实现硬水软化的简单方法是 。
(4)2018年世界环境日的主题是“美丽中国,我是行动者”。为打好污染防治攻坚战,我们采取了一系列应对措施,请写出防治水体污染的一条措施: 。
(1)如图1所示,电解水的实验中,通电一段时间后,试管d中收集到的气体是 ;通过实验可以得出水是由 组成的。
(2)某学校饮水处可以将自来水净化为饮用水其中处理步骤如图2所示:其中活性炭对应的作用是 。
(3)日常生活中,常用 区分硬水和软水,实现硬水软化的简单方法是 。
(4)2018年世界环境日的主题是“美丽中国,我是行动者”。为打好污染防治攻坚战,我们采取了一系列应对措施,请写出防治水体污染的一条措施: 。
17.实验是学习与研究化学的一种重要方式。

(1)用如图一装置进行实验,挤出浓氨水。
①实验现象是 。
②该实验说明微粒具有的性质是 。
(2)如图二为粉尘爆炸的实验装置。用空气吹散烘干的面粉,瞬间 发生爆炸,硬纸板盖被冲飞,蜡烛熄灭。
①吹散面粉的目的是 。
②储存面粉、汽油等易燃物或易爆物时,应注意 。

(1)用如图一装置进行实验,挤出浓氨水。
①实验现象是 。
②该实验说明微粒具有的性质是 。
(2)如图二为粉尘爆炸的实验装置。用空气吹散烘干的面粉,瞬间 发生爆炸,硬纸板盖被冲飞,蜡烛熄灭。
①吹散面粉的目的是 。
②储存面粉、汽油等易燃物或易爆物时,应注意 。
18.化学是一门以实验为基础的科学。请结合图1所示回答问题:
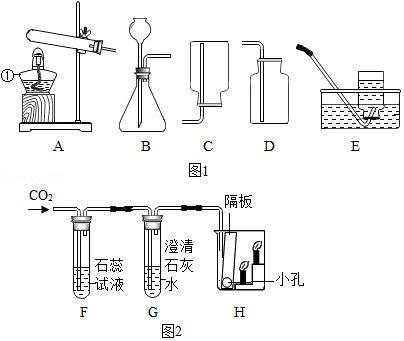
(1)请写出标有序号的仪器名称:① 。
(2)实验室用高锰酸钾制氧气的化学反应方程式为 ,应选择的发生装置和收集装置是 (填字母)。
(3)通常情况下,硫化氢(H2S)是一种密度比空气大,能溶于水的气体,实验室可用块状固体硫化亚铁和稀盐酸反应来制取硫化氢。实验室制取H2S选择的发生和收集装置是 (填字母)。
(4)某同学设计了如图2所示装置并验证二氧化碳的性质,当通入二氧化碳一段时间后,F中的现象是 ;G中澄清石灰水变浑浊,反应的化学方程式为 ;H中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是 。

(1)请写出标有序号的仪器名称:① 。
(2)实验室用高锰酸钾制氧气的化学反应方程式为 ,应选择的发生装置和收集装置是 (填字母)。
(3)通常情况下,硫化氢(H2S)是一种密度比空气大,能溶于水的气体,实验室可用块状固体硫化亚铁和稀盐酸反应来制取硫化氢。实验室制取H2S选择的发生和收集装置是 (填字母)。
(4)某同学设计了如图2所示装置并验证二氧化碳的性质,当通入二氧化碳一段时间后,F中的现象是 ;G中澄清石灰水变浑浊,反应的化学方程式为 ;H中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是 。
19.暖贴发热是利用了铁粉生锈放出热量的原理,某小组同学设计并进行实验,探究铁生锈的条件及影响生锈速率的因素。

Ⅰ.探究铁生锈的条件
某兴趣小组对实验进行了创新设计,如图所示。取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,实验保证足够的时间。
(1)实验①②无明显现象,实验③中铁丝生锈,铁生锈实际上是铁与空气中的 发生反应的结果。
(2)当铁丝足量,时间足够长,实验③进入试管内的水的液面约上升 ,若该实验用来测定空气中氧气含量则优点是 。
Ⅱ.探究影响铁生锈速率的因素
[查阅资料]暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
[猜想假设]
①活性炭能加快铁粉生锈的速率。②食盐能加快铁粉生锈的速率。
[进行实验]下表是2g铁粉、5g 水与不同量活性炭、食盐均匀混合后,在10分钟内温度上升的实验记录。
[解释与结论]
(3)表中x的值为 。
(4)对比实验1和3,得出的结论是 。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁生锈速率”,需要对比 (填实验编号)。
[反思与评价]
(6)暖贴在使用前要注意 。

Ⅰ.探究铁生锈的条件
某兴趣小组对实验进行了创新设计,如图所示。取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,实验保证足够的时间。
(1)实验①②无明显现象,实验③中铁丝生锈,铁生锈实际上是铁与空气中的 发生反应的结果。
(2)当铁丝足量,时间足够长,实验③进入试管内的水的液面约上升 ,若该实验用来测定空气中氧气含量则优点是 。
Ⅱ.探究影响铁生锈速率的因素
[查阅资料]暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
[猜想假设]
①活性炭能加快铁粉生锈的速率。②食盐能加快铁粉生锈的速率。
[进行实验]下表是2g铁粉、5g 水与不同量活性炭、食盐均匀混合后,在10分钟内温度上升的实验记录。
| 实验编号 | 活性炭/g | 食盐/g | 温度上升值/℃ |
| 1 | 0 | 0 | 0.1 |
| 2 | 0.2 | 0 | 22.0 |
| 3 | 0 | x | 3.1 |
| 4 | 0.2 | 0.1 | 56.3 |
[解释与结论]
(3)表中x的值为 。
(4)对比实验1和3,得出的结论是 。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁生锈速率”,需要对比 (填实验编号)。
[反思与评价]
(6)暖贴在使用前要注意 。
20.我国《室内空气质量标准》(GB/T18883﹣2002)规定室内空气中甲醛(HCHO)含不得超过1.0×10﹣1mg/m3。甲醛的含量可根据下列反应测定:4KMnO4+6H2SO4+5HCHO═2K2SO4+4MnSO4+5CO2+11H2O。现将某装修后居室内空气样本750mL通入高锰酸钾和硫酸的混合溶液。样本中的甲醛完全反应消耗KMnO4的质量为6.32×10﹣4mg。
(1)该空气样本750mL中甲醛的质量为 mg。
(2)通过计算,1L该空气中甲醛的含量为 mg/L;故该居室内空气中甲醛的含量 (填“符合”或“不符合”)符合国家标准。
(1)该空气样本750mL中甲醛的质量为 mg。
(2)通过计算,1L该空气中甲醛的含量为 mg/L;故该居室内空气中甲醛的含量 (填“符合”或“不符合”)符合国家标准。
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解