下载高清试卷
【2022年江苏省盐城市东台市中考化学模拟试卷】-第6页
试卷格式:2022年江苏省盐城市东台市中考化学模拟试卷.PDF
试卷热词:最新试卷、2022年、江苏试卷、盐城市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.2022年我国环境日的主题为“共建清洁美丽世界”。下列举措不符合对应要求的是( )
- A. 水更清——防治水体污染
- B. 景更美——提高绿化覆盖
- C. 天更蓝——加强大气治理
- D. 土更净——填埋废弃电池
2.中华文化源远流长。下列工艺品的制作过程中一定发生了化学变化的是( )
- A. 烧制唐三彩
- B. 裁剪纸窗花
- C. 雕刻石狮子
- D. 编制中国结
3.阅读下列资料,完成问题:
“科技冬奥”是2022年北京冬奥的主要特色。
火炬“飞扬”中藏着两项技术首创:一是将内部燃料从天然气改为更加洁净的氢气;二是火炬外壳由碳纤维复合材料制成,不仅具有“轻、固、美”的特点,而且在1000℃的温度下不会起泡、开裂。
国家速滑馆“冰丝带”的寒道,首次在冬奥历史上采用了二氧化碳跨临界直冷制冰技术,为运动员创造更快的成绩提供了保障。
构成液氢的微粒是( )
“科技冬奥”是2022年北京冬奥的主要特色。
火炬“飞扬”中藏着两项技术首创:一是将内部燃料从天然气改为更加洁净的氢气;二是火炬外壳由碳纤维复合材料制成,不仅具有“轻、固、美”的特点,而且在1000℃的温度下不会起泡、开裂。
国家速滑馆“冰丝带”的寒道,首次在冬奥历史上采用了二氧化碳跨临界直冷制冰技术,为运动员创造更快的成绩提供了保障。
构成液氢的微粒是( )
- A. H2
- B. H
- C. H+
- D. H2O
4.阅读下列资料,完成问题:
“科技冬奥”是2022年北京冬奥的主要特色。
火炬“飞扬”中藏着两项技术首创:一是将内部燃料从天然气改为更加洁净的氢气;二是火炬外壳由碳纤维复合材料制成,不仅具有“轻、固、美”的特点,而且在1000℃的温度下不会起泡、开裂。
国家速滑馆“冰丝带”的寒道,首次在冬奥历史上采用了二氧化碳跨临界直冷制冰技术,为运动员创造更快的成绩提供了保障。
对于碳纤维复合材料的特性,下列说法不正确的是( )
“科技冬奥”是2022年北京冬奥的主要特色。
火炬“飞扬”中藏着两项技术首创:一是将内部燃料从天然气改为更加洁净的氢气;二是火炬外壳由碳纤维复合材料制成,不仅具有“轻、固、美”的特点,而且在1000℃的温度下不会起泡、开裂。
国家速滑馆“冰丝带”的寒道,首次在冬奥历史上采用了二氧化碳跨临界直冷制冰技术,为运动员创造更快的成绩提供了保障。
对于碳纤维复合材料的特性,下列说法不正确的是( )
- A. 耐高温
- B. 耐腐蚀
- C. 硬度大
- D. 密度大
5.阅读下列资料,完成问题:
“科技冬奥”是2022年北京冬奥的主要特色。
火炬“飞扬”中藏着两项技术首创:一是将内部燃料从天然气改为更加洁净的氢气;二是火炬外壳由碳纤维复合材料制成,不仅具有“轻、固、美”的特点,而且在1000℃的温度下不会起泡、开裂。
国家速滑馆“冰丝带”的寒道,首次在冬奥历史上采用了二氧化碳跨临界直冷制冰技术,为运动员创造更快的成绩提供了保障。
当物质处于超临界状态时,它同时存在液体和气体的性质。下列有关跨临界二氧化碳的说法正确的是( )
“科技冬奥”是2022年北京冬奥的主要特色。
火炬“飞扬”中藏着两项技术首创:一是将内部燃料从天然气改为更加洁净的氢气;二是火炬外壳由碳纤维复合材料制成,不仅具有“轻、固、美”的特点,而且在1000℃的温度下不会起泡、开裂。
国家速滑馆“冰丝带”的寒道,首次在冬奥历史上采用了二氧化碳跨临界直冷制冰技术,为运动员创造更快的成绩提供了保障。
当物质处于超临界状态时,它同时存在液体和气体的性质。下列有关跨临界二氧化碳的说法正确的是( )
- A. 可用作燃料
- B. 能使澄清石灰水变浑浊
- C. 分子停止运动
- D. 是一种与干冰组成不同的物质
6.下列用氧化铜制取氢氧化铜的系列操作中正确的是( )
- A.
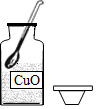
取用药品 - B.
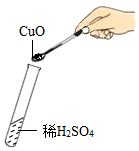
添加药品 - C.
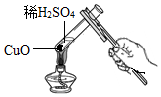
加快反应 - D.
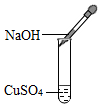
滴加碱液
7.纳米医学上可用四氯金酸(HAuCl4)制备包裹药物的外壳,四氯金酸中氯元素的化合价为-1价,则金元素的化合价为( )
- A. +2
- B. +3
- C. +4
- D. +5
8.“中国芯”的关键材料是硅。如图为元素周期表中的一格和硅原子的结构示意图,下列有关说法错误的是( )
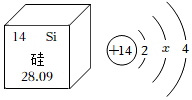

- A. 图中的x为8
- B. 硅属于非金属元素
- C. 硅的相对原子质量为14
- D. 硅元素位于元素周期表第三周期
9.为强化安全意识,提升安全素养,学校举行了消防安全知识竞赛。下列做法正确的是( )
- A. 高楼住宅发生火灾时,立即乘电梯逃生
- B. 电器在使用时着火,立即用水灭火
- C. 炒菜时油锅着火,立即盖上锅盖
- D. 室内起火,打开所有门窗通风
10.今年央视3.15晚会曝光了粉条造假乱象,用廉价木薯粉代替红薯粉,木薯中含有毒物质亚麻仁苦苷(化学式:C10H17NO6)。下列有关亚麻仁苦苷的说法正确的是( )
- A. 氢元素的质量分数最高
- B. 属于高分子化合物
- C. 完全燃烧只生成CO2和H2O
- D. 碳元素与氧元素的质量比为5:4
11.雷电交加的天空可能发生的一个化学反应,其微观过程如图。下列说法错误的是( )
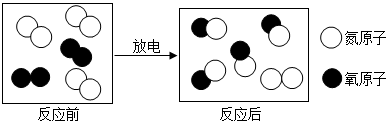

- A. 该反应属于氧化反应
- B. 该反应的生成物为两种物质
- C. 参加反应的反应物分子个数比是1:1
- D. 反应前后元素的化合价都发生了改变
12.推理是化学学习中常用的思维方法,下列推理正确的是( )
- A. 碱溶液能使酚酞溶液变红,所以能使酚酞溶液变红的溶液一定显碱性
- B. 氯化钠、硫酸铜等盐中都含有金属元素,所以盐中一定都含有金属元素
- C. 化合物是由不同种元素组成的,所以由不同种元素组成的物质一定是化合物
- D. 生理盐水、葡萄糖溶液、酒精溶液是无色透明的,所以溶液都是无色透明的
13.如图是氯化钠和硝酸钾两种固体的溶解度曲线。下列说法正确的是( )
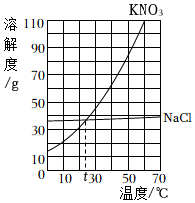

- A. 硝酸钾的溶解度大于氯化钠
- B. t℃时,两种物质溶液的溶质的质量分数一定相等
- C. 若硝酸钾中含有少量氯化钠,提纯方法为蒸发结晶
- D. 60℃时,将50g质量分数为20%的硝酸钾溶液变为饱和溶液,需要加入硝酸钾的质量为34g
14.下列实验方案能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去CO中的CO2 | 将气体通过灼热的CuO |
| B | 除去铁粉中的铜粉 | 加入足量稀硫酸充分反应后,过滤、洗涤、干燥 |
| C | 鉴别CaCO3、NaOH、NH4NO3固体 | 分别取样加入适量的水,搅拌,观察现象 |
| D | 除去KCl溶液中的少量的K2CO3 | 向溶液中滴加过量的BaCl2溶液,过滤 |
- A. A
- B. B
- C. C
- D. D
15.现有Fe2O3和CuO的混合物ag,在高温条件下用足量的CO还原,充分反应后,得到金属混合物2.2g,产生的CO2气体用足量的澄清石灰水全部吸收后,产生白色沉淀5.0g,则a的数值为( )
- A. 2.7
- B. 3.0
- C. 3.1
- D. 3.8
16.化学帮助我们认识身边的物质。
现有:①钛合金②活性炭③碳酸氢钠④氦气,选择适当的物质填空(填序号)。
(1)可用于制造人造骨的是 ;
(2)可用于焙制糕点的是 ;
(3)可用作冰箱除味剂的是 ;
(4)可用于制造电光源的是 。
现有:①钛合金②活性炭③碳酸氢钠④氦气,选择适当的物质填空(填序号)。
(1)可用于制造人造骨的是 ;
(2)可用于焙制糕点的是 ;
(3)可用作冰箱除味剂的是 ;
(4)可用于制造电光源的是 。
17.化学与生活息息相关。
(1)家庭使用的液化石油气能被压缩到钢瓶中,从微观角度说明原因是 ;
(2)老年人应从食物中摄入适量的 (填名称)元素,以防止骨质疏松;
(3)中国将采取更加有力的措施,争取2060年前完全实现碳中和。一种转化CO2的过程如下:二氧化碳与氢气在一定条件下生成甲醇(CH3OH)和水。该转化过程中发生反应的化学方程式为 。
(1)家庭使用的液化石油气能被压缩到钢瓶中,从微观角度说明原因是 ;
(2)老年人应从食物中摄入适量的 (填名称)元素,以防止骨质疏松;
(3)中国将采取更加有力的措施,争取2060年前完全实现碳中和。一种转化CO2的过程如下:二氧化碳与氢气在一定条件下生成甲醇(CH3OH)和水。该转化过程中发生反应的化学方程式为 。
18.如图1是中学化学实验中常用的一些装置。
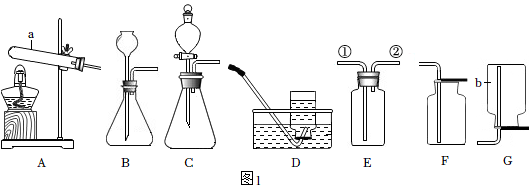
(1)写出图中仪器a的名称 。
(2)实验室用高锰酸钾制取并收集一瓶较纯净的氧气所需的装置为 (填字母序号),此反应的化学方程式为 ,实验室常用 检验该气体。
(3)B、C装置均可作为实验室制取CO2的发生装置,与B相比,选用C装置的优点是 ,若要收集一瓶干燥的CO2,还需要使用装置E,则E中可盛放的物质为 。
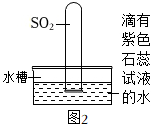
(4)通常状况下,二氧化硫气体的密度比空气大,易溶于水,能与水反应生成亚硫酸(H2SO3)。实验室常用亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取二氧化硫。
①实验室制取SO2的发生装置可用 (填字母序号),若用装置E收集SO2,气体从 (填①或②)端进入。
②如图2所示,把充满SO2的试管倒立在滴有紫色石蕊的水中,可看到的现象是 。

(1)写出图中仪器a的名称 。
(2)实验室用高锰酸钾制取并收集一瓶较纯净的氧气所需的装置为 (填字母序号),此反应的化学方程式为 ,实验室常用 检验该气体。
(3)B、C装置均可作为实验室制取CO2的发生装置,与B相比,选用C装置的优点是 ,若要收集一瓶干燥的CO2,还需要使用装置E,则E中可盛放的物质为 。
(4)通常状况下,二氧化硫气体的密度比空气大,易溶于水,能与水反应生成亚硫酸(H2SO3)。实验室常用亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取二氧化硫。
①实验室制取SO2的发生装置可用 (填字母序号),若用装置E收集SO2,气体从 (填①或②)端进入。
②如图2所示,把充满SO2的试管倒立在滴有紫色石蕊的水中,可看到的现象是 。

19.自然界并不缺少“镁”,而是缺少发现“镁”的眼睛。某化学兴趣小组开启寻“镁”之旅。
第一站:初步认识镁
镁是一种色的固体,质软,有导电性。
(1)将2根打磨光亮的镁条分别放入等质量、等质量分数的稀盐酸和稀硫酸中,充分反应后镁条有剩余,产生氢气的质量 。
A.相等 B.与稀盐酸反应放出的氢气多
C.无法判断 D.与稀硫酸反应放出的氢气多
第二站:制备金属镁

(2)为了使镁离子沉淀下来,充分利用当地的贝壳(主要成分为CaCO3)资源获得试剂①,其化学式为 。
(3)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)。
A.蒸馏
B.吸附
C.结晶
D.过滤
(4)向MgCl2溶液中加入肥皂水,可能观察的现象是 。
(5)电解无水MgCl2的反应属于 (填基本反应类型)。
第三站:再探金属镁
【提出问题】镁与水是否发生反应?反应后的生成物是什么?
【查阅资料】70℃时Mg(OH)2在水中的溶解度很小,但溶于水的部分可以完全解离出Mg2+和OH-。
【实验步骤】
(6)将打磨光亮的镁条放入盛有70℃水的试管中(如图2),发现镁条表面有气泡产生。将收集的气体点燃,产生淡蓝色火焰,证明该气体为 。
(7)向反应后的溶液中立即滴入2滴无色酚酞溶液,观察到镁条附近溶液 ,证明溶液中生成OH-。
【交流讨论】
(8)根据上述实验,写出镁与热水反应的化学方程式 。
【拓展探究】
同学们又探究温度对镁与水反应速率的影响,实验数据记录如下:
(9)根据表中数据,分析温度对镁与水反应速率的影响: 。
(10)一段时间后,同学们观察到镁条表面不再有气泡产生,镁条表面失去光泽。但将表面失去光泽的镁条打磨后再次放入热水中,发现又有气泡产生,说明镁与水反应变缓慢直至停止的可能原因是 。
第一站:初步认识镁
镁是一种色的固体,质软,有导电性。
(1)将2根打磨光亮的镁条分别放入等质量、等质量分数的稀盐酸和稀硫酸中,充分反应后镁条有剩余,产生氢气的质量 。
A.相等 B.与稀盐酸反应放出的氢气多
C.无法判断 D.与稀硫酸反应放出的氢气多
第二站:制备金属镁

(2)为了使镁离子沉淀下来,充分利用当地的贝壳(主要成分为CaCO3)资源获得试剂①,其化学式为 。
(3)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)。
A.蒸馏
B.吸附
C.结晶
D.过滤
(4)向MgCl2溶液中加入肥皂水,可能观察的现象是 。
(5)电解无水MgCl2的反应属于 (填基本反应类型)。
第三站:再探金属镁
【提出问题】镁与水是否发生反应?反应后的生成物是什么?
【查阅资料】70℃时Mg(OH)2在水中的溶解度很小,但溶于水的部分可以完全解离出Mg2+和OH-。
【实验步骤】
(6)将打磨光亮的镁条放入盛有70℃水的试管中(如图2),发现镁条表面有气泡产生。将收集的气体点燃,产生淡蓝色火焰,证明该气体为 。
(7)向反应后的溶液中立即滴入2滴无色酚酞溶液,观察到镁条附近溶液 ,证明溶液中生成OH-。
【交流讨论】
(8)根据上述实验,写出镁与热水反应的化学方程式 。
【拓展探究】
同学们又探究温度对镁与水反应速率的影响,实验数据记录如下:
| 反应温度(℃) | 50 | 55 | 60 | 65 | 70 |
| 收集50mL气体所用时间(s) | 295 | 257 | 196 | 124 | 74 |
(9)根据表中数据,分析温度对镁与水反应速率的影响: 。
(10)一段时间后,同学们观察到镁条表面不再有气泡产生,镁条表面失去光泽。但将表面失去光泽的镁条打磨后再次放入热水中,发现又有气泡产生,说明镁与水反应变缓慢直至停止的可能原因是 。
20.实验室有一包NaCl样品,可能混有的杂质为NaOH、Na2CO3中的一种或两种。化学兴趣小组为确定样品的成分,进行以下实验。
(1)【探究一】测量样品溶液的pH。
取少量样品溶于水,测得溶液的pH大于7。小组同学对样品的成分进行猜想,猜想一:含有 ;猜想二:含有NaCl和NaOH;猜想三:含有NaCl、NaOH和Na2CO3。
(2)【探究二】测量样品与硫酸反应生成气体的体积。
如图1所示,取3.00g样品与足量稀硫酸混合,充分反应后,测得生成气体的体积为220mL(该条件下气体的密度为2.00g/L;装置气密性良好且忽略气体的溶解)。集气瓶上方加入一层植物油的目的是 。
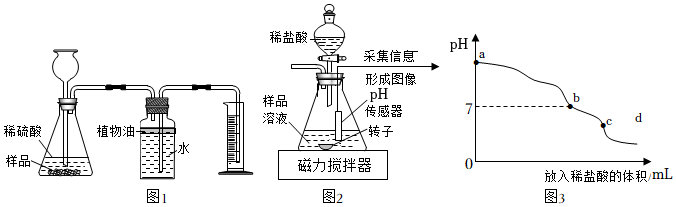
【探究三】测量样品与盐酸反应后氯化钠的质量。
如图2所示,另取3.00g样品置入锥形瓶中,加适量水溶解。逐滴加入过量的稀盐酸,用pH传感器等电子设备采集信息形成图像如图3。将锥形瓶中最终所得溶液蒸发、结晶得到全部固体,其质量为3.48g。
(3)c点溶液呈 (填“酸性”、“碱性”或“中性”)。
(4)ab段溶液pH降低,可能发生反应的化学方程式为 (写一个即可)。
(5)蒸发时除使用蒸发皿、铁架台(带铁圈)外,还需要用到的仪器有 。
(6)【实验结论】关于样品的成分,猜想 (填“一”、“二”或“三”)是正确的。
(7)【定量计算】结合探究二、三,计算样品中氯化钠的质量分数(精确到0.1%)。
(8)【交流反思】下列因素会导致所测样品中氯化钠的质量分数偏小的是 (填序号)。
A.探究二中俯视读取量筒中水的体积
B.探究二实验后生成气体在锥形瓶中仍有滞留
C.探究三中加入的稀盐酸量不足
D.探究三中蒸发时有液体溅出
(1)【探究一】测量样品溶液的pH。
取少量样品溶于水,测得溶液的pH大于7。小组同学对样品的成分进行猜想,猜想一:含有 ;猜想二:含有NaCl和NaOH;猜想三:含有NaCl、NaOH和Na2CO3。
(2)【探究二】测量样品与硫酸反应生成气体的体积。
如图1所示,取3.00g样品与足量稀硫酸混合,充分反应后,测得生成气体的体积为220mL(该条件下气体的密度为2.00g/L;装置气密性良好且忽略气体的溶解)。集气瓶上方加入一层植物油的目的是 。

【探究三】测量样品与盐酸反应后氯化钠的质量。
如图2所示,另取3.00g样品置入锥形瓶中,加适量水溶解。逐滴加入过量的稀盐酸,用pH传感器等电子设备采集信息形成图像如图3。将锥形瓶中最终所得溶液蒸发、结晶得到全部固体,其质量为3.48g。
(3)c点溶液呈 (填“酸性”、“碱性”或“中性”)。
(4)ab段溶液pH降低,可能发生反应的化学方程式为 (写一个即可)。
(5)蒸发时除使用蒸发皿、铁架台(带铁圈)外,还需要用到的仪器有 。
(6)【实验结论】关于样品的成分,猜想 (填“一”、“二”或“三”)是正确的。
(7)【定量计算】结合探究二、三,计算样品中氯化钠的质量分数(精确到0.1%)。
(8)【交流反思】下列因素会导致所测样品中氯化钠的质量分数偏小的是 (填序号)。
A.探究二中俯视读取量筒中水的体积
B.探究二实验后生成气体在锥形瓶中仍有滞留
C.探究三中加入的稀盐酸量不足
D.探究三中蒸发时有液体溅出
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解