下载高清试卷
【2020年重庆市中考化学试卷(B卷)】-第1页
试卷格式:2020年重庆市中考化学试卷(B卷).PDF
试卷热词:最新试卷、2020年、重庆试卷、化学试卷、九年级试卷、中考试卷、初中试卷

扫码查看解析
试卷题目
1.2020年世界环境日的主题是“关爱自然,刻不容缓”。下列做法不符合这一主题的是( )
- A. 植树造林
- B. 保护野生动物
- C. 合理使用化肥
- D. 大力开采地下水
2.空气中能供人呼吸的气体是( )
- A. N2
- B. O2
- C. CO2
- D. Ne
3.下列变化中,发生了化学变化的是( )
- A. 海水蒸发
- B. 矿石粉碎
- C. 路面结冰
- D. 钢铁锈蚀
4.小麦、大米、玉米都是酿造啤酒的原料,这些原料中都富含的营养素是( )
- A. 糖类
- B. 蛋白质
- C. 维生素
- D. 油脂
5.下列饮料中,不属于溶液的是( )
- A. 汽水
- B. 白酒
- C. 酸奶
- D. 苏打水
6.甲状腺肿大的患者,特别要注意合理食用的食物是( )
- A. 加碘食盐
- B. 富硒鸡蛋
- C. 葡萄糖酸锌口服液
- D. 高铁酱油
7.下列物质属于纯净物的是( )
- A. 钛合金
- B. 大理石
- C. 蒸馏水
- D. 煤
8.下列粒子中,不能直接构成物质的是( )
- A. 原子
- B. 分子
- C. 离子
- D. 中子
9.下列肥料中,能与尿素[CO(NH2)2]加工配制成复合肥料的是( )
- A. (NH4)2SO4
- B. KCl
- C. NH3•H2O
- D. NH4Cl
10.下列实验中玻璃棒不是用来搅拌的是( )
- A. 稀释浓硫酸
- B. 测定溶液pH
- C. 蒸发食盐水
- D. 溶解蔗糖
11.通过学习化学,我们学会了从化学的视角认识水,下列对水的认识错误的是( )
- A. 水由氢气和氧气组成
- B. 冰中的水分子也在不断运动
- C. 硬水中含有较多可溶性钙、镁化合物
- D. 水可与生石灰发生化学反应
12.下列说法正确的是( )
- A. 石油是可再生能源
- B. 高炉炼铁炼出的是纯铁
- C. 医用口罩过滤层使用了有机合成材料
- D. 易拉罐和矿泉水瓶属于不可回收垃圾
13.如图所示,水中的白磷能否燃烧与鼓入的气体和水温有关,表中能使白磷燃烧的选项是( )

| 选项 | 气体X | 水温/℃ |
| A | 氧气 | 5 |
| B | 氮气 | 40 |
| C | 二氧化碳 | 80 |
| D | 空气 | 80 |

- A. A
- B. B
- C. C
- D. D
14.碳及其部分化合物的转化关系如图所示,其中X、Y表示转化中的另一种反应物。下列说法错误的是( )


- A. X可以是单质或氧化物
- B. 反应①中CO一定发生了氧化反应
- C. Y可以是CaCl2溶液
- D. 打开碳酸饮料瓶盖时会发生反应②
15.雷电交加的天空发生的一个化学反应,其微观过程可用如图模型图表示,下列说法错误的是( )
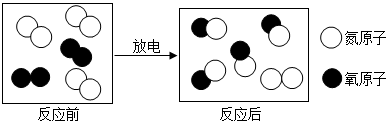

- A. 反应前后原子、分子的数目都没有改变
- B. 反应前后各元素的化合价都发生了改变
- C. 该反应是化合反应
- D. 参加反应的各物质与生成物之间分子个数比为1:1:1
16.一定温度下,向ag FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如图所示。下列叙述错误的是( )


- A. Fe(OH)3沉淀完全时消耗NaOH的质量为ng
- B. P点对应的溶液中NaOH达到饱和状态
- C. m=c﹣a
- D. 生成Fe(OH)3的质量为(n﹣b+a)g
17.用化学用语填空。
(1)2个镁原子 ,2个氢分子 。
(2)天然气的主要成分是 。
(3)碳原子的结构示意图 。
(1)2个镁原子 ,2个氢分子 。
(2)天然气的主要成分是 。
(3)碳原子的结构示意图 。
18.2020年,罕见的新冠病毒疫情爆发,各种消毒剂如酒精、二氧化氯、过氧乙酸等被广泛使用,根据所学知识回答下列问题。
(1)使用酒精消毒时,要注意安全,避免失火,酒精(C2H5OH)在空气中完全燃烧的化学方程式为 。
(2)二氧化氯(ClO2)具有强氧化性,可发生反应:6ClO2+16NH3═5R+6NH4Cl+12H2O,则R的化学式为 。
(3)过氧乙酸(CH3COOOH)中碳元素与氢元素的质量比为 。过氧乙酸溶液中通常还含有过氧化氢、醋酸等物质,向过氧乙酸溶液中加入下列物质,不能产生气体的是 。
A.CuSO4 B.NaCl C.Na2CO3 D.MnO2
(1)使用酒精消毒时,要注意安全,避免失火,酒精(C2H5OH)在空气中完全燃烧的化学方程式为 。
(2)二氧化氯(ClO2)具有强氧化性,可发生反应:6ClO2+16NH3═5R+6NH4Cl+12H2O,则R的化学式为 。
(3)过氧乙酸(CH3COOOH)中碳元素与氢元素的质量比为 。过氧乙酸溶液中通常还含有过氧化氢、醋酸等物质,向过氧乙酸溶液中加入下列物质,不能产生气体的是 。
A.CuSO4 B.NaCl C.Na2CO3 D.MnO2
19.氯化钠、碳酸钠、硝酸钾在不同温度时的溶解度如下表所示,某同学根据表中数据作出了其中一种物质的溶解度曲线(如图所示),请根据表和图中信息填空。
(1)曲线M是表中 的溶解度曲线,该物质在5℃时的溶解度约为 g。
(2)如果将表中三种物质的溶解度曲线全部画出,在0℃~40℃范围内会有 个两线交点。
(3)10℃时,将15g氯化钠和15g硝酸钾固体同时加入盛有50g水的烧杯中,充分搅拌、溶解、静置后,烧杯底部剩余的固体是 。

| 温度/℃溶解度/g物质 | 0 | 10 | 20 | 30 | 40 |
| 氯化钠 | 35.7 | 35.8 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 16 | 18 | 36.5 | 50 |
| 硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
(1)曲线M是表中 的溶解度曲线,该物质在5℃时的溶解度约为 g。
(2)如果将表中三种物质的溶解度曲线全部画出,在0℃~40℃范围内会有 个两线交点。
(3)10℃时,将15g氯化钠和15g硝酸钾固体同时加入盛有50g水的烧杯中,充分搅拌、溶解、静置后,烧杯底部剩余的固体是 。

20.纽扣电池是生活中常用的电源,如图是银锌纽扣电池的构造示意图,回答下列问题。
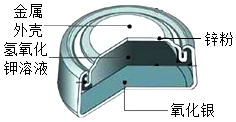
(1)纽扣电池的外壳可以加工得很薄,说明金属具有 性。
(2)氧化银加热分解可以得到两种单质,其化学反应方程式为 。
(3)该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是 ,为了验证该结论,某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论证据的是 (填序号)。
A.银表面没有气泡生成
B.铁表面最终生成气体的总量比锌多
C.铁表面产生气泡的速率比锌慢

(1)纽扣电池的外壳可以加工得很薄,说明金属具有 性。
(2)氧化银加热分解可以得到两种单质,其化学反应方程式为 。
(3)该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是 ,为了验证该结论,某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论证据的是 (填序号)。
A.银表面没有气泡生成
B.铁表面最终生成气体的总量比锌多
C.铁表面产生气泡的速率比锌慢
21.孔雀石的主要成分是CuCO3•Cu(OH)2及少量不溶性杂质(杂质不与酸反应),某同学按下列实验步骤制取了少量氧化铜。

(1)白色沉淀的化学式为 。
(2)写出步骤③中发生反应的化学方程式 ; 。
(3)蓝色沉淀受热分解生成另一种氧化物的化学式是 。
(4)若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达 种。

(1)白色沉淀的化学式为 。
(2)写出步骤③中发生反应的化学方程式 ; 。
(3)蓝色沉淀受热分解生成另一种氧化物的化学式是 。
(4)若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达 种。
22.化学实验中,常常要涉及到仪器和装置的连接。
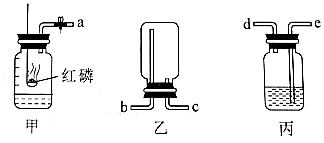
(1)甲、乙、丙装置中都用到了导管、橡皮塞和 。
(2)利用红磷燃烧测定空气中氧气的含量,应将甲中导管a端与丙中导管 端相连接(填字母,下同)。
(3)如果实验室用乙装置收集二氧化碳,空气应从导管的 端排出。丙装置正在用排水法收集氧气,氧气是从导管 端进入,如果用丙装置干燥氧气,容器中的液体是 (填名称)。

(1)甲、乙、丙装置中都用到了导管、橡皮塞和 。
(2)利用红磷燃烧测定空气中氧气的含量,应将甲中导管a端与丙中导管 端相连接(填字母,下同)。
(3)如果实验室用乙装置收集二氧化碳,空气应从导管的 端排出。丙装置正在用排水法收集氧气,氧气是从导管 端进入,如果用丙装置干燥氧气,容器中的液体是 (填名称)。
23.化学规律建立在实验基础之上,质量守恒定律可以用许多化学实验加以验证。

(1)小东同学按照课本上的实验进行验证(如图1所示)。一段时间后,可以观察到铁钉表面出现 ,其反应的化学反应方程式为 ,反应前后天平读数不变,但溶液颜色变化不明显。
(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
【实验分析】从以上现象分析,两个设想都不合适,其中按设想 (填“一”或“二”)进行的实验能够验证质量守恒定律。
实验1中溶液颜色几乎不变的原因可能是 (填序号)。
A.铁与饱和硫酸铜溶液不反应
B.铁表面形成了一层氧化膜,阻止了反应的进一步进行
C.生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D.水也参与了该反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸铜溶液呈酸性,所以总质量减小的原因可能是 。
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水,将实验2中的烧杯换成如图2所示装置,均能达到实验目的,但该装置中缺少一种物品,请你在装置图中画出。

(1)小东同学按照课本上的实验进行验证(如图1所示)。一段时间后,可以观察到铁钉表面出现 ,其反应的化学反应方程式为 ,反应前后天平读数不变,但溶液颜色变化不明显。
(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
| 实验内容 | 实验现象 | |
| 实验1 | 烧杯中换成饱和硫酸铜溶液 | ①1小时后溶液颜色几乎不变②天平读数不变③铁钉表面有变化 |
| 实验2 | 铁钉换成锌粒 | ①溶液颜色明显变浅②天平读数减小③锌粒表面有变化 |
【实验分析】从以上现象分析,两个设想都不合适,其中按设想 (填“一”或“二”)进行的实验能够验证质量守恒定律。
实验1中溶液颜色几乎不变的原因可能是 (填序号)。
A.铁与饱和硫酸铜溶液不反应
B.铁表面形成了一层氧化膜,阻止了反应的进一步进行
C.生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D.水也参与了该反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸铜溶液呈酸性,所以总质量减小的原因可能是 。
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水,将实验2中的烧杯换成如图2所示装置,均能达到实验目的,但该装置中缺少一种物品,请你在装置图中画出。
24.84消毒液的有效成分是次氯酸钠(NaClO),次氯酸钠工业制法的反应原理是:Cl2+2NaOH═NaClO+NaCl+H2O.某同学将Cl2通入185.8g NaOH溶液中(NaOH过量),充分反应后得到混合溶液200g。计算:(计算结果精确到0.1%)
(1)参加反应的氯气质量是 g。
(2)混合溶液中次氯酸钠的质量分数。
(3)84消毒液中起消毒作用的是次氯酸钠中的氯元素。已知某品牌84消毒液中起消毒作用的氯元素质量分数为6%,计算该84消毒液中次氯酸钠的质量分数。
(1)参加反应的氯气质量是 g。
(2)混合溶液中次氯酸钠的质量分数。
(3)84消毒液中起消毒作用的是次氯酸钠中的氯元素。已知某品牌84消毒液中起消毒作用的氯元素质量分数为6%,计算该84消毒液中次氯酸钠的质量分数。
查看全部题目