下载高清试卷
【2020年广东省深圳市中考化学试卷】-第1页
试卷格式:2020年广东省深圳市中考化学试卷.PDF
试卷热词:最新试卷、2020年、广东试卷、深圳市试卷、化学试卷、九年级试卷、中考试卷、初中试卷
扫码查看解析
试卷题目
1.下列描述正确的是( )
- A. “滴水成冰”是化学变化
- B. “花香四溢”表明分子在不断运动
- C. “釜底抽薪”是为了降低可燃物的着火点
- D. “百炼成钢”指生铁经多次煅炼转化为纯铁
2.如图为铕在元素周期表中的相关信息,下列有关铕的说法正确的是( )
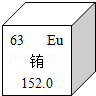

- A. 铕原子中的质子数为63
- B. 铕的相对原子质量是152.0g
- C. 2Eu2+表示2个铕原子
- D. Eu2O3中铕元素的化合价为+6价
3.化学与人类的科学技术、生产生活密切相关。下列说法错误的是( )
- A. 钛合金可应用于火箭和航天飞机
- B. 头盔缓冲层中的塑料属于合成材料
- C. 垃圾分类有利于废旧金属的回收利用
- D. 霉变的花生经冲洗、蒸煮后仍可食用
4.小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是( )
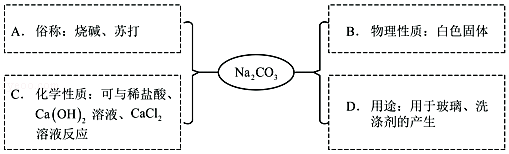

- A. A
- B. B
- C. C
- D. D
5.“艾叶香,香满堂;粽子香,香厨房。”据研究,粽子的香味源于粽叶的主要成分﹣﹣对乙烯基苯酚(化学式为C8H8O)。下列说法正确的是( )
- A. 对乙烯基苯酚不属于有机物
- B. 对乙烯基苯酚由3种元素组成
- C. 对乙烯基苯酚中C、H、O三种元素的质量比为8:8:1
- D. 对乙烯基苯酚由8个C原子、8个H原子、1个O原子构成
6.下列实验不能达到相应目的的是( )
- A.
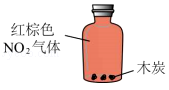 验证木炭具有吸附性
验证木炭具有吸附性 - B.
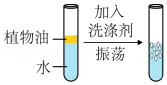 观察乳化现象
观察乳化现象 - C.
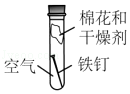 探究铁生锈的条件
探究铁生锈的条件 - D.
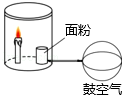 验证面粉在一定条件下能爆炸
验证面粉在一定条件下能爆炸
7.我国化学家研究出一种新型催化剂,在太阳光照射下实现了水的高效分解。该反应过程的微观示意图如图:
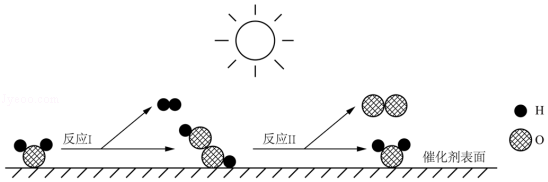
下列说法错误的是( )

下列说法错误的是( )
- A.
 表示的物质属于氧化物
表示的物质属于氧化物 - B. 反应Ⅰ的化学方程式为H2OH2O2+H2↑
催化剂 - C. 反应Ⅱ中,反应前后原子的种类和数目均不变
- D. 该成果对氢能源的推广应用有重要的实践意义
8.如图为Ca(OH)2的溶解度曲线;如表为20℃时溶解度的相对大小。
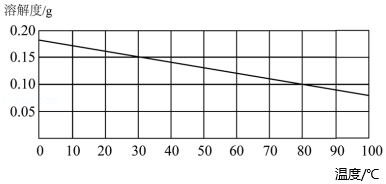
下列说法正确的是( )

| 溶解度/g | 一般称为 |
| <0.01 | 难溶 |
| 0.01~1 | 微溶 |
| 1~10 | 可溶 |
| >10 | 易溶 |
下列说法正确的是( )
- A. Ca(OH)2属于易溶物质
- B. Ca(OH)2的溶解度随温度的升高而增大
- C. 30℃时,Ca(OH)2的饱和溶液中溶质与溶剂的质量比为3:20
- D. 70℃时Ca(OH)2的饱和溶液,降温到50℃时没有析出固体
9.下列方法能达到除杂目的的是( )
| 选项 | 物质(括号内为杂质) | 方法 |
| A | CH4(CO) | 点燃混合气体 |
| B | 铜粉(炭粉) | 在空气中灼烧固体混合物 |
| C | O2(水蒸气) | 将混合气体通过浓硫酸 |
| D | NaCl(CaCl2) | 加水溶解、过滤 |
- A. A
- B. B
- C. C
- D. D
10.如图,将胶头滴管中的物质X滴入装有物质Y的试管中,两物质充分反应。下列说法错误的是( )


- A. X为稀硫酸,若反应有气泡产生,则生成的气体一定是H2
- B. X为AgNO3溶液,Y为Cu片,根据现象可判断金属活动性:Cu>Ag
- C. X为BaCl2溶液,Y为Na2SO4溶液,反应产生白色沉淀
- D. X为稀盐酸,Y为Al(OH)3,该反应可应用于治疗胃酸过多症
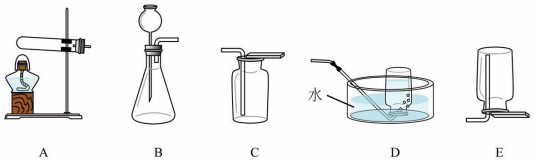
11.初步学习运用简单的装置和方法制取某些气体,是初中学生的化学实验技能应达到的要求。
(1)某学习小组将实验室制取常见气体的相关知识归纳如下:
(2)该小组将制取的O2和CO2(各一瓶)混淆了,设计如下方案进行区分。
(3)制取气体的过程包括:a.选择制取装置;b.验证所得气体;c.明确反应原理。据此,该小组总结出实验室里制取气体的一般思路为 (填“甲”或“乙”或“丙”)。
甲、a→b→c 乙、b→a→c 丙、c→a→b
(1)某学习小组将实验室制取常见气体的相关知识归纳如下:

| 气体 | 方法(或原理) | 发生装置 | 收集装置 |
| O2 | 方法1:加热氯酸钾 | 均可选择A装置(可根据需要添加棉花) | 均可选择④ 装置(填标号) |
| 方法2:加热① (填化学式) | |||
| 方法3:分解过氧化氢溶液 | 均可选择③ 装置(填标号) | ||
| CO2 | 化学方程式为② |
(2)该小组将制取的O2和CO2(各一瓶)混淆了,设计如下方案进行区分。
| 方案 | 现象 | 结论 |
| 方案1:将带火星的木条分别伸入两个集气瓶中 | 若带火星的木条① | 则该瓶气体是O2 |
| 方案2:向两个集气瓶中分别滴入少量的② 溶液,振荡 | 若溶液变浑浊 | 则该瓶气体是CO2 |
| 方案3:向两个集气瓶中分别倒入少量的水,振荡后再滴加几滴紫色石蕊溶液 | 若紫色石蕊溶液变为③ 色 | 则该瓶气体是CO2 |
| …… | …… | …… |
(3)制取气体的过程包括:a.选择制取装置;b.验证所得气体;c.明确反应原理。据此,该小组总结出实验室里制取气体的一般思路为 (填“甲”或“乙”或“丙”)。
甲、a→b→c 乙、b→a→c 丙、c→a→b
12.如图所示流程可用于制备硫酸铵。
Ⅰ.制硫酸:

(1)反应①的化学方程式为 。
(2)反应②为SO3+H2O═H2SO4,该反应属于 反应(填基本反应类型)。
Ⅱ.合成氨:

(3)“原料气”中N2的制备:N2约占空气体积的五分之 ,可通过分离液态空气的方法得到。
(4)“原料气”中H2的制备:高温时,CH4和水蒸气在催化剂作用下反应得到H2和CO2,该反应的化学方程式为 。
(5)NH3溶于水时形成氨水。室温下,氨水的pH 7(填“>”或“<”)。
Ⅲ.制备硫酸铵:
(6)将NH3通入稀释后的硫酸溶液中,得到硫酸铵。用水稀释浓硫酸时,需将 缓慢地加入 中,并不断搅拌。
(7)(NH4)2SO4在农业生产中常被用作 (填标号)。
A.氮肥 B.磷肥 C.钾肥
Ⅰ.制硫酸:

(1)反应①的化学方程式为 。
(2)反应②为SO3+H2O═H2SO4,该反应属于 反应(填基本反应类型)。
Ⅱ.合成氨:

(3)“原料气”中N2的制备:N2约占空气体积的五分之 ,可通过分离液态空气的方法得到。
(4)“原料气”中H2的制备:高温时,CH4和水蒸气在催化剂作用下反应得到H2和CO2,该反应的化学方程式为 。
(5)NH3溶于水时形成氨水。室温下,氨水的pH 7(填“>”或“<”)。
Ⅲ.制备硫酸铵:
(6)将NH3通入稀释后的硫酸溶液中,得到硫酸铵。用水稀释浓硫酸时,需将 缓慢地加入 中,并不断搅拌。
(7)(NH4)2SO4在农业生产中常被用作 (填标号)。
A.氮肥 B.磷肥 C.钾肥
13.氧气是人类生产活动的重要资源。
(1)下列属于O2的化学性质的是 (填标号)。
A.O2能支持燃烧
B.O2的密度比空气的密度略大
C.O2在低温、高压时能变为液体或固体
(2)小圳同学进行实验室制备O2的相关探究。
【查阅】他得知在KClO3分解制O2的反应中,Fe2O3可作催化剂。
【实验】他用电子秤称取0.49g Fe2O3和一定量的KClO3,充分混合后加热至KClO3完全分解,冷却至室温,称得剩余固体的质量为1.98g。
【计算】①剩余固体中KCl的质量是 g。
②该反应生成O2的质量(根据化学方程式写出完整的计算步骤)。
【思考】他发现制备O2较慢,猜测KClO3和Fe2O3的质量比可能会影响反应的快慢。
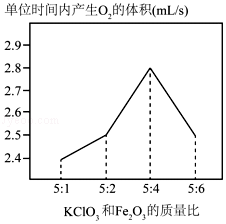
【探究】③他调节KClO3和Fe2O3的质量比制备O2,整理数据绘制出如图,从图中得出KClO3和Fe2O3最佳质量比是 。
【结论】④根据质量守恒定律,请你计算出小圳同学在【实验】中称取的KClO3的质量为 g,KClO3和Fe2O3的质量比是 (填最简比),不是最佳质量比。
(1)下列属于O2的化学性质的是 (填标号)。
A.O2能支持燃烧
B.O2的密度比空气的密度略大
C.O2在低温、高压时能变为液体或固体
(2)小圳同学进行实验室制备O2的相关探究。
【查阅】他得知在KClO3分解制O2的反应中,Fe2O3可作催化剂。
【实验】他用电子秤称取0.49g Fe2O3和一定量的KClO3,充分混合后加热至KClO3完全分解,冷却至室温,称得剩余固体的质量为1.98g。
【计算】①剩余固体中KCl的质量是 g。
②该反应生成O2的质量(根据化学方程式写出完整的计算步骤)。
【思考】他发现制备O2较慢,猜测KClO3和Fe2O3的质量比可能会影响反应的快慢。
【探究】③他调节KClO3和Fe2O3的质量比制备O2,整理数据绘制出如图,从图中得出KClO3和Fe2O3最佳质量比是 。
【结论】④根据质量守恒定律,请你计算出小圳同学在【实验】中称取的KClO3的质量为 g,KClO3和Fe2O3的质量比是 (填最简比),不是最佳质量比。

查看全部题目