下载高清试卷
【2020-2021学年广东省揭阳市空港区九年级(上)期中化学试卷】-第1页
试卷格式:2020-2021学年广东省揭阳市空港区九年级(上)期中化学试卷.PDF
试卷热词:最新试卷、2021年、广东试卷、揭阳市试卷、化学试卷、九年级上学期试卷、期中试卷、初中试卷

扫码查看解析
试卷题目
1.中华文字博大精深,下列成语的本意主要涉及化学变化的是( )
- A. 春风化雨
- B. 火上浇油
- C. 叶落知秋
- D. 滴水成冰
2.下列物质的用途是利用其物理性质的是( )
- A. 氧气用于气割
- B. 氢气作燃料
- C. 液氮冷冻
- D. 氩气作保护气
3.下列化学实验操作正确的是( )
- A.
 振荡试管
振荡试管 - B.
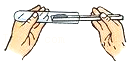 取固体药品
取固体药品 - C.
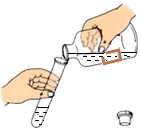 倾倒溶液
倾倒溶液 - D.
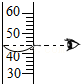 量筒读数
量筒读数
4.地壳中含量最多的金属元素是( )
- A. Fe
- B. Al
- C. Si
- D. O
5.医疗急救中输氧,其中“氧”指的是( )
- A. 氧气
- B. 氧元素
- C. 臭氧
- D. 氧单质
6.2020年6月,某高速路上一辆液化石油气槽罐车发生爆炸。爆炸产生的以下物质不属于空气污染物的是( )
- A. NO2
- B. CO
- C. 粉尘
- D. CO2
7.如图是探究空气和呼出气体中CO2的含量差异。下列叙述不正确的是( )
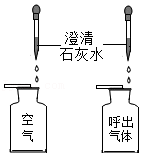

- A. 滴入的澄清石灰水的滴数要相同
- B. 该实验证明呼出气体中CO2体积含量比空气大
- C. 该实验证明人体呼出的气体是CO2
- D. 滴入石灰水振荡集气瓶有利气液充分接触短时产生更明显现象
8.取用80g水,最好使用下列哪些仪器进行操作达到目的( )
- A. 托盘天平、小烧杯和胶头滴管
- B. 100mL量筒
- C. 50mL量筒
- D. 100mL量筒和胶头滴管
9.下列有关催化剂的说法正确的是( )
- A. 在化学反应后其质量减小
- B. 过氧化氢分解反应中,只能用二氧化锰作催化剂
- C. 在化学反应后其化学性质不变
- D. 催化剂只能加快化学反应速率
10.如图两位同学在讨论氧的元素符号的意义。下面他们关于氧元素符号意义说法错误的是( )


- A. 表示氧原子
- B. 表示一个氧原子
- C. 表示氧元素
- D. 表示氧气
11.下面反应既不是化合反应,又不是分解反应,但却是氧化反应的是( )
- A. 石蜡+氧气水+二氧化碳点燃
- B. 氧化汞汞+氧气加热
- C. 硫+氧气二氧化硫点燃
- D. 硫酸铜+氢氧化钠→氢氧化铜+硫酸钠
12.下列各组物质中,属于纯净物的是( )
- A. 医用生理盐水
- B. 瓶装矿泉水
- C. 冰水混合物
- D. 未经污染的空气
13.下列对河水的净化操作中,净化程度最高的是( )
- A. 蒸馏
- B. 过滤
- C. 加入活性炭
- D. 静置沉淀
14.下列做法违背节水理念的是( )
- A. 防止水龙头滴漏
- B. 采用大水漫灌农作物
- C. 使用节水器具
- D. 循环利用工业用水
15.某同学利用图甲所示装置测定空气中氧气的含量,其中燃烧匙内的白磷用电加热装置点燃,瓶内气压用气体压强传感器测定,其变化如图乙所示。则下列分析合理的是( )
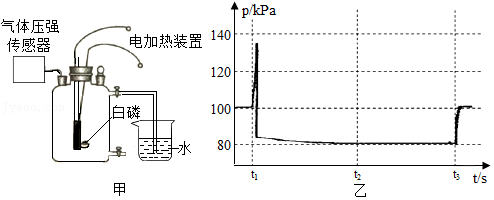

- A. t1时刻后的一段时间能观察到白磷燃烧产生大量白色烟雾
- B. 从瓶内气压达到最高点直至t2时刻,瓶内温度始终保持不变
- C. 根据t2时刻瓶内的气压值,可以计算出氧气占空气体积的百分比
- D. t3时刻后的一段时间内瓶内气压又显著增加,其原因是温度又升高了
16.水和空气都是重要的自然资源,与人类的生产生活密切相关。
(1)生活中常用 区分硬水和软水。硬水软化其实是降低水中镁离子和 (填离子名称)的浓度;
(2)宏观看水是由 (填元素符号)两种元素组成,微观看是由 (“分子”或“原子”或“离子”)构成;
(3)保护环境势在必行。请写出造成水体污染的原因 (答一点即可);
(4)稀有气体用途广泛, (填名称)可用于填充气球或飞艇;
(5)食物包装袋充入一种单质气体 可达到食物防腐的作用;
(6)空气质量日报可以及时准确反映空气质量状况。空气质量级别分为六级,级别越高则空气污染程度越 (填“轻”或“重”)。
(1)生活中常用 区分硬水和软水。硬水软化其实是降低水中镁离子和 (填离子名称)的浓度;
(2)宏观看水是由 (填元素符号)两种元素组成,微观看是由 (“分子”或“原子”或“离子”)构成;
(3)保护环境势在必行。请写出造成水体污染的原因 (答一点即可);
(4)稀有气体用途广泛, (填名称)可用于填充气球或飞艇;
(5)食物包装袋充入一种单质气体 可达到食物防腐的作用;
(6)空气质量日报可以及时准确反映空气质量状况。空气质量级别分为六级,级别越高则空气污染程度越 (填“轻”或“重”)。
17.在宏观、微观和符号之间建立联系是化学学科的特点。
(一)氢、碳和氧的原子结构示意图如图1所示,回答下列问题。
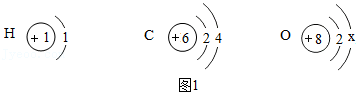
(1)x的值是 。
(2)氢原子失去一个电子后形成 (填符号)。
(3)根据下表信息可知氕、氘、氚都属于氢元素,理由是 。
(4)如表可获得的结论有 (答一条即可)。
(5)科学家们已经俘获了少量的反氢原子。正电子、负质子等都是反粒子,它们跟通常所说的电子、质子相比较,质量相等但电性相反。请你推测反氢原子的结构可能是 (填字母代号)。
A.由1个带正电荷的质子和1个带负电荷的电子构成
B.由1个带负电荷的质子和1个带正电荷的电子构成
C.由1个带正电荷的质子和1个带正电荷的电子构成
D.由1个带负电荷的质子和1个带负电荷的电子构成
(二)近年来,我国科研人员在“甲烷二氧化碳重整和Ni基催化剂”的研究方面取得突破。如图2是甲烷与二氧化碳反应的微观示意图。
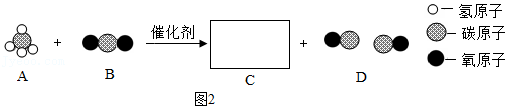
(6)在框内补充C的微观模型图。
(7)该反应利用两种温室气体,兼具环保和经济价值;反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,分为 (填微粒名称)并重新组合。
(8)写出该反应的文字表达式: 。
(一)氢、碳和氧的原子结构示意图如图1所示,回答下列问题。

(1)x的值是 。
(2)氢原子失去一个电子后形成 (填符号)。
(3)根据下表信息可知氕、氘、氚都属于氢元素,理由是 。
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 相对原子质量 |
| 氕 | 1 | 0 | 1 | 1 |
| 氘 | 1 | 1 | 1 | 2 |
| 氚 | 1 | 2 | 1 | 3 |
(4)如表可获得的结论有 (答一条即可)。
(5)科学家们已经俘获了少量的反氢原子。正电子、负质子等都是反粒子,它们跟通常所说的电子、质子相比较,质量相等但电性相反。请你推测反氢原子的结构可能是 (填字母代号)。
A.由1个带正电荷的质子和1个带负电荷的电子构成
B.由1个带负电荷的质子和1个带正电荷的电子构成
C.由1个带正电荷的质子和1个带正电荷的电子构成
D.由1个带负电荷的质子和1个带负电荷的电子构成
(二)近年来,我国科研人员在“甲烷二氧化碳重整和Ni基催化剂”的研究方面取得突破。如图2是甲烷与二氧化碳反应的微观示意图。

(6)在框内补充C的微观模型图。
(7)该反应利用两种温室气体,兼具环保和经济价值;反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,分为 (填微粒名称)并重新组合。
(8)写出该反应的文字表达式: 。
18.空腔果实内由于不发生光合作用,其中的气体可能与空气产生差异,某同学选择一个熟透的葫芦,按下列方案进行研究:
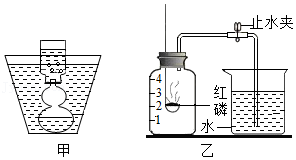
(1)图甲所示,收集葫芦中气体采用的方法是 。
(2)图乙中用来测定葫芦中 的含量,燃烧匙伸入集气瓶之前,止水夹 (填代号“要事先夹紧”或“不能夹紧”),集气瓶中发生反应的文字表达式是 。
(3)检验葫芦中有无CO2气体,应采用的方法是: 。

(1)图甲所示,收集葫芦中气体采用的方法是 。
(2)图乙中用来测定葫芦中 的含量,燃烧匙伸入集气瓶之前,止水夹 (填代号“要事先夹紧”或“不能夹紧”),集气瓶中发生反应的文字表达式是 。
(3)检验葫芦中有无CO2气体,应采用的方法是: 。
19.某研究小组对过氧化氢溶液制取氧气进行如下探究。
实验一:氧气制取和性质实验
(1)现有如图1装置
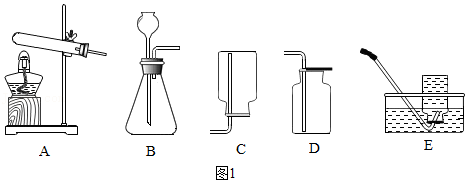
①写出B装置中任一种仪器的名称 。
②实验室用过氧化氢溶液制氧气的反应的文字表达为 ,应选择的发生装置是 (填标号,下同),收集较纯净氧气的装置应选择 。
③用收集的氧气进行“铁丝在氧气中燃烧”的实验,瓶中预先铺层细沙的目的是 ,反应的文字表达为 。
实验二:探究H2O2溶液浓度、溶液酸碱度和温度“三度”对反应速率的影响
(2)设计如表实验方案:
①实验①~②的实验目的是 。
②a= ;b= 。
实验三:探究制取氧气的适宜催化剂
(3)实验方案如下:
Ⅰ.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用如图2装置进行实验。改用其他三种微球,分别重复上述实验,得到如图3的锥形瓶内压强随时间变化的曲线图。
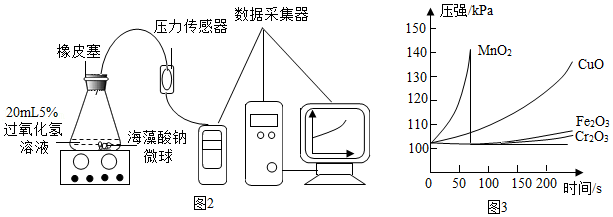
①每次实验时,海藻酸钠微球数应相同的原因 。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是 。
③从实验曲线看,催化效果较好、反应温和的催化剂是 。
实验一:氧气制取和性质实验
(1)现有如图1装置

①写出B装置中任一种仪器的名称 。
②实验室用过氧化氢溶液制氧气的反应的文字表达为 ,应选择的发生装置是 (填标号,下同),收集较纯净氧气的装置应选择 。
③用收集的氧气进行“铁丝在氧气中燃烧”的实验,瓶中预先铺层细沙的目的是 ,反应的文字表达为 。
实验二:探究H2O2溶液浓度、溶液酸碱度和温度“三度”对反应速率的影响
(2)设计如表实验方案:
| 实验编号 | 溶液浓度 | 溶液酸碱度 | 溶液温度 | 记录每分钟气泡数 |
| ① | 30 | 5 | 20 | |
| ② | 30 | 7 | 20 | |
| ③ | 20 | 10 | b | |
| ④ | 15 | 10 | 20 | |
| ⑤ | a | 10 | 15 |
①实验①~②的实验目的是 。
②a= ;b= 。
实验三:探究制取氧气的适宜催化剂
(3)实验方案如下:
Ⅰ.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用如图2装置进行实验。改用其他三种微球,分别重复上述实验,得到如图3的锥形瓶内压强随时间变化的曲线图。

①每次实验时,海藻酸钠微球数应相同的原因 。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是 。
③从实验曲线看,催化效果较好、反应温和的催化剂是 。
20.氨是一种重要的化学物质,可用于制造硝酸和氮肥。工业合成氨的流程如图1所示。
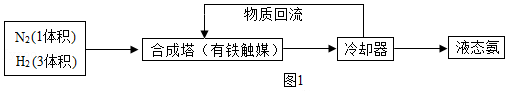
(1)氢气在点燃之前务必检验 。
(2)空气氮气体积约占空气体积 %,工业上可用 的方法获得合成氨的原料N2。
(3)若用电解水方法制得原料气H2,则该反应的文字表达式为 。
(4)回流“合成塔”的物质是 (填“纯净物”或“混合物”)。
(5)合成塔中的铁触媒在反应中起 作用。
(6)液态氨的分子间隔 (填“大于”或“小于”)气态氨的分子间隔。
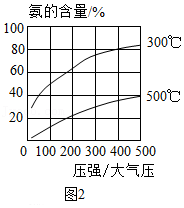
(7)氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图2所示。那么按下列条件进行合成氨反应,平衡时氨的含量最高的是 (填字母)。
A.200大气压和300℃
B.200大气压和500℃
C.400大气压和300℃
D.400大气压和500℃

(1)氢气在点燃之前务必检验 。
(2)空气氮气体积约占空气体积 %,工业上可用 的方法获得合成氨的原料N2。
(3)若用电解水方法制得原料气H2,则该反应的文字表达式为 。
(4)回流“合成塔”的物质是 (填“纯净物”或“混合物”)。
(5)合成塔中的铁触媒在反应中起 作用。
(6)液态氨的分子间隔 (填“大于”或“小于”)气态氨的分子间隔。
(7)氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图2所示。那么按下列条件进行合成氨反应,平衡时氨的含量最高的是 (填字母)。

A.200大气压和300℃
B.200大气压和500℃
C.400大气压和300℃
D.400大气压和500℃
21.如图是氧分子模型和元素周期表中“氧格”信息。据此解决下列问题:
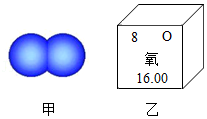
(1)已知相对原子质量≈质子数+中子数,则一般的氧原子中含有 个中子;
(2)一个氧分子由 构成,共含有 个电子。
(3)做氧气性质实验需要4瓶容积为250mL的氧气,则氧气总质量为 ,相当于 L(填整数)空气中的氧气含量。(温馨提示:氧气密度1.293g/L)
(4)已知一个碳原子质量为1.993×10﹣26kg。根据图乙可计算出一个氧分子的实际质量为 。

(1)已知相对原子质量≈质子数+中子数,则一般的氧原子中含有 个中子;
(2)一个氧分子由 构成,共含有 个电子。
(3)做氧气性质实验需要4瓶容积为250mL的氧气,则氧气总质量为 ,相当于 L(填整数)空气中的氧气含量。(温馨提示:氧气密度1.293g/L)
(4)已知一个碳原子质量为1.993×10﹣26kg。根据图乙可计算出一个氧分子的实际质量为 。
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解