下载高清试卷
【2020年四川省达州市中考化学一模试卷】-第1页
试卷格式:2020年四川省达州市中考化学一模试卷.PDF
试卷热词:最新试卷、2020年、四川试卷、达州市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.端午节吃粽子是传统习俗,在制作粽子的过程中一定发生了化学变化的是( )
- A. 水洗糯米
- B. 刀切肉块
- C. 粽叶包粽
- D. 烧火煮粽
2.下列实验操作正确的是( )
- A.
 稀释浓硫酸
稀释浓硫酸 - B.
 粗食盐水过滤
粗食盐水过滤 - C.
 点燃酒精灯
点燃酒精灯 - D.
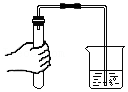 检查装置气密性
检查装置气密性
3.2019年3月21日,江苏省盐城市某化工园区发生爆炸事故,爆炸物为苯,查得一个苯分子的结构如图所示,下列说法正确的是( )


- A. 苯的分子式为C6H6
- B. 苯中碳元素和氢元素的质量比为1:1
- C. 一个苯分子中的质子总数为78
- D. 苯完全燃烧后只生成二氧化碳
4.氨催化氧化是制硝酸的主要反应之一,该反应前后分子种类变化的微观示意图如图。下列说法正确的是( )


- A. 生成的丙与丁的分子个数比为2:3
- B. 乙的相对分子质量为32g
- C. 反应前后分子的个数不变
- D. 反应过程中共涉及三种氧化物
5.下列知识归纳都正确的一组是( )
| A.物质类型与组成 | B.化学与生活 |
| 生铁、钢都是铁合金纯碱、烧碱都是碱干冰、可燃冰都是冰 | 生活中软化硬水可用肥皂水酒精、汽油、液化气都是易燃物油锅、电器着火都可用水浇灭 |
| C.物质与使用 | D.化学与健康 |
| 点燃可燃性气体前都要验纯铵态氮肥不能与草木灰(碱性)混用食醋可以清除水垢 | 人体缺碘易患贫血病老年人缺钙易患佝偻症儿童缺锌引起食欲不振、发育不良 |
- A. A
- B. B
- C. C
- D. D
6.用K2CO3溶液吸收CO2得到KHCO3,化学方程式为:K2CO3+CO2+H2O═2KHCO3.向K2CO3溶液中通入CO2,至K2CO3恰好完全反应,得到溶质的质量分数为20%的溶液50.0g。则原K2CO3溶液中溶质的质量分数为( )
- A. 13.8%
- B. 14.4%
- C. 15.4%
- D. 16.8%
7.下列除去杂质所选用的试剂正确的是( )
| 选项 | 物质 | 杂质(少量) | 除杂试剂 |
| A | N2 | O2 | 灼热的铜网 |
| B | CaO | Ca(OH)2 | 水 |
| C | NaCl溶液 | Na2SO4 | Ba(NO3)2溶液 |
| D | FeSO4溶液 | CuSO4 | 锌粉 |
- A. A
- B. B
- C. C
- D. D
8.下列图象与所对应操作相符的是( )
- A.
 用两份等质量、等质量分数的过氧化氢溶液制取氧气
用两份等质量、等质量分数的过氧化氢溶液制取氧气 - B.
 向一定质量分数的盐酸中不断加水
向一定质量分数的盐酸中不断加水 - C.
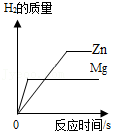 向等质量的锌片、镁片中分别加入足量的等质量分数的稀硫酸
向等质量的锌片、镁片中分别加入足量的等质量分数的稀硫酸 - D.
 向一定质量的氯化铜和稀盐酸的混合溶液中不断加NaOH溶液
向一定质量的氯化铜和稀盐酸的混合溶液中不断加NaOH溶液
9.从Fe、C、S、H、O、N六种元素中选择适当的元素按要求填空。
(1)用适当的数字和符号填空:
①三个亚铁离子 。
②两个氮分子 。
③双氧水中氧的化合价 。
(2)写出符合下列要求的物质的化学式:
①可作复合肥料的是 。
②能形成硫酸型酸雨的空气污染物是 。
③相对分子质量最小的氧化物是 。
(1)用适当的数字和符号填空:
①三个亚铁离子 。
②两个氮分子 。
③双氧水中氧的化合价 。
(2)写出符合下列要求的物质的化学式:
①可作复合肥料的是 。
②能形成硫酸型酸雨的空气污染物是 。
③相对分子质量最小的氧化物是 。
10.中国科学院院士张青莲教授主持测定了铟等元素的相对原子质量的新值,为相对原子质量的测定做出了卓越贡献,铟元素在元素周期表中的某些信息及原子结构示意图如图所示,请回答下列问题。
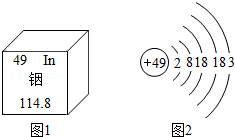
(1)铟元素的相对原子质量为 。
(2)铟原子的核电荷数为 ,在化学反应中铟原子容易 (填“得到”或“失去”)电子。

(1)铟元素的相对原子质量为 。
(2)铟原子的核电荷数为 ,在化学反应中铟原子容易 (填“得到”或“失去”)电子。
11.小军利用周末去外婆家做客,外婆家座落在有“梯田王国”之美誉的紫鹊界。

(1)中午,外婆做了一顿别致的午餐,有:①红米煮的饭,②水煮稻花鱼,③竹笋炒腊肉,④凉拌醋黄瓜。其中富含糖类的是 。(填序号)
(2)做饭菜用的水就是从山洞中引米的山泉水。你认为小军可以通过加入 米判断山泉水是硬水还是软水。
(3)做菜用的炊具是一口铁锅,铁锅能用于做菜是利用了铁具有良好的 性。铁锅的手柄是用塑料做的,塑料属于 (填“金属材料”或“合成材料”)
(4)用完午餐后,小军主动帮外婆洗碗。用洗洁精去除餐具上的油污是利用了洗洁精的 作用。

(1)中午,外婆做了一顿别致的午餐,有:①红米煮的饭,②水煮稻花鱼,③竹笋炒腊肉,④凉拌醋黄瓜。其中富含糖类的是 。(填序号)
(2)做饭菜用的水就是从山洞中引米的山泉水。你认为小军可以通过加入 米判断山泉水是硬水还是软水。
(3)做菜用的炊具是一口铁锅,铁锅能用于做菜是利用了铁具有良好的 性。铁锅的手柄是用塑料做的,塑料属于 (填“金属材料”或“合成材料”)
(4)用完午餐后,小军主动帮外婆洗碗。用洗洁精去除餐具上的油污是利用了洗洁精的 作用。
12.硝酸钾和氯化钾的溶解度曲线如图所示:
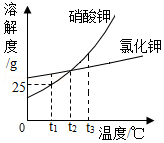
(1) ℃时,硝酸钾和氯化钾的溶解度相等;
(2)t1℃时,将50g硝酸钾加入50g水中,充分溶解后,所得溶液中溶质的质量分数为 ;
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是 ;
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t2℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是 (填字母代号)。
A. 都是饱和溶液 B. 溶液质量a<b C. 溶质质量a=b
D. 溶剂质量a<b E. 溶质的质量分数a=b

(1) ℃时,硝酸钾和氯化钾的溶解度相等;
(2)t1℃时,将50g硝酸钾加入50g水中,充分溶解后,所得溶液中溶质的质量分数为 ;
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是 ;
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t2℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是 (填字母代号)。
A. 都是饱和溶液 B. 溶液质量a<b C. 溶质质量a=b
D. 溶剂质量a<b E. 溶质的质量分数a=b
13.金属具有广泛的应用。
(1)铁锅用来炒菜,主要是利用铁的 (填“导热”或“导电”)性。
(2)如图流程为洁净铁钉的有关实验。

①中铁与硫酸铜反应的化学方程式为 。
②中铁钉锈蚀主要是铁与空气中的氧气和 发生化学反应。
③中铁锈与稀硫酸反应的化学方程式为 。
(3)某炼铁厂要冶炼1000t含杂质3%的生铁,需要含Fe2O380%的赤铁矿石的质量约是 t(计算结果精确至0.1)。
(4)某金属粉末可能由镁、锌、铁、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法正确的是 (填序号)。
A.样品中一定含有镁 B.样品中一定不含有银,可能含有镁
C.所得溶液中溶质总质量为12g D.加入的稀硫酸的溶质质量分数为19.6%
(1)铁锅用来炒菜,主要是利用铁的 (填“导热”或“导电”)性。
(2)如图流程为洁净铁钉的有关实验。

①中铁与硫酸铜反应的化学方程式为 。
②中铁钉锈蚀主要是铁与空气中的氧气和 发生化学反应。
③中铁锈与稀硫酸反应的化学方程式为 。
(3)某炼铁厂要冶炼1000t含杂质3%的生铁,需要含Fe2O380%的赤铁矿石的质量约是 t(计算结果精确至0.1)。
(4)某金属粉末可能由镁、锌、铁、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法正确的是 (填序号)。
A.样品中一定含有镁 B.样品中一定不含有银,可能含有镁
C.所得溶液中溶质总质量为12g D.加入的稀硫酸的溶质质量分数为19.6%
14.如图所示,A是金属氧化物,B是金属单质,C是黄色溶液,D是浅绿色溶液,E是红褐色沉淀,反应③是物质F与氧气、水发生的化合反应,请回答下列问题:

(1)写出C的化学式 。
(2)化学反应①的基本类型是 。
(3)写出反应②和③的化学方程式:
② ;③ 。

(1)写出C的化学式 。
(2)化学反应①的基本类型是 。
(3)写出反应②和③的化学方程式:
② ;③ 。
15.请分析下列实验装置,阅读所给材料,回答问题:

材料:氨气(NH3)常温下是一种具有刺激性气味的无色气体,对人体有较大毒性,密度比空气小,极易溶于水,其水溶液显碱性。实验室可用加热氯化铵(NH4Cl)和熟石灰两种固体的方法制取氨气,同时生成氯化钙和水。铵盐易溶于水,Ca(OH)2微溶于水,CaCl2溶液显中性,NH4Cl溶液显酸性。
(1)实验室制取氨气的化学方程式为 ,应选取的发生装置是 (填装置编号)。
(2)用C装置收集氨气时,气体应从 口通入(填“a”或“b”);检验氨气可用湿润的 石蕊试纸(填“红色”或“蓝色”)。
(3)某同学对充分反应后反应器内的固体物质做进一步研究:
【提出问题】固体物质的成分是什么?
【作出猜想】猜想I:Ca(OH)2、NH4Cl和CaCl2
猜想II:Ca(OH)2和CaCl2
猜想III:NH4Cl和CaCl2
猜想IV:只有CaCl2
有同学对上述猜想提出质疑:有一种猜想不合理。你认为是 。
【实验探究】①取反应器内少量固体于试管中,加水溶解、过滤,得到滤液。
(4)②取少量溶液于试管中,滴加无色酚酞试液溶液,颜色无变化,说明 (填一种猜想)不正确。
(5)③再取少量滤液于另一试管中,滴加AgNO3溶液,产生白色沉淀,该同学认为固体中含有NH4Cl,于是得出结论猜想III正确。你认为该同学的结论 (填“合理“或“不合理”),理由是 。
(6)【评价反思】该同学认为实验装置仍有不足之处,请你提出改进措施: 。

材料:氨气(NH3)常温下是一种具有刺激性气味的无色气体,对人体有较大毒性,密度比空气小,极易溶于水,其水溶液显碱性。实验室可用加热氯化铵(NH4Cl)和熟石灰两种固体的方法制取氨气,同时生成氯化钙和水。铵盐易溶于水,Ca(OH)2微溶于水,CaCl2溶液显中性,NH4Cl溶液显酸性。
(1)实验室制取氨气的化学方程式为 ,应选取的发生装置是 (填装置编号)。
(2)用C装置收集氨气时,气体应从 口通入(填“a”或“b”);检验氨气可用湿润的 石蕊试纸(填“红色”或“蓝色”)。
(3)某同学对充分反应后反应器内的固体物质做进一步研究:
【提出问题】固体物质的成分是什么?
【作出猜想】猜想I:Ca(OH)2、NH4Cl和CaCl2
猜想II:Ca(OH)2和CaCl2
猜想III:NH4Cl和CaCl2
猜想IV:只有CaCl2
有同学对上述猜想提出质疑:有一种猜想不合理。你认为是 。
【实验探究】①取反应器内少量固体于试管中,加水溶解、过滤,得到滤液。
(4)②取少量溶液于试管中,滴加无色酚酞试液溶液,颜色无变化,说明 (填一种猜想)不正确。
(5)③再取少量滤液于另一试管中,滴加AgNO3溶液,产生白色沉淀,该同学认为固体中含有NH4Cl,于是得出结论猜想III正确。你认为该同学的结论 (填“合理“或“不合理”),理由是 。
(6)【评价反思】该同学认为实验装置仍有不足之处,请你提出改进措施: 。
16.咸宁市市某校2018年实验操作模拟考试的一个考题是:用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。
【进行实验】
(1) c中 ;
(2)写出a试管中发生反应的化学方程式 。
把c试管反应后的物质进行过滤,得到滤液。
(3)【提出问题】滤液中溶质的成分是什么?
猜想一:Na2CO3和NaOH;猜想二:NaOH;猜想三: 。
提示:Ca(OH)2微溶于水。
【实验过程】为证明猜想一是否正确,进行了如下实验
(4)取一定量滤液于试管中,加入一种盐溶液(写物质化学式) ;
(5)写出上述有白色沉淀生成的化学方程式 。
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值。
(6) 在白瓷板上放一小片pH试纸,用玻璃棒蘸取 。
(7)【反思与交流】a试管中的废液显酸性,从环保、经济、操作简便等方面考虑,应向废液加入(写化学式) 后再排放。
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 分别用a,b,c三支试管取样,各加入一定量碳酸钠溶液 | a中有气泡产生 | a中物质是稀盐酸 |
| b中无明显现象 | b中物质是食盐水 | |
| (1) c中________ | c中物质是澄清石灰水 |
(1) c中 ;
(2)写出a试管中发生反应的化学方程式 。
把c试管反应后的物质进行过滤,得到滤液。
(3)【提出问题】滤液中溶质的成分是什么?
猜想一:Na2CO3和NaOH;猜想二:NaOH;猜想三: 。
提示:Ca(OH)2微溶于水。
【实验过程】为证明猜想一是否正确,进行了如下实验
| 实验步骤 | 实验现象 | 实验结论 |
| (4)取一定量滤液于试管中,加入一种盐溶液(写物质化学式)________ | 有白色沉淀 | 猜想一正确 |
(4)取一定量滤液于试管中,加入一种盐溶液(写物质化学式) ;
(5)写出上述有白色沉淀生成的化学方程式 。
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值。
| 用pH试纸测定a试管反应后废液碱性的过程 | 测定结果 |
| (6) 在白瓷板上放一小片pH试纸,用玻璃棒蘸取________。 | pH<7(废液显酸性) |
(6) 在白瓷板上放一小片pH试纸,用玻璃棒蘸取 。
(7)【反思与交流】a试管中的废液显酸性,从环保、经济、操作简便等方面考虑,应向废液加入(写化学式) 后再排放。
17.对销售的化肥,国家有明确的质量要求。某兴趣小组对市售的某钾肥进行了检测,称取2.0g样品放入烧杯中,加入适量的水溶解后,逐滴加入10%的BaCl2溶液,产生沉淀的质量与所加入BaCl2溶液质量的关系如图1所示(假定杂质不参加反应)。
已知:K2SO4+BaCl2═BaSO4↓+2KCl。

(1)20.8g BaCl2溶液中所含溶质的质量为 g。
(2)通过计算,判断该钾肥中K2SO4的质量分数是否符合图2的包装说明?(写出计算过程)
已知:K2SO4+BaCl2═BaSO4↓+2KCl。

(1)20.8g BaCl2溶液中所含溶质的质量为 g。
(2)通过计算,判断该钾肥中K2SO4的质量分数是否符合图2的包装说明?(写出计算过程)
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解