下载高清试卷
【2021年四川省成都市武侯区中考化学二诊试卷】-第1页
试卷格式:2021年四川省成都市武侯区中考化学二诊试卷.PDF
试卷热词:最新试卷、2021年、四川试卷、成都市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.下列变化属于化学变化的是( )
- A. 生石灰吸水干燥气体
- B. 氢氧化钠固体吸水潮解
- C. 分离液态空气制氧气
- D. 浓盐酸敞口放置出现白雾
2.下列实验操作正确的是( )
- A.
 熄灭酒精灯
熄灭酒精灯 - B.
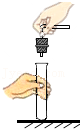 塞紧橡胶塞
塞紧橡胶塞 - C.
 移走加热后的蒸发皿
移走加热后的蒸发皿 - D.
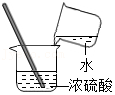 稀释浓硫酸
稀释浓硫酸
3.分类是化学学习中常用的方法。下列有关物质分类正确的是( )
- A. 单质:钢、液氧、红磷
- B. 碱:烧碱、纯碱、氨水
- C. 有机物:蛋白质、二氧化碳、乙醇
- D. 酸:盐酸、醋酸、硫酸
4.四川大学成功研制了我国首套二氧化碳零排放天然气制氢设备。该设备以液态金属锡为媒介,助力甲烷裂解,实现二氧化碳零排放、高效制氢。反应的微观示意图如图。下列说法正确的是( )
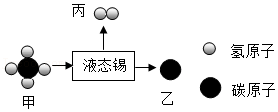

- A. 金属锡作反应的催化剂
- B. 反应中甲、丙分子个数比为1:1
- C. 反应中碳元素化合价降低
- D. 物质甲由1个碳原子和4个氢原子构成
5.建立“宏观﹣微观﹣符号”之间的联系是化学学科特有的思维方式。根据图中提供的信息判断,下列说法正确的是( )
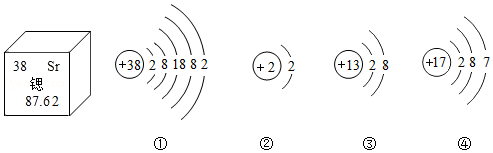

- A. 锶元素的相对原子质量为87.62g
- B. ①和②两元素的化学性质相似
- C. ①和④两元素组成物质的化学式为SrCl2
- D. ③所示的元素位于第二周期
6.化学与生活、生产、环境密切相关。下列归纳完全正确的一组是( )
| A.化学与健康 | B.化学与环境 |
| ①碘、铁、锌是人体必需的微量元素②人体缺钙会引起贫血③糖类、油脂、维生素是人体主要供能物质 | ①广泛使用新能源可以有效减少碳排放②乱扔塑料可能引起白色污染③煤燃烧产生的二氧化硫易形成酸雨 |
| C.化学与安全 | D.化学与材料 |
| ①点燃氢气前,一定要检验纯度②煤气泄漏应立即打开排气扇抽气③用煤炉取暖时,放置水能防止CO中毒 | ①塑料、棉花和合成橡胶属于合成材料②生铁、四氧化三铁和黄金属于金属材料③玻璃钢和钢筋混凝土属于复合材料 |
- A. A
- B. B
- C. C
- D. D
7.钴(Co)的化合物在锂电池生产中应用广泛。LiCoO2(钴酸锂)在酸性条件下具有较强的氧化性,可发生如下反应:2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+4H2O+O2↑。已知锂(Li)与钠原子最外层电子数相同。下列说法正确的是( )
- A. 上述反应中共有7种含氧化合物
- B. LiCoO2、Li2SO4、CoSO4都属于盐
- C. LiCoO2中钴酸根离子的符号为CoO22﹣
- D. 反应生成的水和氧气的质量比为4:1
8.下列实验设计能达到实验目的的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 除去氯化钠溶液中三种可溶性杂质MgCl2、Na2SO4和CaCl2 | 依次加过量的氢氧化钡、碳酸钠溶液,过滤,再向滤液中加入适量的稀盐酸 |
| B | 证明硫酸与氢氧化钠反应后,硫酸过量 | 取样,加入硝酸钡溶液,观察现象 |
| C | 除去H2中混有的HCl气体 | 将气体通过盛有碳酸钠溶液的洗气瓶洗气 |
| D | 鉴别NaOH溶液和Na2CO3溶液 | 取样,分别加入酚酞试液,观察现象 |
- A. A
- B. B
- C. C
- D. D
9.已知同温同压下,气体体积比等于气体的分子数目之比。常温下,向盛有一定量氧气的密闭容器通入氢气,用电火花点燃,使其充分反应,恢复至相同温度。测得容器中剩余气体的体积与通入氢气的体积关系如图所示。下列说法错误的是( )
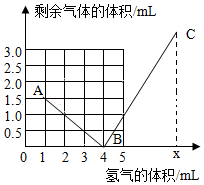

- A. B点表示氢气与氧气恰好反应
- B. 氧气的起始体积为2mL
- C. AB间,容器中剩余气体为氧气
- D. C点对应纵坐标为(x﹣2)
10.20℃时,KCl的溶解度是34g。取40℃的KCl溶液65g放入烧杯中,如图甲。按图示进行操作(整个过程中忽略溶剂损失)。
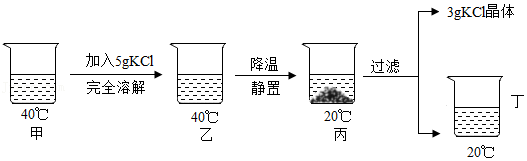
下列说法不正确的是( )

下列说法不正确的是( )
- A. 溶液中KCl的质量分数大小为:丙>甲
- B. 丁图溶液中溶质和溶剂的质量比为17:50
- C. 乙图中的KCl溶液一定为饱和溶液
- D. 实验可知,KCl的溶解度随温度升高而增大
11.向含有AgNO3和Cu(NO3)2的混合溶液中逐渐加入Zn粉,溶液的质量与加入Zn粉的质量关系如图所示。下列说法不正确的是( )
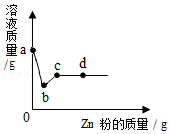

- A. ab间的反应为Zn+2AgNO3═Zn(NO3)2+2Ag
- B. c点溶液中的溶质仅有Zn(NO3)2一种
- C. d点对应的固体只有2种单质
- D. 整个实验过程,溶液由蓝色变为无色
12.常温下,向滴有酚酞试液的氢氧化钠溶液中滴加稀盐酸,如图1所示,并不断搅拌。烧杯中溶液温度变化如图2所示。关于上述实验的有关说法中,正确的是( )
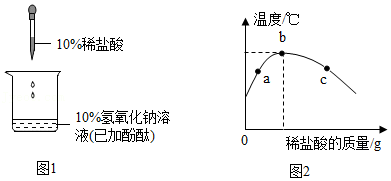
①a点时,溶液中所含溶质为HCl、NaCl(酚酞除外)
②从b点到c点,溶液的pH逐渐变大
③c点时,溶液为无色
④实验说明该反应为放热反应
⑤比较溶液中离子数目多少:a=b<c

①a点时,溶液中所含溶质为HCl、NaCl(酚酞除外)
②从b点到c点,溶液的pH逐渐变大
③c点时,溶液为无色
④实验说明该反应为放热反应
⑤比较溶液中离子数目多少:a=b<c
- A. ①②③
- B. ②③④
- C. ①③⑤
- D. ③④⑤
13.某固体粉末,可能含碳、镁、铜、氧化镁、氯化钠中的一种或几种。为探究该固体粉末的组成,设计如图所示实验。
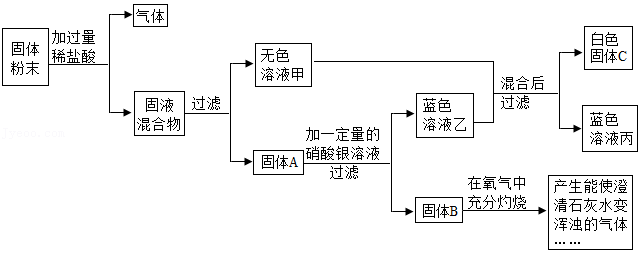
下列说法不正确的是( )

下列说法不正确的是( )
- A. 实验表明所加硝酸银溶液一定是过量
- B. 白色固体C为AgCl,故原固体粉末中必含氯化钠
- C. 无法确定固体粉末中是否含氧化镁
- D. 蓝色溶液丙中一定含有Mg2+、H+、Cu2+
14.一定温度下,向盛有ag Na2CO3溶液的烧杯中加入Ba(NO3)2固体,溶液的质量与加入Ba(NO3)2固体的质量变化关系如图所示。下列叙述错误的是( )
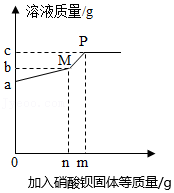

- A. Na2CO3完全反应时,消耗Ba(NO3)2的质量为ng
- B. 反应生成BaCO3沉淀的质量为(a+n﹣b)g
- C. P点时对溶质Ba(NO3)2而言,溶液达到饱和状态
- D. m、n的关系为:m=c+n﹣a
15.生活处处皆化学,厨房中蕴含着许多化学知识。回答下列问题:
(1)厨房中有食盐、食醋、小苏打、铁强化酱油等物质。焙制糕点所用发酵粉的主要成分是 (写化学式);“铁强化酱油”中的“铁”指 (填“单质”“原子”或“元素”);向食醋中加鸡蛋壳,可观察到的现象是 ;食盐的主要成分是氯化钠,氯化钠由 (填符号)构成。
(2)用铁锅炒菜是利用金属的 性;如果油锅着火,盖上锅盖即可灭火,其原理是 。
(3)用洗洁精去除餐具油污时,洗洁精使油污分散成细小液滴,随水流动。这种现象称为 。
(4)冰箱内放置活性炭可去除冰箱内的异味,是因为活性炭具有较强的 性。
(5)长时间放置的铁质搁物架在地面上留下锈迹,可用稀盐酸将其除去,其反应的化学方程式为 。
(1)厨房中有食盐、食醋、小苏打、铁强化酱油等物质。焙制糕点所用发酵粉的主要成分是 (写化学式);“铁强化酱油”中的“铁”指 (填“单质”“原子”或“元素”);向食醋中加鸡蛋壳,可观察到的现象是 ;食盐的主要成分是氯化钠,氯化钠由 (填符号)构成。
(2)用铁锅炒菜是利用金属的 性;如果油锅着火,盖上锅盖即可灭火,其原理是 。
(3)用洗洁精去除餐具油污时,洗洁精使油污分散成细小液滴,随水流动。这种现象称为 。
(4)冰箱内放置活性炭可去除冰箱内的异味,是因为活性炭具有较强的 性。
(5)长时间放置的铁质搁物架在地面上留下锈迹,可用稀盐酸将其除去,其反应的化学方程式为 。
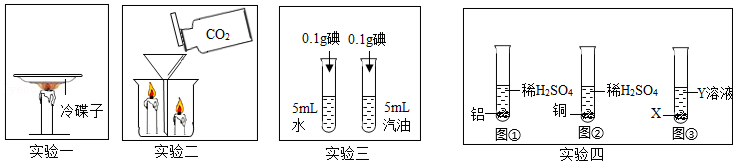
16.某兴趣小组设计并完成如图所示的实验。
回答下列问题:
(1)实验一中碟子底部出现黑色物质,该实验说明了 。
(2)实验二中低处蜡烛先熄灭,高处蜡烛后熄灭,说明二氧化碳具有的物理性质是 ,具有的化学性质是 。
(3)实验三的实验目的是 。
(4)实验四的实验目的是比较铝和铜的金属活动性强弱。若选用图①和图②进行实验,可观察到的现象为 。若选用图③进行实验,X与Y溶液能发生反应,其反应的化学方程式为 。由实验四可得出结论:金属活动性强弱为:Al>Cu。

回答下列问题:
(1)实验一中碟子底部出现黑色物质,该实验说明了 。
(2)实验二中低处蜡烛先熄灭,高处蜡烛后熄灭,说明二氧化碳具有的物理性质是 ,具有的化学性质是 。
(3)实验三的实验目的是 。
(4)实验四的实验目的是比较铝和铜的金属活动性强弱。若选用图①和图②进行实验,可观察到的现象为 。若选用图③进行实验,X与Y溶液能发生反应,其反应的化学方程式为 。由实验四可得出结论:金属活动性强弱为:Al>Cu。
17.双氧水是一种常见的消毒液,它是过氧化氢的水溶液。回答下列问题:
(1)过氧化氢中氧元素的化合价为 。
(2)过氧化氢中氢元素和氧元素的质量比为 。
(3)为了测定过氧化氢溶液中溶质的质量分数。向烧杯中加入136g过氧化氢溶液,再向其中加入2g二氧化锰,至不再产生气泡为止,测得烧杯中剩余物质总质量为134.8g。
计算:
①生成氧气的质量是 g(不考虑氧气在水中的溶解)。
②过氧化氢溶液中溶质的质量分数是多少?
(1)过氧化氢中氧元素的化合价为 。
(2)过氧化氢中氢元素和氧元素的质量比为 。
(3)为了测定过氧化氢溶液中溶质的质量分数。向烧杯中加入136g过氧化氢溶液,再向其中加入2g二氧化锰,至不再产生气泡为止,测得烧杯中剩余物质总质量为134.8g。
计算:
①生成氧气的质量是 g(不考虑氧气在水中的溶解)。
②过氧化氢溶液中溶质的质量分数是多少?
18.A、B、C、D、E是初中化学常见的物质。其中D是一种常见的温室气体,E溶液能使紫色石蕊变红。A、B、C、D、E之间的关系如图所示。反应条件、部分反应物和生成物已略去,“一”表示相连的两种物质之间可以发生反应,“→”表示物质的转化关系。

(1)写出下列物质的化学式:D ;E 。
(2)若A、B均为黑色固体,则A的化学式为 ;B与D的反应属于 (填“放热”或“吸热”)反应。
(3)若A、B、C均为化合物,且A的阴离子与大理石主要成分的阴离子相同,则A的化学式为 ,B与C反应的化学方程式为 。

(1)写出下列物质的化学式:D ;E 。
(2)若A、B均为黑色固体,则A的化学式为 ;B与D的反应属于 (填“放热”或“吸热”)反应。
(3)若A、B、C均为化合物,且A的阴离子与大理石主要成分的阴离子相同,则A的化学式为 ,B与C反应的化学方程式为 。
19.立德粉(ZnS•BaSO4)是一种常用白色颜料,以重晶石(BaSO4)为原料生产立德粉的主要工艺流程如图:
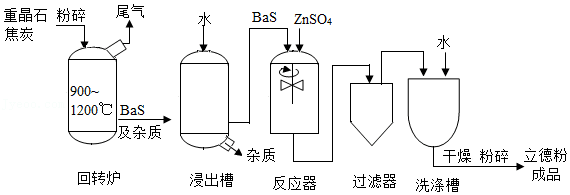
资料:BaS可溶于水,ZnS和BaSO4均难溶于水。
(1)重晶石与焦炭加入回转炉前先粉碎的目的是 。回转炉中,重晶石(BaSO4)与焦炭在高温下焙烧制得BaS,其反应的化学方程式为BaSO4+4C
4X↑+BaS,则X的化学式为 。
(2)反应器中发生的化学反应属于基本反应类型中的 反应。
(3)上述流程中,主要用于分离、提纯的设备有浸出槽、 和洗涤槽。

资料:BaS可溶于水,ZnS和BaSO4均难溶于水。
(1)重晶石与焦炭加入回转炉前先粉碎的目的是 。回转炉中,重晶石(BaSO4)与焦炭在高温下焙烧制得BaS,其反应的化学方程式为BaSO4+4C
| 高温 |
(2)反应器中发生的化学反应属于基本反应类型中的 反应。
(3)上述流程中,主要用于分离、提纯的设备有浸出槽、 和洗涤槽。
20.小明从实验室向老师借了如图所示的仪器完成实验。
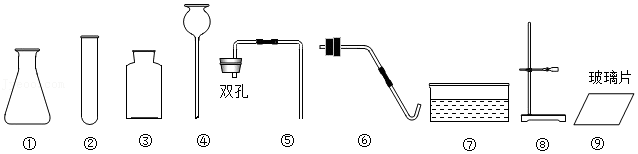
回答下列问题:
(1)仪器①的名称是 。
(2)利用氯酸钾和二氧化锰来制取并收集O2,选择组装实验装置所需的仪器是 (填序号)。为完成该实验,装置中还必需添加一种仪器,其名称为 。该反应的化学方程式为 。
(3)利用石灰石和盐酸制取、收集并检验CO2。
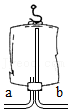
①用如图所示充满空气的医用塑料袋收集二氧化碳,则二氧化碳应从 (填“a”或“b”)端通入。
②将产生的CO2通入澄清石灰水溶液,未出现浑浊现象,可能的原因是 。

回答下列问题:
(1)仪器①的名称是 。
(2)利用氯酸钾和二氧化锰来制取并收集O2,选择组装实验装置所需的仪器是 (填序号)。为完成该实验,装置中还必需添加一种仪器,其名称为 。该反应的化学方程式为 。
(3)利用石灰石和盐酸制取、收集并检验CO2。

①用如图所示充满空气的医用塑料袋收集二氧化碳,则二氧化碳应从 (填“a”或“b”)端通入。
②将产生的CO2通入澄清石灰水溶液,未出现浑浊现象,可能的原因是 。
21.(1)三星堆考古再次成为考古界的热点。此次考古出土了大量的青铜器、象牙等文物。青铜是铜、锡、铅组成的合金。青铜器中的铜在氯离子等作用下,生成活性很强的氯化亚铜(CuCl)。氯化亚铜易与氧气、水反应生成氯化氢和碱式氯化铜[化学式为Cu2(OH)3Cl],其反应的化学方程式为 。去除文物表面的Cl﹣是保护青铜器文物的重要手段。
同学们发现生活中铜制品长期露置在潮湿空气中也会锈蚀,生成“铜绿”[化学式为Cu2(OH)2CO3]。为探究生活中某铜样品的锈蚀程度(即该铜样品中单质铜的质量分数),并回收铜。
查间资料:①Cu2(OH)2CO3+2H2SO4═2CuSO4+CO2↑+3H2O
②Cu2O+H2SO4═CuSO4+Cu+H2O
实验设计:取铜样品(假设除铜和铜绿外,不含其它物质),设计甲、乙两方案。
方案甲:
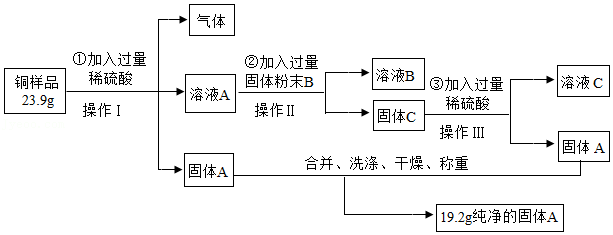
(2)操作Ⅰ、Ⅱ、Ⅲ的名称是 ,该操作中都要用到玻璃棒,其作用是 。
(3)若溶液B为浅绿色,任写一个步骤②中发生反应的化学方程式 。
(4)溶液C中的金属离子 (填离子符号)。
方案乙:
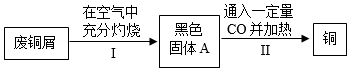
(5)步骤Ⅰ中铜绿受热分解生成黑色固体A、CO2和H2O,还发生另一个化合反应也生成黑色固体A,黑色固体A的化学式为 。
(6)步骤Ⅱ所得铜中往往含有少量的Cu2O。检验铜中含有Cu2O的实验方法为
(填实验步骤,实验现象)。
数据处理:
(7)①根据方案甲中数据可知,铜样品中单质铜的质量分数为 (小数点保留到0.1%)。
②利用方案乙还原16.0g黑色固体A,得到Cu和Cu2O的混合物共ag。则a的取值范围为 <a<14.4g。
反思评价:
(8)方案乙的主要缺点为 (任写一条)。
同学们发现生活中铜制品长期露置在潮湿空气中也会锈蚀,生成“铜绿”[化学式为Cu2(OH)2CO3]。为探究生活中某铜样品的锈蚀程度(即该铜样品中单质铜的质量分数),并回收铜。
查间资料:①Cu2(OH)2CO3+2H2SO4═2CuSO4+CO2↑+3H2O
②Cu2O+H2SO4═CuSO4+Cu+H2O
实验设计:取铜样品(假设除铜和铜绿外,不含其它物质),设计甲、乙两方案。
方案甲:

(2)操作Ⅰ、Ⅱ、Ⅲ的名称是 ,该操作中都要用到玻璃棒,其作用是 。
(3)若溶液B为浅绿色,任写一个步骤②中发生反应的化学方程式 。
(4)溶液C中的金属离子 (填离子符号)。
方案乙:

(5)步骤Ⅰ中铜绿受热分解生成黑色固体A、CO2和H2O,还发生另一个化合反应也生成黑色固体A,黑色固体A的化学式为 。
(6)步骤Ⅱ所得铜中往往含有少量的Cu2O。检验铜中含有Cu2O的实验方法为
(填实验步骤,实验现象)。
数据处理:
(7)①根据方案甲中数据可知,铜样品中单质铜的质量分数为 (小数点保留到0.1%)。
②利用方案乙还原16.0g黑色固体A,得到Cu和Cu2O的混合物共ag。则a的取值范围为 <a<14.4g。
反思评价:
(8)方案乙的主要缺点为 (任写一条)。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解