下载高清试卷
【2021-2022学年浙江省绍兴市嵊州市九年级(上)期末化学试卷】-第1页
试卷格式:2021-2022学年浙江省绍兴市嵊州市九年级(上)期末化学试卷.PDF
试卷热词:最新试卷、2022年、浙江试卷、绍兴市试卷、化学试卷、九年级上学期试卷、期末试卷、初中试卷
扫码查看解析
试卷题目
1.膳食纤维能促进肠道蠕动,有利于人体健康,下列食物中膳食纤维含量最高的是( )
- A. 青菜
- B. 大米
- C. 鸡蛋
- D. 花生仁
2.操作的规范性,安全性是实验成败的关键,下列实验操作正确的是( )
- A.
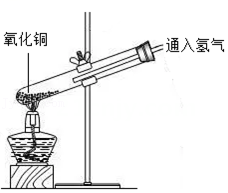 氢气还原氧化铜
氢气还原氧化铜 - B.
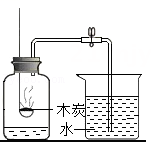 测定空气中氧气含量
测定空气中氧气含量 - C.
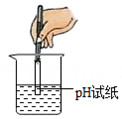 测定溶液的pH
测定溶液的pH - D.
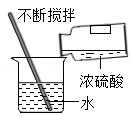 稀释浓硫酸
稀释浓硫酸
3.如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作,下列说法正确的是( )
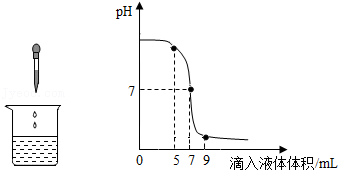

- A. 该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中
- B. 当滴入液体体积为5mL时,烧杯内溶液呈酸性
- C. 当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应
- D. 当滴入液体体积为9mL时,烧杯内溶液中的微粒有2种
4.表中所示实验操作能达到相应实验目的的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO中的少量CO2 | 通过足量的 NaOH和CaO固体 |
| B | 除去碳粉中的铁粉 | 在空气中灼烧 |
| D | 除去HCl中的少量H2SO4 | 加入足量的AgNO3溶液,过滤 |
| D | 除去NaOH 溶液中少量Na2CO3 | 加入过量的Ba(NO3)2溶液,过滤 |
- A. A
- B. B
- C. C
- D. D
5.一包固体可能由硝酸铜、硫酸钠、氯化钠、碳酸钠、氢氧化钠中的一种或几种组成。为了探究该固体的组成,某兴趣小组设计并开展以下实验。其中,步骤I中固体全部消失,溶液呈蓝色,无气泡产生,步骤II、III中均可观察到有白色沉淀生成。下列说法正确的是( )
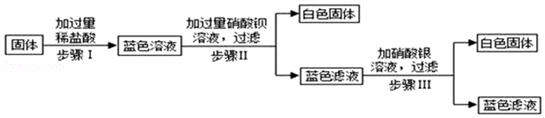

- A. 步骤Ⅰ的实验现象说明原固体中一定没有氢氧化钠
- B. 步骤Ⅱ所得的白色固体中一定含有碳酸钡
- C. 步骤Ⅱ所得蓝色滤液中含有的阳离子只有3种
- D. 原固体中一定有硝酸铜、硫酸钠,可能有氯化钠、氢氧化钠
6.纯净的二氧化硅是现代光学及光纤制品的基本原料。
(1)二氧化硅的化学性质极稳定,氢氟酸(HF)是唯一可以与之发生反应的酸(生成物为H2O和SiF4气体),该反应的化学方程式为 。
(2)二氧化硅与碳酸钙在高温下反应生成硅酸钙(CaSiO3)和二氧化碳,其中硅酸钙在物质分类上属于 (选填序号)。
①单质 ②氧化物 ③酸 ④碱 ⑤盐
(1)二氧化硅的化学性质极稳定,氢氟酸(HF)是唯一可以与之发生反应的酸(生成物为H2O和SiF4气体),该反应的化学方程式为 。
(2)二氧化硅与碳酸钙在高温下反应生成硅酸钙(CaSiO3)和二氧化碳,其中硅酸钙在物质分类上属于 (选填序号)。
①单质 ②氧化物 ③酸 ④碱 ⑤盐
7.在盐酸中加入过量的某种金属粉末,反应的微观模型如图所示,图中圆圈表示该反应前后溶液中存在的主要离子。
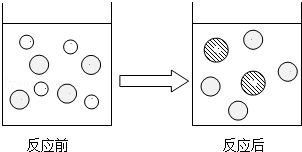
(1)下列金属中能与盐酸发生类似反应的是 。
A. Cu
B. Mg
C. Al
D. Na
(2)则“ ”所代表的离子是 (填离子符号)。
”所代表的离子是 (填离子符号)。

(1)下列金属中能与盐酸发生类似反应的是 。
A. Cu
B. Mg
C. Al
D. Na
(2)则“
 ”所代表的离子是 (填离子符号)。
”所代表的离子是 (填离子符号)。8.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水,某兴趣小组对生成物中碳的氧化物种类进行了如图所示的实验探究:
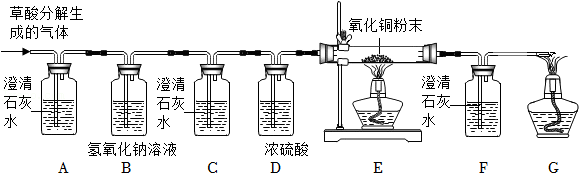
(1)若观察到 装置(填字母)中的澄清石灰水变挥浊,证明草酸分解有CO2生成。
(2)有两种实验现象都能证明草酸分解的气体中含有CO:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;②E装置中出现 的现象。
(3)G装置点燃的酒精灯的作用是 。

(1)若观察到 装置(填字母)中的澄清石灰水变挥浊,证明草酸分解有CO2生成。
(2)有两种实验现象都能证明草酸分解的气体中含有CO:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;②E装置中出现 的现象。
(3)G装置点燃的酒精灯的作用是 。
9.实验室中的试剂一般要密封保存,否则可能会与空气接触而变质.某研究性学习小组发现一瓶未密闭的NaOH固体,对其成分提出以下假设,并完成了实验探究.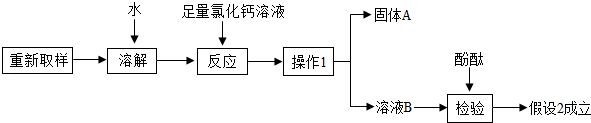
假设1:只含NaOH; 假设2:含NaOH和Na2CO3; 假设3:只含Na2CO3
(1)取少量样品于试管中,加入足量稀盐酸,观察到 ,说明假设1不成立,假设2或假设3成立.
(2)进一步探究的过程如下:
①“操作1”的名称是 ,其中要用到玻璃棒,其作用是 .
②加入足量CaCl2溶液的作用是 .
③加酚酞检验“溶液B”的现象是 .

假设1:只含NaOH; 假设2:含NaOH和Na2CO3; 假设3:只含Na2CO3
(1)取少量样品于试管中,加入足量稀盐酸,观察到 ,说明假设1不成立,假设2或假设3成立.
(2)进一步探究的过程如下:
①“操作1”的名称是 ,其中要用到玻璃棒,其作用是 .
②加入足量CaCl2溶液的作用是 .
③加酚酞检验“溶液B”的现象是 .
10.影响化学反应速率的因素有多种,如锌和稀硫酸反应的速率与锌粒的大小、硫酸溶液的溶质质量分数等有关。在实验过程中,小明发现添加少量硫酸铜溶液也能加快反应。硫酸铜溶液量的多少会影响反应速度吗?
在6支试管中分别加入2颗大小形状都相同的锌粒,倒入等质量的同种硫酸。按如表所示条件进行实验。并测量收集50毫升氢气所用的时间。记录如下:
(1)为确认反应速率的变化是由于硫酸铜溶液量的多少而引起的,C试管中所加水的体积为 毫升。
(2)分析上表数据可知,CuSO4溶液量的增加对锌和稀硫酸反应速率的影响是 。
(3)加入的CuSO4能与Zn发生置换反应生成铜,但无法解释CuSO4溶液的量为什么会影响反应速率。小明查阅资料发现以下观点,其中能作为支持加快反应速率的证据有 。
A.CuSO4溶液和Zn发生的化学反应是放热反应
B.CuSO4溶液和Zn反应生成的铜覆盖在锌粒的表面
C.过量的CuSO4溶液会使硫酸溶液的质量分数变小
D.反应生成的铜能使酸中的H+更容易得到电子变为H2
在6支试管中分别加入2颗大小形状都相同的锌粒,倒入等质量的同种硫酸。按如表所示条件进行实验。并测量收集50毫升氢气所用的时间。记录如下:
| 试管编号 | A | B | C | D | E | F |
| 加入 CuSO4稀溶液的体积/毫升 | 0 | 0.5 | 1 | 1.5 | 2 | 4 |
| 加入水的体积/毫升 | 4 | 3.5 | 2.5 | 2 | 0 | |
| 收集50毫升H2所用的时间/秒 | 348 | 246 | 190 | 165 | 230 | 360 |
(1)为确认反应速率的变化是由于硫酸铜溶液量的多少而引起的,C试管中所加水的体积为 毫升。
(2)分析上表数据可知,CuSO4溶液量的增加对锌和稀硫酸反应速率的影响是 。
(3)加入的CuSO4能与Zn发生置换反应生成铜,但无法解释CuSO4溶液的量为什么会影响反应速率。小明查阅资料发现以下观点,其中能作为支持加快反应速率的证据有 。
A.CuSO4溶液和Zn发生的化学反应是放热反应
B.CuSO4溶液和Zn反应生成的铜覆盖在锌粒的表面
C.过量的CuSO4溶液会使硫酸溶液的质量分数变小
D.反应生成的铜能使酸中的H+更容易得到电子变为H2
11.某化肥厂以“钾泻盐”(MgSO4•KCl•nH2O)为原料制造高质量钾肥,化肥中KCl含量的高低会直接影响着化肥的品质。某兴趣小组为了测定“钾泻盐”中KCl的质量分数及n的值,设计了如下两种实验方案:
方案一:如图所示: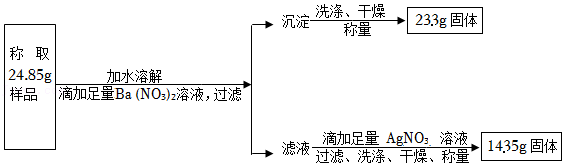
方案二:如图所示:

试可答下列问题:
(1)加入足量AgNO3溶液后,方案二中生成固体的质量大于方案一,原因是方案二中所得28.7克固体物质中除生成了 外,还生成了微溶的Ag2SO4。
(2)方案一中,滴加足量的Ba(NO3)2溶液,过滤后所得滤液中除可能含有Ba(NO3)2外,一定含有的溶质是 。
(3)该钾泻盐样品中KCl的质量分数为多少?(精确到1%)
(4)该钾泻盐化学式中n的值是多少?(要写出计算过程)
方案一:如图所示:

方案二:如图所示:

试可答下列问题:
(1)加入足量AgNO3溶液后,方案二中生成固体的质量大于方案一,原因是方案二中所得28.7克固体物质中除生成了 外,还生成了微溶的Ag2SO4。
(2)方案一中,滴加足量的Ba(NO3)2溶液,过滤后所得滤液中除可能含有Ba(NO3)2外,一定含有的溶质是 。
(3)该钾泻盐样品中KCl的质量分数为多少?(精确到1%)
(4)该钾泻盐化学式中n的值是多少?(要写出计算过程)
查看全部题目
相关试卷推荐
更多热门试卷
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解