下载高清试卷
【2021年湖北省咸宁市中考化学模拟试卷(5月份)】-第1页
试卷格式:2021年湖北省咸宁市中考化学模拟试卷(5月份).PDF
试卷热词:最新试卷、2021年、湖北试卷、咸宁市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷
扫码查看解析
试卷题目
1.下列现象中,一定发生了化学变化的是( )
- A. 水杯摔碎了
- B. 壶中的水沸腾了
- C. 湿衣服变干了
- D. 剩饭变馊了
2.以下实验操作规范的是( )
- A.
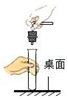 连接仪器
连接仪器 - B.
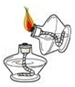 点酒精灯
点酒精灯 - C.
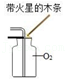 氧气的验满
氧气的验满 - D.
 倾倒液体
倾倒液体
3.下列化学方程式书写完全正确的是( )
- A. H2CO3═H2O+CO2
- B. CH4+2O2═CO2+2H2O
- C. Cu+2HCl═CuCl2+H2↑
- D. CaO+H2O═Ca(OH)2
4.有下列说法:①活性炭在净水中起着吸附和消毒作用;②铁在空气中燃烧火星四射,生成黑色固体;③水蒸发为水蒸气是因为分子的体积变大;④元素周期表有7个周期,18个族;⑤尿素、硝酸钾都属于复合肥;⑥二氧化碳是由一个碳原子和二个氧原子构成的;⑦消防队员用高压水枪来灭火是利用了降低温度到可燃物着火点以下的原理。其中正确的组合是( )
- A. ②③⑥⑦
- B. ①④⑤⑥
- C. ③⑥⑦
- D. 只有⑦
5.下列化学用语与所表达的意义对应正确的是( )
- A. Ne——氖气
- B.
 ——镁离子的结构图
——镁离子的结构图 - C. Fe2+——铁离子
- D. N2——2 个氮原子
6.如图为甲、乙、丙三种固体物质的溶解度曲线。下列说法正确的是( )
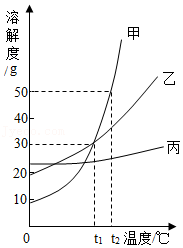

- A. 甲物质的溶解度大于乙物质的溶解度
- B. t2℃时,甲物质的溶液中溶剂与溶质的质量比为2:1
- C. 现有t1℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是:甲=乙>丙
- D. 若甲中含有少量丙,可用蒸发结晶的方法提纯甲
7.在一个密闭的容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的说法正确的是( )
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 4 | 2 | 18 | 16 |
| 反应后的质量(g) | 14 | m | 10 | 14 |
- A. 该反应的基本类型为分解反应
- B. 物质Y一定是反应的催化剂
- C. 若Z和W的相对分子质量之比为2:1,则化学方程式中它们的化学计量数之比为2:1
- D. 反应生成的X的质量为14g
8.归纳推理是一种重要的思维方法,下列归纳推理正确的是( )
- A. 常温下,pH大于7的溶液呈碱性,则碱性溶液的pH一定大于7
- B. 酸溶液能使紫色石蕊溶液变红,所以能使紫色石蕊变红的溶液一定是酸溶液
- C. 饱和的澄清石灰水变浑浊一定发生了化学变化
- D. 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
9.芯片是电脑、手机等智能家电的核心部件,它是以高纯度的单质硅(Si)为材料制成的。硅及其氧化物能发生如下反应:①Si+O2
SiO2②SiO2+Na2CO3
Na2SiO3+CO2↑③SiO2+2C
Si+2CO↑④Si+2NaOH+H2O
Na2SiO3+2X↑,下列说法不正确的是( )
| △ |
| 高温 |
| 高温 |
| △ |
- A. 反应①属于化合反应,反应③属于置换反应
- B. 上述四个反应中共涉及到6种不同的氧化物,反应④中X物质的化学式为H2O
- C. 上述反应②中各元素的化合价都没有发生改变
- D. Si和SiO2在一定条件下可以相互转化
10.20g Fe2O3和CuO的混合物与200g某硫酸溶液恰好完全反应后,再滴加100g 24%的NaOH溶液至恰好沉淀完全。则所用硫酸溶液溶质的质量分数为( )
- A. 9.8%
- B. 14.7%
- C. 19.6%
- D. 29.4%
11.化学基础与常识。
(1)如图,超市手推车各部件中,由有机合成材料制成的是把手和 。

(2)保持二氧化硫化学性质的最小微粒是 (填符号)。
(3)工业生产硫酸中的某一步反应用微观模型图表示如图:
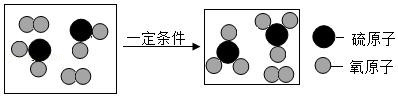
参加反应的反应物间分子个数比是 。
(4)钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为FeTO3)制备钛的流程如图:
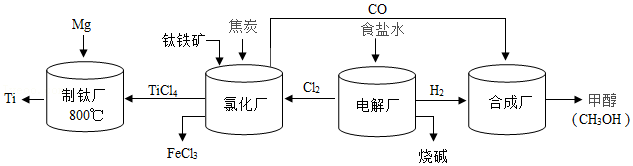
①钛酸亚铁(FeTiO3)不属于 (双项选择,填序号)。
A、化合物
B、有机物
C、纯净物
D、单质
②电解厂参加反应的物质为 。
(1)如图,超市手推车各部件中,由有机合成材料制成的是把手和 。

(2)保持二氧化硫化学性质的最小微粒是 (填符号)。
(3)工业生产硫酸中的某一步反应用微观模型图表示如图:

参加反应的反应物间分子个数比是 。
(4)钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为FeTO3)制备钛的流程如图:

①钛酸亚铁(FeTiO3)不属于 (双项选择,填序号)。
A、化合物
B、有机物
C、纯净物
D、单质
②电解厂参加反应的物质为 。
12.化学与生活紧密相连,请运用化学知识回答以下问题。
(1)在煤炉上放一壶水不能防止一氧化碳中毒,原因是 (用文字解释)。
(2)水通电的反应 (化学方程式表示)。
(3)生活中人们可用稀硫酸除铁锈,其原理是 (化学方程式表示)。
(4)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分为CaCO3和Mg(OH)2],可以用盐酸来洗涤,写出其中发生的中和反应 (化学方程式表示)。
(5)工业上可用Cl2与NaOH溶液作用制漂白液:Cl2+2NaOH═NaCl+NaClO+H2O。与此类似,可用Cl2与石灰乳[主要成分Ca(OH)2]制漂白粉,试写出此反应的化学方程式 。
(1)在煤炉上放一壶水不能防止一氧化碳中毒,原因是 (用文字解释)。
(2)水通电的反应 (化学方程式表示)。
(3)生活中人们可用稀硫酸除铁锈,其原理是 (化学方程式表示)。
(4)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分为CaCO3和Mg(OH)2],可以用盐酸来洗涤,写出其中发生的中和反应 (化学方程式表示)。
(5)工业上可用Cl2与NaOH溶液作用制漂白液:Cl2+2NaOH═NaCl+NaClO+H2O。与此类似,可用Cl2与石灰乳[主要成分Ca(OH)2]制漂白粉,试写出此反应的化学方程式 。
13.有限的元素可组成种类繁多的物质,依据表中的元素回答下列问题。
(1)若某物质为厨房里的常见调味品,则它可以是 (填化学式)。
(2)若某物质是磁铁矿的主要成分,则该物质是 (填名称)
(3)两种黑色固体物质发生反应可以生成一种红色物质,该反应方程式为 。
(4)A、B、C、D、E是五种不同类别的常见物质,且都由表中的元素组成。其中A被认为是最理想的清洁、高能燃料。D物质是一种最常用的溶剂,B物质可用于玻璃、造纸、纺织、洗涤剂的生产等。图中“→”表示物质间的转化关系(注:转化过程中所涉及到的物质均要求由上表中的元素组成),部分反应物、生成物及反应条件已略去。
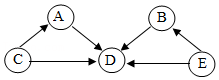
①请写出C→A的反应方程式 。
②若E→D的反应不属于任何基本反应类型,则方程式为 。
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 铜 | 钠 | 铁 |
| 元素符号 | H | C | O | Cl | Cu | Na | Fe |
(1)若某物质为厨房里的常见调味品,则它可以是 (填化学式)。
(2)若某物质是磁铁矿的主要成分,则该物质是 (填名称)
(3)两种黑色固体物质发生反应可以生成一种红色物质,该反应方程式为 。
(4)A、B、C、D、E是五种不同类别的常见物质,且都由表中的元素组成。其中A被认为是最理想的清洁、高能燃料。D物质是一种最常用的溶剂,B物质可用于玻璃、造纸、纺织、洗涤剂的生产等。图中“→”表示物质间的转化关系(注:转化过程中所涉及到的物质均要求由上表中的元素组成),部分反应物、生成物及反应条件已略去。

①请写出C→A的反应方程式 。
②若E→D的反应不属于任何基本反应类型,则方程式为 。
14.在100g的某盐酸中加入硝酸银溶液,反应为AgNO3+HCl═HNO3+AgCl↓,至恰好完全反应,经过滤、洗涤、干燥、称量得到质量为28.7g的AgCl沉淀,求盐酸的溶质质量分数。
15.实验室常用如图所示的装置制取气体和气体性质的验证。请回答:
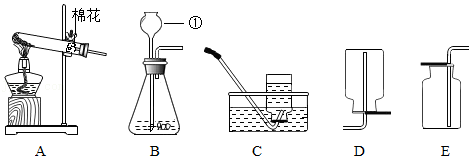
(1)仪器①的名称为 。
(2)实验室里若用A、C装置组合制取并收集氧气,其反应的原理为 (用化学方程式表示)。
(3)实验室制取二氧化碳气体,应选择的发生装置和最佳收集装置是 。
(4)实验室只能用D收集氨气,由此说明氨气具有的物理性质是 。

(1)仪器①的名称为 。
(2)实验室里若用A、C装置组合制取并收集氧气,其反应的原理为 (用化学方程式表示)。
(3)实验室制取二氧化碳气体,应选择的发生装置和最佳收集装置是 。
(4)实验室只能用D收集氨气,由此说明氨气具有的物理性质是 。
16.碳酸氢钠在日常生活中有广泛的用途,工业上制取它有多种方法,其中有一种是气相固碳法,反应的原理是:Na2CO3+H2O+CO2═2NaHCO3。
【实验操作】某实验小组在室温为15℃时,将10g氢氧化钠固体完全溶解溶于80g水中(见图1烧杯),而后匀速的通入CO2,同时用传感器测定溶液的pH变化,同时用数据采集器记录并绘制图象如图2所示。
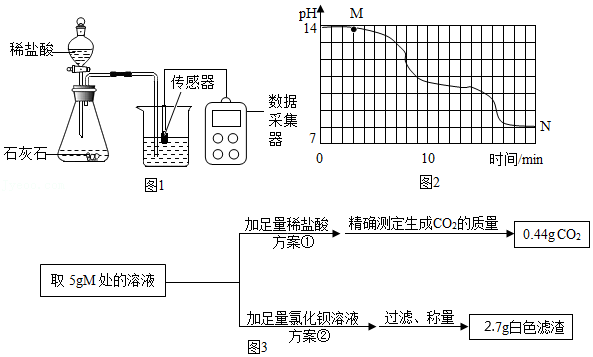
【实验问题及分析】
(1)图1锥形瓶中发生的反应为 (方程式表示)。
(2)通过图2分析,①NaOH溶液、②Na2CO3溶液、③NaHCO3溶液的酸碱度由小到大的顺序为 (填序号)。
(3)为了确定M处溶液的成分,小组中的李刚同学进行如下实验:
针对小刚同学的探究过程,有同学认为他得出的结论不可靠,理由是 。为了形成正确的结论,你的改进意见为: 。
【数据处理】小组同学想进一步探究M点处溶液中碳酸钠的质量分数,设计了两套不同的方案进行实验并测得数据如图3。
(4)根据方案①所得数据,计算M点处溶液中碳酸钠的质量分数为 。
【实验反思】
(5)另一组同学根据方案②所得数据计算出的碳酸钠质量分数与方案①相比明显偏大,你分析其中的可能原因是 。
【实验操作】某实验小组在室温为15℃时,将10g氢氧化钠固体完全溶解溶于80g水中(见图1烧杯),而后匀速的通入CO2,同时用传感器测定溶液的pH变化,同时用数据采集器记录并绘制图象如图2所示。

【实验问题及分析】
(1)图1锥形瓶中发生的反应为 (方程式表示)。
(2)通过图2分析,①NaOH溶液、②Na2CO3溶液、③NaHCO3溶液的酸碱度由小到大的顺序为 (填序号)。
(3)为了确定M处溶液的成分,小组中的李刚同学进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量M点处溶液于试管中,加入适量的氢氧化钡溶液 | 产生白色沉淀 | M点处溶液中含有碳酸钠和氢氧化钠 |
| ②取上述步骤①试管中的少量上层清液,滴加几滴酚酞溶液。 | 发现溶液变红 |
针对小刚同学的探究过程,有同学认为他得出的结论不可靠,理由是 。为了形成正确的结论,你的改进意见为: 。
【数据处理】小组同学想进一步探究M点处溶液中碳酸钠的质量分数,设计了两套不同的方案进行实验并测得数据如图3。
(4)根据方案①所得数据,计算M点处溶液中碳酸钠的质量分数为 。
【实验反思】
(5)另一组同学根据方案②所得数据计算出的碳酸钠质量分数与方案①相比明显偏大,你分析其中的可能原因是 。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解