下载高清试卷
【2021年安徽省亳州市中考化学一模试卷】-第1页
试卷格式:2021年安徽省亳州市中考化学一模试卷.PDF
试卷热词:最新试卷、2021年、安徽试卷、亳州市试卷、化学试卷、九年级试卷、中考模拟试卷、初中试卷

扫码查看解析
试卷题目
1.我国古代科技发展卓著,下列成果的应用中涉及化学变化的是( )
- A.

玉石雕刻 - B.

甲骨刻字 - C.

粮食酿酒 - D.

活字印刷
2.2020年4月22日是第51个世界地球日,主题是“珍爱地球,人与自然和谐共生”。下列行为符合这一活动主题的是( )
- A. 为降低成本,工业废水直接排放
- B. 注意个人卫生,提倡使用一次性木筷
- C. 采用绿色化学工艺,使原料尽可能转化为产品
- D. 垃圾全是无用物质,为方便处理,全部焚烧去除
3.下列各项警示标识与存放的物质不相符合的是( )
- A.

甲醛 - B.

酒精 - C.

烧碱 - D.

浓硫酸
4.化学来源于生活应用于生活。下列物质的用途不正确的是( )
- A. 活性炭用作冰箱除味剂
- B. 氧气用于潜水和医疗急救
- C. 熟石灰用作干燥剂
- D. 碳酸氢钠可用于糕点焙制
5.中成药连花清瘟胶囊在防治新冠肺炎中作用显著,其主要成分之一的绿原酸的分子式为C16H18O9。下列有关说法不正确的是( )
- A. 绿原酸含有三种非金属
- B. 一个绿原酸分子中含有43个原子
- C. 绿原酸分子中碳、氢原子个数之比为8:9
- D. 绿原酸不属于氧化物
6.下列实验操作中正确的是( )
- A.

倾倒液体 - B.

点燃酒精灯 - C.

读体积 - D.

测水温
7.氮化镓是新一代半导体材料。氮、镓的原子结构示意图和它们在元素周期表中的信息如图所示,下列说法正确的是( )
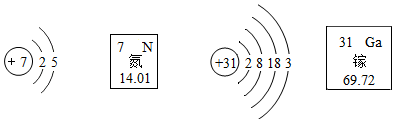

- A. 氮化镓的化学式为GaN
- B. 镓元素的相对原子质量是31
- C. 氮元素和镓元素位于同一周期
- D. 1个N2分子中含有7个电子
8.课本中用加入少量Na2SO4的水进行电解水实验,从该实验中不能获取的信息是( )
- A. 纯水的导电能力弱
- B. 负极产生气体的速率比正极快
- C. 常温下,水的pH=7
- D. 水由氢元素和氧元素组成
9.中国化学家使用特殊的催化剂实现了CO2和H2转化为A或B等有机物的反应,原理如图所示,下列说法不正确的是( )


- A. 此方法实现了由无机物向有机物转化的重要的战略意义
- B. 该反应前后原子种类和数目没有改变
- C. 在催化剂Ⅰ中发生反应的化学方程式为CO2+H2CO+H2O
Fe3O4 - D. 反应前后两种催化剂的质量和性质都不变
10.归纳推理是学习化学的一种重要的思维方法,下列归纳推理正确的是( )
- A. 化合物有由多种元素组成的,则有多种元素组成的物质一定是化合物
- B. 常温下,pH大于7的溶液呈碱性,则碱性溶液的pH一定大于7
- C. 置换反应有单质生成,则有单质生成的反应一定是置换反应
- D. 铝和稀硫酸反应会产生硫酸铝和氢气,则所以铁和稀硫酸反应产生硫酸铁和氢气
11.将纯净的氯化钠固体配制成溶液。20℃时,向4个盛有50g水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4组实验数据如表:下列分析错误的是( )
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 10 | 15 | 20 | 25 |
| 溶液质量/g | 60 | 65 | 68 | 68 |
- A. ①②所得溶液时20℃时氯化钠的不饱和溶液
- B. ③④所得溶液的溶质质量分数相等
- C. 20℃时,氯化钠的溶解度为36g
- D. 20℃时,往②所得溶液加入2g氯化钠,溶液达到饱和
12.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是( )


- A. 甲中逸出的气体只含CO2
- B. 乙中液体变红,证明CO2能与水反应
- C. 加热后红色不褪去,说明碳酸受热不分解
- D. 欲达到实验目的,可将盐酸改为稀硫酸
13.阅读下列科技短文,回答问题。
说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物,其实你真的了解SO2吗?难道它只是有害物质吗?
一、SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业,葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,食糖加工过程中可使用SO2进行脱色,按照我国《食品添加剂使用标准(GB2760-2014)》,合理使用SO2不会对人体健康造成危害。
二、SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化,工业利用硫制硫酸的主要过程示意如图:

硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,工业上可先用氨水吸收,再用硫酸处理,将重新生成的SO2循环利用,工业上也可将熟石灰制成石灰乳吸收二氧化硫生成亚硫酸钙(CaSO4)。
三、SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2,为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量,改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理,还可以采取“优化能源结构、减少燃煤使用”的措施,例如“煤改气、煤改电”工程,有效改善了空气质量。
(1)葡萄酒酿制过程中SO2的作用是 。
(2)用硫制硫酸的主要过程中,其中H2SO4中硫元素的化合价为 。
(3)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨。我们把pH< ,称为酸雨。工业上用石灰乳吸收二氧化硫反应的化学方程式为 。
(4)下列措施能减少SO2排放的是 (填序号)。
A.将煤块粉碎
B.对燃煤进行脱硫处理
C.推广煤改气、煤改电
D.循环利用工业尾气中的SO2
说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物,其实你真的了解SO2吗?难道它只是有害物质吗?
一、SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业,葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,食糖加工过程中可使用SO2进行脱色,按照我国《食品添加剂使用标准(GB2760-2014)》,合理使用SO2不会对人体健康造成危害。
二、SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化,工业利用硫制硫酸的主要过程示意如图:

硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,工业上可先用氨水吸收,再用硫酸处理,将重新生成的SO2循环利用,工业上也可将熟石灰制成石灰乳吸收二氧化硫生成亚硫酸钙(CaSO4)。
三、SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2,为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量,改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理,还可以采取“优化能源结构、减少燃煤使用”的措施,例如“煤改气、煤改电”工程,有效改善了空气质量。
(1)葡萄酒酿制过程中SO2的作用是 。
(2)用硫制硫酸的主要过程中,其中H2SO4中硫元素的化合价为 。
(3)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨。我们把pH< ,称为酸雨。工业上用石灰乳吸收二氧化硫反应的化学方程式为 。
(4)下列措施能减少SO2排放的是 (填序号)。
A.将煤块粉碎
B.对燃煤进行脱硫处理
C.推广煤改气、煤改电
D.循环利用工业尾气中的SO2
14.气体制备、收集是初中化学的重要知识。请你结合如图,回答有关问题。

(1)写出图中仪器①的名称: 。
(2)实验室用氯酸钾制取氧气应选择的发生装置是 (填字母),写出反应的化学方程式: 。
(3)下列哪种方法可以得到平稳的氧气流? (填序号)。
①把二氧化锰加入装有过氧化氢溶液的试管中
②把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
(4)下列不能用E装置收集的气体是 (填序号)。
①CO2
②O2
③H2
④SO2

(1)写出图中仪器①的名称: 。
(2)实验室用氯酸钾制取氧气应选择的发生装置是 (填字母),写出反应的化学方程式: 。
(3)下列哪种方法可以得到平稳的氧气流? (填序号)。
①把二氧化锰加入装有过氧化氢溶液的试管中
②把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
(4)下列不能用E装置收集的气体是 (填序号)。
①CO2
②O2
③H2
④SO2
15.氧化镁是医疗上的一种常用药剂,通常与氢氧化铝合用,主要用于治疗伴有便秘的胃酸过多等症,以镁矿石(主要成分MgCO3、SiO2)为原料生产MgO的工艺流程如图所示。已知SiO2难溶于水和常见的酸。

(1)酸浸前将镁矿粉粉碎的目的是 。
(2)滤渣X的主要成分是 。
(3)沉淀过程中MgSO4与NH3•H2O发生复分解反应,生成物中有Mg(OH)2沉淀,请写出此反应的化学方
程式 。
(4)请写出副产品Y的一种用途 。

(1)酸浸前将镁矿粉粉碎的目的是 。
(2)滤渣X的主要成分是 。
(3)沉淀过程中MgSO4与NH3•H2O发生复分解反应,生成物中有Mg(OH)2沉淀,请写出此反应的化学方
程式 。
(4)请写出副产品Y的一种用途 。
16.某小组同学用如图所示装置做氧化铜与稀盐酸反应的兴趣实验,发现有的同学得到蓝色溶液,有的同学得到绿色溶液。老师提示这种现象可能与所得氯化铜溶液有关。同学们对这个现象进行探究。
实验1:探究影响氯化铜溶液颜色的因素
取溶质质量分数不同的氯化铜溶液各20mL置于同样的烧杯中,分别置于不同温度的水浴箱中加热(忽略溶剂蒸发)。待溶液温度恒定后,观察溶液颜色,记录如表:
实验2:探究室温下氯化铜溶液的变色浓度范围
a.室温下,称取15.4g的氯化铜固体溶于35.0g水中,配制成溶质质量分数30.6%的氯化铜溶液。
b.将上述氯化铜溶液依次加入等质量的水稀释,配制成不同溶质质量分数的氯化铜溶液,观察溶液颜色,记录如表:
【结果与讨论】
(1)氧化铜和稀盐酸反应的化学方程式为 。
(2)实验1中,④⑤⑥的实验目的是 。
(3)根据实验1的结果可知,③⑥⑨中影响氯化铜溶液颜色的因素是 。
【反思与评价】
(4)室温下,小文将20g氯化铜固体溶于80g水中,则此溶液的颜色为 。
(5)小昕配制了一杯质量分数为12%的氯化铜溶液,溶液为浅蓝色,若要使此溶液由蓝向绿色转变,可进行的操作有 (填字母序号)。
A.将溶液放在水浴箱中加热到70℃
B.加入适量的氯化铜固体并使之溶解
C.加入适量的水稀释
【拓展探究】如何将绿色的氯化铜溶液变为蓝色或变黄呢?

【查阅资料】
1、氯化铜溶于水后在水溶液中电离出大量的Cu2+和Cl-。
2、氯化铜溶液的颜色会随着溶液中的Cu2+与其他离子形成不同的络合离子而改变。
其中:水合铜离子[Cu(H2O)4]2+为蓝色:四氯合铜络离子[CuCl4]2-为黄色。
3、由光学知识可知:黄色光+蓝色光=绿色光
因此,氯化铜溶液变绿的原因实际上是溶液中的[Cu(H2O)4]2+和[CuCl4]2-混合形成的。
(6)【设计实验】
1、取少量绿色的氯化铜溶液,加入 。
(7)请分析,步骤2中加入稀盐酸溶液未变黄的原因 。
(8)若将将绿色的氯化铜溶液变为黄色,可向其中加入 。
实验1:探究影响氯化铜溶液颜色的因素
取溶质质量分数不同的氯化铜溶液各20mL置于同样的烧杯中,分别置于不同温度的水浴箱中加热(忽略溶剂蒸发)。待溶液温度恒定后,观察溶液颜色,记录如表:
| 烧杯编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 溶质质量分数/% | 5 | 5 | 5 | 10 | 10 | 10 | 20 | 20 | 20 |
| 水浴箱温度/℃ | 30 | 50 | 70 | 30 | 50 | 70 | 30 | 50 | 70 |
| 溶液颜色 | 浅蓝 | 浅蓝 | 蓝 | 蓝 | 蓝绿 | 翠绿 | 蓝绿 | 翠绿 | 墨绿 |
实验2:探究室温下氯化铜溶液的变色浓度范围
a.室温下,称取15.4g的氯化铜固体溶于35.0g水中,配制成溶质质量分数30.6%的氯化铜溶液。
b.将上述氯化铜溶液依次加入等质量的水稀释,配制成不同溶质质量分数的氯化铜溶液,观察溶液颜色,记录如表:
| 溶质质量分数/% | 30.6 | 25.5 | 21.9 | 19.2 | 17.0 | 15.3 |
| 溶液颜色 | 深绿 | 翠绿 | 蓝绿 | 蓝绿 | 蓝 | 浅蓝 |
【结果与讨论】
(1)氧化铜和稀盐酸反应的化学方程式为 。
(2)实验1中,④⑤⑥的实验目的是 。
(3)根据实验1的结果可知,③⑥⑨中影响氯化铜溶液颜色的因素是 。
【反思与评价】
(4)室温下,小文将20g氯化铜固体溶于80g水中,则此溶液的颜色为 。
(5)小昕配制了一杯质量分数为12%的氯化铜溶液,溶液为浅蓝色,若要使此溶液由蓝向绿色转变,可进行的操作有 (填字母序号)。
A.将溶液放在水浴箱中加热到70℃
B.加入适量的氯化铜固体并使之溶解
C.加入适量的水稀释
【拓展探究】如何将绿色的氯化铜溶液变为蓝色或变黄呢?

【查阅资料】
1、氯化铜溶于水后在水溶液中电离出大量的Cu2+和Cl-。
2、氯化铜溶液的颜色会随着溶液中的Cu2+与其他离子形成不同的络合离子而改变。
其中:水合铜离子[Cu(H2O)4]2+为蓝色:四氯合铜络离子[CuCl4]2-为黄色。
3、由光学知识可知:黄色光+蓝色光=绿色光
因此,氯化铜溶液变绿的原因实际上是溶液中的[Cu(H2O)4]2+和[CuCl4]2-混合形成的。
(6)【设计实验】
| 目的 | 步骤 | 现象 |
| 1、将绿色的氯化铜溶液变为蓝色 | 取少量绿色的氯化铜溶液,加入________ | 溶液变蓝 |
| 2、将绿色的氯化铜溶液变为黄色 | 取少量绿色的氯化铜溶液,加入稀盐酸 | 溶液未变黄 |
1、取少量绿色的氯化铜溶液,加入 。
(7)请分析,步骤2中加入稀盐酸溶液未变黄的原因 。
(8)若将将绿色的氯化铜溶液变为黄色,可向其中加入 。
17.为测定某盐酸中溶质的质量分数,小明同学取该盐酸50g,向其中加入足量的碳酸钠粉末,完全反应后收集到6.6g气体。

(1)计算该盐酸中溶质的质量分数。
(2)小明将测定结果与标签上所示信息(标签如图)进行对比,发现测定结果与标签有偏差。若实验操作过程均无误,则引起结果偏差的原因可能是 。

(1)计算该盐酸中溶质的质量分数。
(2)小明将测定结果与标签上所示信息(标签如图)进行对比,发现测定结果与标签有偏差。若实验操作过程均无误,则引起结果偏差的原因可能是 。
查看全部题目
如何查看答案以及解析
扫描右侧二维码查看试卷答案解析以及视频讲解